上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|冠酶:DNA酶与纳米酶融合的创新成果
139 人阅读发布时间:2025-02-19 14:01
DNA聚合酶
今天要分享的是一篇2022年发表在《Journal of the American Chemical Society》上的文章,题为“Amalgamation of DNAzymes and Nanozymes in a Coronazyme”。这篇文章的通讯作者是美国肯特州立大学的茅涵斌教授和沈昊教授

酶作为一类高效的天然催化剂,具备高度的活性和对底物的专一性选择,但它们的应用受到了稳定性差、作用底物范围有限以及成本高昂等因素的制约。为了克服这些限制,科研人员开发了多种新型人工酶,包括纳米酶和DNA酶等,它们能够突破天然酶的局限。在某些研究中,纳米酶和DNA酶被结合形成复合体,类似于广泛研究的蛋白冠,DNA在纳米颗粒上的修饰能够形成DNA冠。尽管如此,DNA冠在纳米酶催化过程中的作用尚不完全明确:部分研究显示DNA冠可能阻碍纳米颗粒表面活性位点,降低催化活性;而另一些研究则发现DNA冠可能通过增强底物吸附来提升催化活性。在这项研究中,研究人员利用DNA冠包覆金纳米颗粒,将纳米酶和DNA酶融合成为一种新型人工酶——冠酶,这种冠酶展现出更高的催化效率和较好的特异性,研究人员对冠酶的催化机制进行了深入探究。
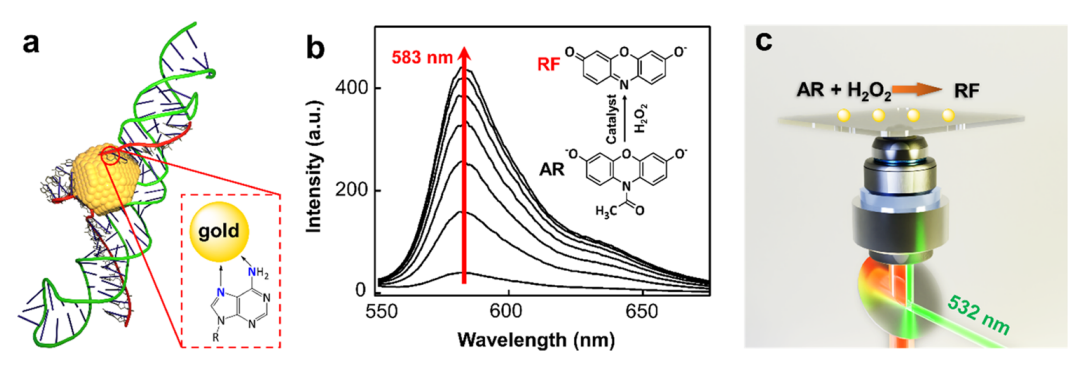
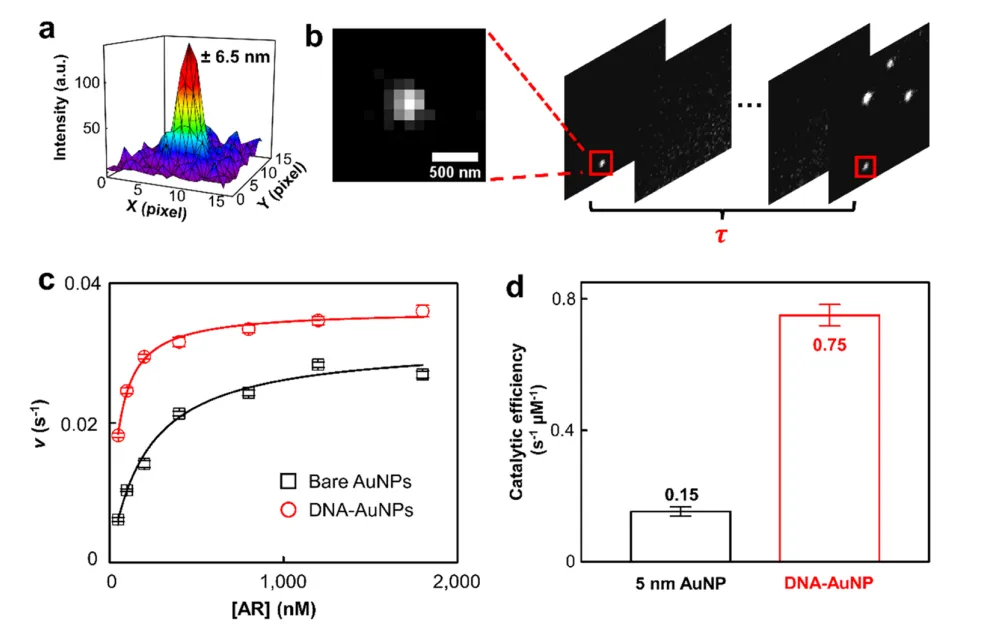
研究者们首先评估了冠酶模拟过氧化物酶活性的单分子催化能力。在此过程中,金纳米颗粒(AuNP)作为过氧化物酶的模拟物,利用AR这一荧光底物来评估冠酶的催化效能。在AuNP的催化下,AR转化为高荧光强度的分子RF,其发射波长为583 nm。研究者们进一步对这一单分子催化事件进行了超分辨率成像。具体操作是,先将纳米酶固定在微流体腔室中,然后在特定的缓冲溶液条件下观察到,由同一纳米酶催化产生的RF在相同位置反复出现荧光爆发。在35×35 mm²的视场内,对多个纳米酶进行定位,确保RF分子的荧光信号能够被准确地归属于产生它的纳米酶,即通过将每个荧光点的中心拟合为二维高斯函数,实现了10 nm级别的分辨率。在此方法中,同一纳米酶连续生成两个RF分子之间的时间间隔t,代表了单个分子反应的周转时间,通过统计多个t值得以反映纳米酶的催化活性。对于未修饰DNA的5 nm AuNP,其平均周转速率-1随AR浓度增加而增加,直至达到饱和状态,而修饰了DNA冠的AuNP(AuNP@DNA)显示出更高的平均周转速率,并且其饱和反应活性超过了原始的5 nm AuNP。综合来看,AuNP@DNA的催化效率是其母体AuNP的5倍,是目前已报道的AR氧化催化效率最高的纳米酶之一。
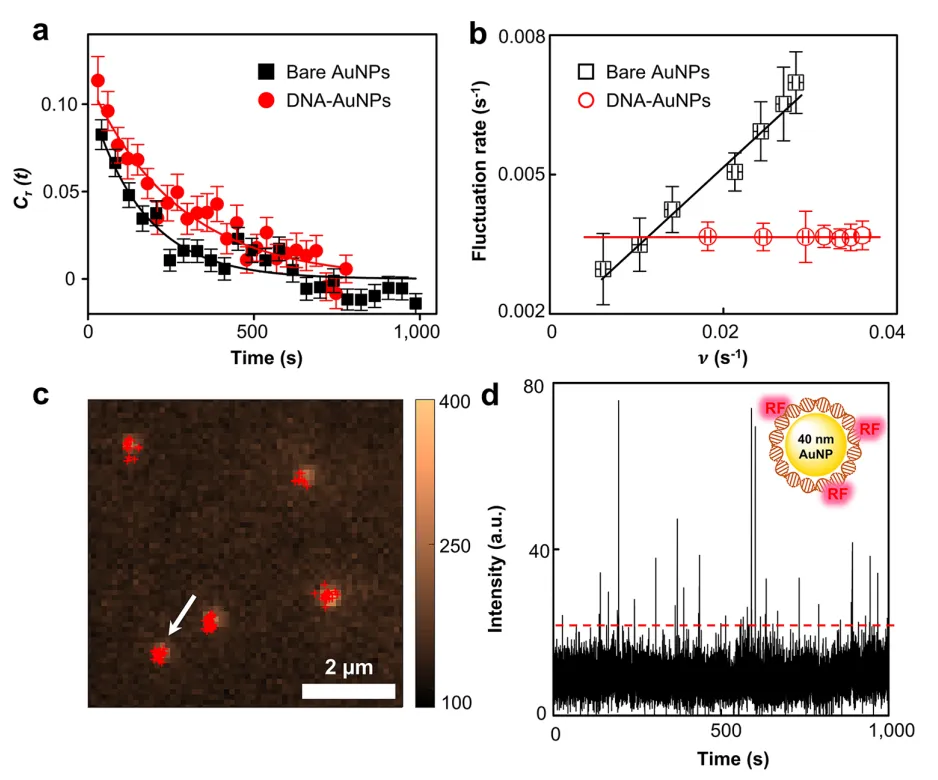
可以对AuNP@DNA的反应活性、表面重构现象、长程反应机制以及荧光猝灭现象进行更深入的解释和阐述。
AuNP@DNA的反应活性和表面重构现象:
单个AuNP@DNA的反应活性并不是稳定的,而是随时间波动,这种现象被称为“动态紊乱”。这种波动并不是随机的,而是通过检测自相关系数Ct(t)的衰减所展示出的“记忆效应”,反映出催化过程中纳米颗粒的表面重构现象。对于5 nm AuNP,其Ct(t)的变化依赖于反应周转,这是来源于它的表面与底物的相互作用,因此高浓度的底物会导致更快的反应周转速率和表面重组。
AuNP@DNA的长程反应机制:
作者提出了一种发生在DNA冠内的长程反应机制:AR的氧化反应,始于过氧化氢在AuNP上可逆的O-O键断裂所生成的羟基自由基,这些自由基氧化了邻近的DNA碱基,将其转化为自由基阳离子,当电荷接触到与DNA结合的AR后,发生电荷(空穴)的迁移。最后,AR通过两个连续的单电子转移过程转化为RF,而DNA碱基被还原到初始状态。
AuNP@DNA的荧光猝灭现象:
支持这个机制的一个直接证据是在40 nm AuNP上的荧光猝灭现象:虽然40 nm AuNP在整体上有很明显的反应活性,但由于RF的荧光在AuNP的表面被猝灭,故在单分子水平上没有观察到荧光点。然而,修饰有DNA冠的40 nm AuNP却出现了单分子荧光发射,这表明RF的形成发生在DNA冠内,而不是在AuNP表面。
AuNP@DNA的单分子荧光发射:
修饰有DNA冠的40 nm AuNP出现了单分子荧光发射,这进一步证实了RF的形成发生在DNA冠内,而不是在AuNP表面,这与长程反应机制的提出相符合。
这些发现不仅揭示了AuNP@DNA在催化过程中的动态行为,还为理解其在生物分析和生物医学中的潜在应用提供了重要的基础。
在探讨金纳米颗粒(AuNP)作为纳米酶在催化酶促反应中的应用时,研究人员发现AuNP本身对底物的特异性不高,这意味着它们可以催化多种不同的化学反应,但无法区分特定的底物。为了提高AuNP的底物特异性,研究人员进一步研究了DNA冠(DNA冠层)对AuNP催化活性的影响。
构建类脱氢酶活性的纳米酶模型:
研究人员构建了一个模拟脱氢酶活性的纳米酶模型,用于比较其催化反应与已知的AR氧化反应。
RZ和RF的催化转化:
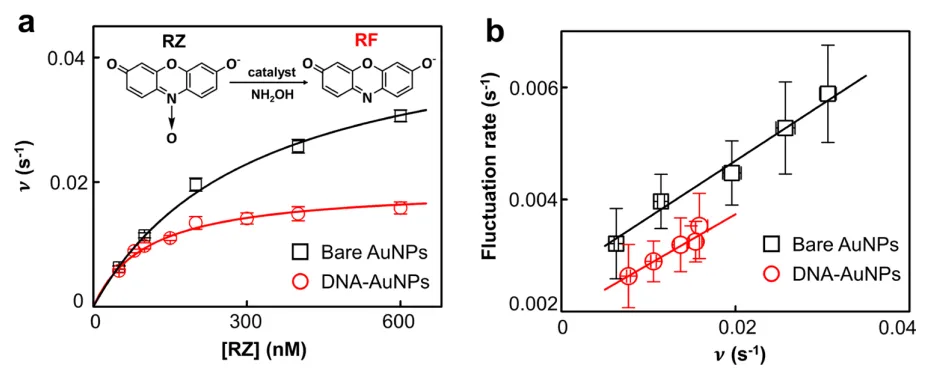
RZ是一种非荧光的吩噁嗪染料,但在纳米酶和过氧化氢(NH2OH)的存在下,可以被催化转化为荧光产物RF(图4a插图所示)。
单分子观测结果:
通过单分子观测技术,研究人员发现5 nm的AuNP在催化RZ还原和AR氧化反应中表现出相似的效率,这表明AuNP对这两种反应的催化缺乏特异性。
DNA冠对催化效率的影响:
在AuNP上加入DNA冠后,其对RZ的还原效率并没有显著提高,这表明DNA冠并不促进RZ的还原反应(图4a)。
反应活性波动分析:
对RZ还原反应的活性波动分析显示,无论是5 nm AuNP还是AuNP@DNA,RZ的还原过程都明显依赖于反应周转速率(图4b)。这表明RZ的还原主要发生在AuNP的表面,而不是DNA冠中。
DNA冠对底物接近性的影响:
DNA冠的存在可能会阻碍底物接近AuNP表面的活性位点,从而降低反应活性。
综上所述,DNA冠并没有提高AuNP对RZ还原反应的催化效率,反而可能因为阻碍底物接近活性位点而降低了反应活性。这些发现对于设计具有特定底物特异性的纳米酶具有重要意义,提示我们在设计纳米酶时需要考虑底物接近性和DNA冠对催化位点的潜在影响。
为了深入理解DNA冠如何影响AuNP的底物特异性以及催化反应的选择性,研究人员进行了密度泛函理论(DFT)计算,以探究DNA碱基对与反应底物和产物之间的相互作用能。
DFT计算结果:
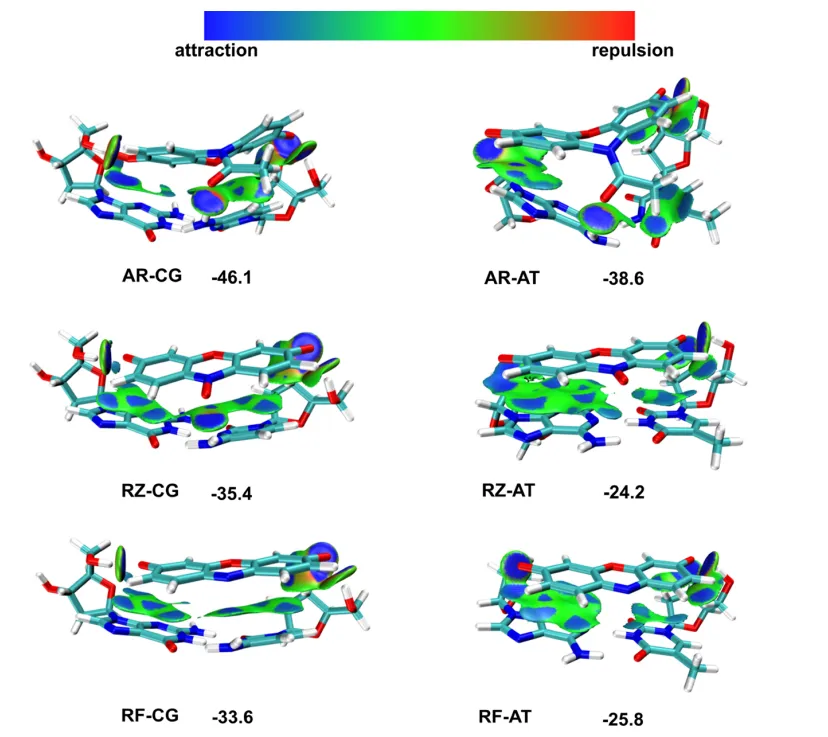
通过DFT计算,研究人员发现AR(底物)对A-T和C-G碱基对的结合能分别为-38.6和-46.1 kcal/mol,这表明AR与DNA冠之间存在强烈的吸附作用。
AR与DNA冠的相互作用:
AR与DNA冠的强烈相互作用意味着AR更倾向于与DNA冠结合,这增强了AuNP对AR的反应选择性。
RZ与DNA冠的相互作用:
相比之下,RZ(另一种底物)与DNA冠的相互作用明显较弱,这表明DNA冠对RZ的吸附作用不如AR强烈。
反应选择性的增强:
DNA冠的这种选择性吸附作用使得AuNP对AR的反应选择性增强,且反应更可能直接发生在DNA碱基上。
产物RF与DNA冠的相互作用:
对于产物RF,其与DNA冠的结合能也相对较低,这意味着在AR转化为RF的反应中,存在显著的结合能损失。
产物解离与反应正向进行:
这种结合能的损失有利于产物RF从DNA冠上解离,从而促进了反应的正向进行。
RZ还原反应的催化效率:
对于RZ转化为RF的反应,由于结合能变化不明显,因此在DNA冠存在的情况下,RZ还原的催化效率没有显著变化。
综上所述,DFT计算结果揭示了DNA冠通过选择性吸附底物AR,增强了AuNP对特定底物的反应选择性,并且这种选择性吸附作用对于产物的解离和反应的正向进行具有重要作用。这些发现对于设计具有特定底物特异性的纳米酶催化剂具有重要的指导意义。
研究人员将金纳米颗粒(AuNP)与DNA酶相结合,开发了一种新型人工酶,这种酶不仅催化效率高,而且具有优异的底物选择性。这种人工酶通过整合AuNP和DNA的结构与功能,模拟了自然界中酶的作用机制,因此被命名为“冠酶”。研究人员利用单分子荧光技术和光镊技术对冠酶进行了详细的特性分析和表征。
此外,研究还指出,通过使用不同的纳米颗粒和非DNA基的冠材料,可以设计出多种变体的冠酶。这些冠酶因其独特的催化特性和底物特异性,展现出在科研和实际应用中的巨大潜力,包括但不限于生物催化、传感、药物递送以及环境修复等多个领域。总的来说,冠酶的发现和研究为纳米生物技术和酶工程领域带来了新的思路和工具。
| 名称 | 货号 | 规格 |
| 双链DNA酶 | abs60248-50T | 50T |
| DNase Ⅰ | UA070036-1KU | 1KU |
| 脱氧核糖核酸酶Ⅰ(牛胰) | abs47047435-500mg | 500mg |
| DNAJC7 Antibody | 80718S | 100ul |



































