上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|PUMILIO蛋白:抑制p21,加速结直肠癌生长
123 人阅读发布时间:2025-03-03 13:23
PUMILIO Proteins Promote Colorectal Cancer Growth via Suppressing p21
引言
结直肠癌(CRC)作为全球最常见的恶性肿瘤之一,其发病率和死亡率居高不下,给公共卫生带来了巨大挑战。根据2018年全球流行病学数据,CRC在所有癌症中占比10%,居第三位,而死亡率则居第二位。尽管近年来在CRC的遗传和分子机制方面取得了显著进展,如APC、TP53、KRAS等基因的改变以及Wnt、RAS-MAPK、PI3K等关键信号通路的作用已被广泛研究,但CRC的发病率和死亡率依然居高不下,并呈现出上升趋势。因此,探索CRC发病机制的新分子机制,对于实现早期检测、诊断和靶向治疗至关重要。
最近的研究表明,RNA结合蛋白在CRC的起始和发展过程中扮演着重要角色。然而,这些蛋白在CRC中的确切作用以及它们如何调控CRC中的RNA靶点,在很大程度上仍是未知的。PUMILIO蛋白(PUM1和PUM2)作为一类重要的RNA结合蛋白,近年来引起了广泛关注。本文将对2022年3月25日发表在Nature Communications杂志上的一项研究进行解析,该研究由来自中国上海科技大学的Yuanyuan Gong及其团队完成,题为“PUMILIO proteins promote colorectal cancer growth via suppressing p21”。

研究背景
PUMILIO蛋白(PUM蛋白)是一类高度保守的RNA结合蛋白,最初在果蝇中被发现,并因其对Nanos mRNA的调控作用而得名。在哺乳动物中,PUM蛋白家族包括PUM1和PUM2两个成员,它们通过结合特定的mRNA序列(即Nanos响应元件,NRE),参与调控mRNA的稳定性、翻译效率和定位。近年来,越来越多的研究表明,PUM蛋白在多种人类疾病中发挥着重要作用,包括癌症、神经退行性疾病和病毒感染等。
在癌症方面,PUM蛋白的异常表达与多种肿瘤的发生和发展密切相关。例如,在乳腺癌、肺癌和前列腺癌等肿瘤中,PUM蛋白的表达水平显著升高,且其高表达与不良预后和肿瘤进展呈正相关。然而,关于PUM蛋白在CRC中的具体作用及其机制,目前仍缺乏深入研究。
研究方法
在本研究中,Yuanyuan Gong及其团队采用了多种实验方法和技术手段,系统地探讨了PUM1和PUM2在CRC中的功能和作用机制。具体方法包括:
-
数据库分析和临床样本检测:研究者首先利用两个在线数据库(人类蛋白质图谱和癌症基因组图谱TCGA)分析了PUM1和PUM2在不同肿瘤中的表达情况,并收集了来自22例CRC患者的人类CRC样本及其邻近组织,对PUM1和PUM2的mRNA表达进行了成对比较。
-
转录组测序:为了探索PUM蛋白在CRC中的分子机制,研究者利用深度测序技术分析了Pum1-/-和Pum2-/- HCT116细胞的转录组,鉴定了差异表达基因,并进行了主成分分析(PCA)以评估实验的可重复性。
-
RNA深度测序和蛋白质质谱分析:研究者进一步利用RNA深度测序和蛋白质质谱分析技术,探讨了PUM1对p21的调控作用,并验证了其在RNA和蛋白质水平上的变化。
-
RNA共免疫沉淀(RIP)实验:为了确定PUM蛋白与p21 mRNA的直接结合作用,研究者进行了RIP实验,并比较了PUM1和PUM2对p21 mRNA的富集程度。
-
动物实验:最后,研究者利用CRC模型小鼠,通过静脉注射纳米颗粒包装的抗PUM SiRNA,评估了抗PUM治疗对肿瘤生长的影响。
研究结果
- PUM1和PUM2在CRC中表达增加
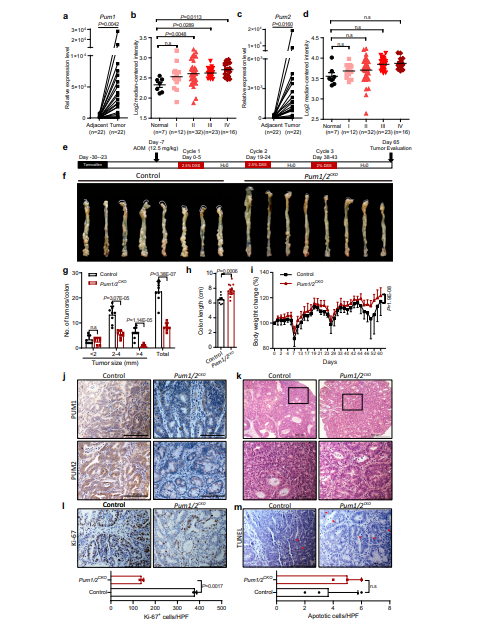
研究者首先分析了两个在线数据库中的数据,发现与其他癌症类型相比,PUM1在CRC中具有最高的蛋白质水平,并且PUM2在CRC中也高表达。进一步分析TCGA数据集显示,与正常结肠组织相比,CRC组织中Pum1的转录物表达水平较高,而Pum2的表达水平则相对较低。为了验证这一结果,研究者对来自22例CRC患者的人类CRC样本及其邻近组织中的mRNA表达进行了成对比较,发现Pum1和Pum2在CRC临床标本中高度表达。特别是,在15例患者中Pum1的mRNA水平比其配对的邻近正常组织高至少10倍,而在13例患者中Pum2的mRNA水平也呈现出类似的高表达。此外,TCGA数据集还显示,Pum1的表达与CRC阶段呈正相关,而Pum2的表达则与CRC阶段无显著相关性。受试者工作特性(ROC)曲线分析进一步表明,在CRC中,Pum1的诊断价值高于Pum2。此外,PUM1的表达与CRC患者的生存率可能存在负相关。这些数据表明,PUM1和PUM2参与了人类CRC的进展。
- PUM1主要通过直接调控癌相关基因和细胞周期相关基因发挥作用
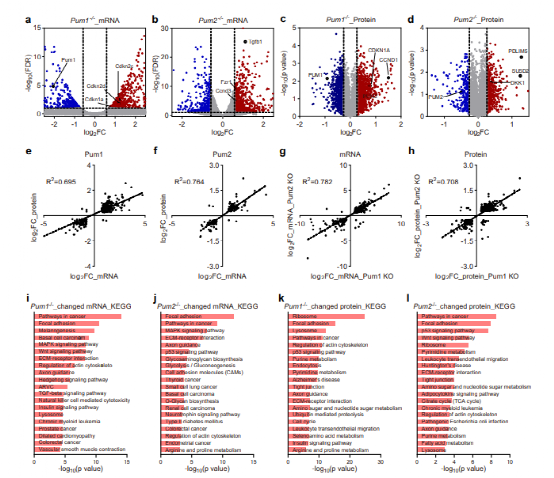
为了探索CRC中PUM功能的分子机制,研究者利用深度测序技术分析了Pum1-/-和Pum2-/- HCT116细胞的转录组。在Pum1敲除细胞中,研究者鉴定了1132个差异表达基因,其中740个基因的mRNA水平升高,392个基因的mRNA水平降低。值得注意的是,几个细胞周期抑制因子基因被上调,包括Cdkn1a/p21、Cdkn2d和Cdkn2c,这些基因的肿瘤抑制功能已得到充分证实。此外,一个关键的癌基因Myc被下调。同样,在Pum2敲除细胞中,研究者也鉴定了差异表达基因,并发现上调基因包含一组略有不同的细胞周期基因,如Ccnd3和Tgfb1。这些结果表明,PUM1和PUM2在CRC中可能通过调控不同的细胞周期基因来发挥作用。
- PUM1直接抑制p21以调控CRC的生长
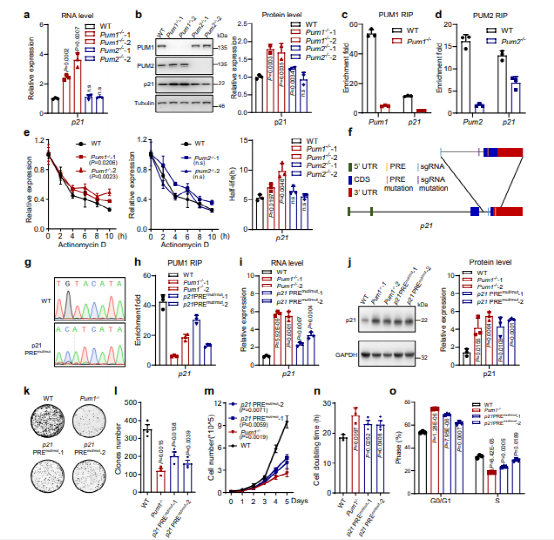
在PAR-CLIP-seq实验揭示的PUM1直接靶点中,p21是一个重要的G1/S相变调控因子。此外,p21表达与CRC的总生存率呈负相关。因此,研究者重点研究了PUM蛋白对p21的调控作用。RNA深度测序和蛋白质质谱分析显示,p21在RNA和蛋白质水平上都受到PUM1的抑制。进一步利用RT-qPCR和蛋白质印迹法验证发现,Pum1-/-细胞中p21的RNA和蛋白水平均显著升高,而Pum2-/-细胞中p21 RNA和蛋白水平的增加则不如Pum1-/-细胞中的增加显著。与此一致,RIP实验表明,p21 mRNA被Pum1强结合(7.4倍富集),而被Pum2弱结合(1.9倍富集)。这些结果表明,PUM1通过直接抑制p21来调控CRC的生长。
- 抗PUM治疗可有效降低CRC肿瘤生长
最后,研究者利用CRC模型小鼠,通过静脉注射纳米颗粒包装的抗PUM SiRNA,评估了抗PUM治疗对肿瘤生长的影响。结果发现,抗PUM治疗显著降低了CRC模型小鼠的肿瘤生长。这一结果进一步支持了PUM蛋白在CRC中的重要作用,并为抗PUM治疗CRC提供了潜在的新途径。
结论与展望
本研究系统地探讨了PUM1和PUM2在CRC中的功能和作用机制,并得出了以下结论:
-
PUM1和PUM2在人类CRC中表达增加,且PUM1的表达与CRC阶段和患者生存率呈负相关。
-
PUM1主要通过直接调控癌相关基因和细胞周期相关基因(如p21)来发挥作用,而PUM2则可能通过调控不同的细胞周期基因来影响CRC的进展。
-
PUM1通过直接抑制p21来调控CRC的生长,这一发现为深入了解CRC肿瘤发生的重要分子机制提供了新见解。
-
抗PUM治疗可有效降低CRC肿瘤生长,为CRC的潜在新治疗途径提供了实验依据。
展望未来,研究者将进一步深入探讨PUM蛋白在CRC中的具体作用机制,以及与其他信号通路的相互作用关系。同时,也将继续优化抗PUM治疗策略,以期实现CRC的早期检测、诊断和靶向治疗。此外,鉴于PUM蛋白在多种人类疾病中的重要作用,研究者还将探索其在其他疾病中的潜在作用机制和治疗靶点,为更多疾病的治疗提供新的思路和方法。
| 名称 | 货号 | 规格 |
| Rabbit anti-p21 Monoclonal Antibody(3K5) | abs159643-100ul | 100ul |
| Purified Mouse Anti-p21(SX118) | 556430 | 100ug |
| Purified Mouse Anti-p21(SXM30) | 556431 | 100ug |
| ANTI-P21 | PA534805 | EA |