上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|利用患者特异性iPSC衍生的心肌细胞揭示Brugada综合征表型严重程度差异
243 人阅读发布时间:2025-07-23 15:39
Patient-specific iPSC-derived cardiomyocytes reveal variable phenotypic severity of Brugada syndrome
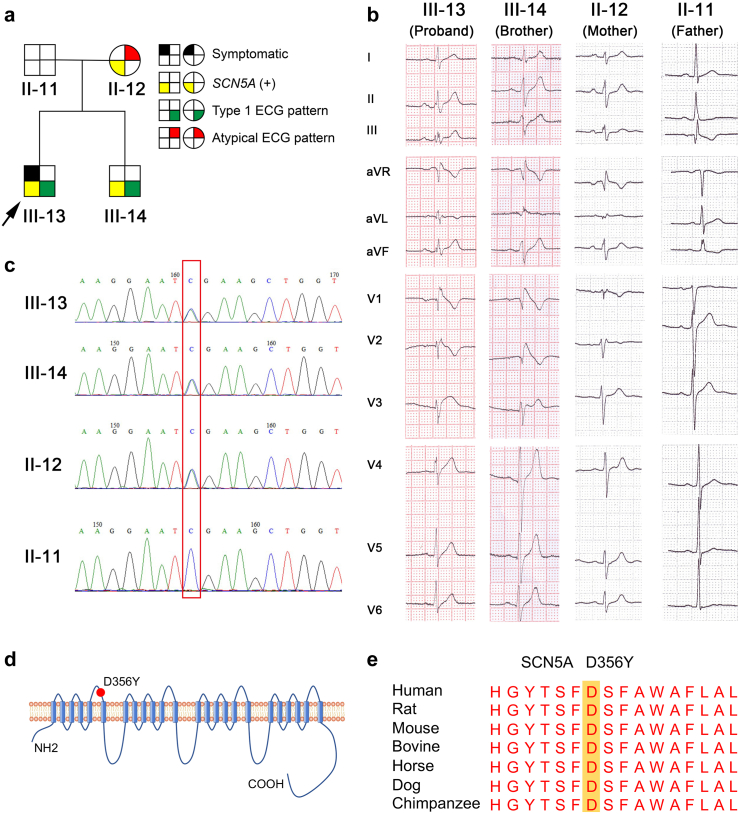
Brugada综合征(BrS)是一种心脏离子通道病,可能导致患者发生猝死(SCD)。尽管SCN5A基因是与BrS最为频繁相关的基因,但基因型与表型之间的关联并不总是完全吻合。特定SCN5A变异的临床表型可能从无症状到猝死不等。为了深入探究这种表型差异,科研人员采用了一种创新的方法:比较来自SCN5A突变阳性(D356Y)BrS家族中的重症患者、无症状突变携带者(AMC)及健康对照者的诱导多能干细胞(iPSC)衍生的心肌细胞(iPSC-CMs)。

一、研究背景与意义
BrS作为一种遗传性心脏疾病,其临床表现的多样性一直是临床医生和研究人员关注的焦点。SCN5A基因编码的Nav1.5钠离子通道在心脏电活动中起着至关重要的作用,而SCN5A的突变可能导致Nav1.5功能异常,进而引发BrS。然而,相同SCN5A突变的个体间可能存在截然不同的临床表现,这提示我们除了基因因素外,还可能存在其他影响疾病表型的因素。
本研究通过利用iPSC技术,成功地从皮肤成纤维细胞中生成了iPSC,并进一步将其分化为心肌细胞。这种方法为研究人员提供了一个独特的平台,使他们能够在体外模拟BrS患者的心脏细胞,从而深入探究SCN5A突变对心脏细胞电活动的影响,以及不同个体间表型差异的潜在机制。
二、研究方法与技术路线
1. iPSC的生成与分化
本研究首先收集了SCN5A突变阳性BrS家族中的重症患者、无症状突变携带者及健康对照者的皮肤成纤维细胞。随后,利用非整合型仙台病毒将这些成纤维细胞重编程为iPSC。这一步骤的关键在于确保iPSC具有与原始细胞相同的遗传信息,同时能够分化为多种细胞类型,包括心肌细胞。
在成功生成iPSC后,研究人员采用单层分化协议将其分化为心肌细胞。这一过程中,iPSC经历了特定的信号传导途径激活和抑制,最终分化为具有心脏电生理特性的心肌细胞。
2. 电生理特性与离子通道功能的评估
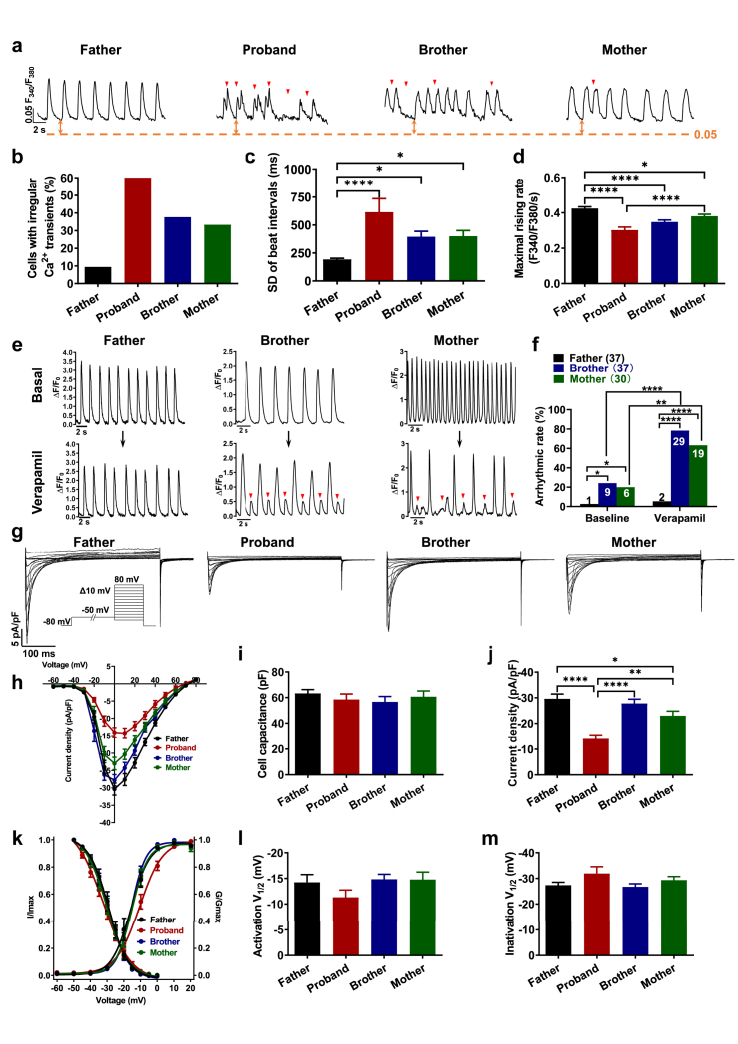
为了探究SCN5A突变对心肌细胞电活动的影响,研究人员对生成的iPSC-CMs进行了全面的电生理特性评估。这包括测量跳动间隔变异性、去极化速度、心律失常发生率以及Na+和Ca2+离子通道的功能。这些评估不仅有助于揭示SCN5A突变对心肌细胞电活动的影响,还能够为理解BrS的发病机制提供重要线索。
3. CRISPR/Cas9介导的基因编辑与药物筛选
为了进一步验证SCN5A突变在BrS发病机制中的作用,研究人员采用了CRISPR/Cas9基因编辑技术,对重症患者的iPSC-CMs中的SCN5A突变进行了纠正。通过比较纠正前后iPSC-CMs的电生理特性变化,研究人员能够评估SCN5A突变对心肌细胞电活动的影响程度。
此外,为了寻找可能用于治疗BrS的药物,研究人员还利用建立的BrS iPSC-CM模型进行了药物筛选。通过评估不同药物对iPSC-CMs电生理特性的影响,研究人员希望能够发现具有抗心律失常作用的药物,为BrS患者提供新的治疗选择。
三、研究结果与发现
1. SCN5A突变对iPSC-CMs电生理特性的影响
研究发现,与对照组相比,携带D356Y突变的iPSC-CMs表现出增加的跳动间隔变异性、减慢的去极化速度、心律失常发生率增加以及Na+通道功能和Ca2+信号传导缺陷。这些发现进一步证实了SCN5A突变对心肌细胞电活动的影响,并为理解BrS的发病机制提供了重要证据。
2. 无症状突变携带者与重症患者之间的表型差异
值得注意的是,研究发现无症状突变携带者(AMC)的iPSC-CMs表型严重程度较重症患者为轻。这一发现提示我们,除了SCN5A突变外,还可能存在其他因素(如遗传因素、环境因素或细胞适应性改变等)影响BrS的表型严重程度。
此外,研究还发现,当使用氟卡尼(一种已知的Na+通道阻滞剂)处理AMC和重症患者的iPSC-CMs时,AMC的iPSC-CMs表现出更轻微的心律失常反应。这一发现进一步支持了表型严重程度与Na+通道功能之间的关联,并提示我们药物反应可能因个体而异。
3. CRISPR/Cas9介导的基因编辑对表型的影响
通过CRISPR/Cas9介导的基因编辑技术纠正重症患者iPSC-CMs中的SCN5A突变后,研究人员发现心律失常表型得到有效改善,Na+和Ca2+电流得到恢复。这一发现不仅证实了SCN5A突变在BrS发病机制中的关键作用,还表明基因编辑技术可能为BrS患者提供新的治疗策略。
4. 药物筛选的结果与临床应用前景
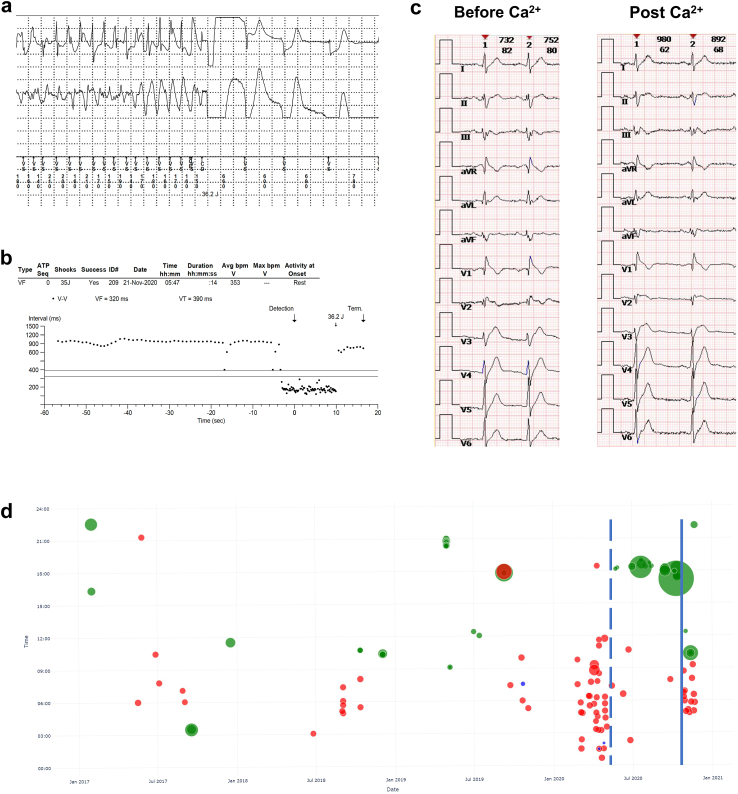
药物筛选实验表明,奎尼丁和索他洛尔在个体依赖的方式下表现出抗心律失常作用。这一发现为BrS患者提供了新的治疗选择,并可能有助于改善患者的预后。此外,临床上对重症患者进行中期随访时发现,静脉和口服钙剂部分减少了恶性心律失常事件。这一发现进一步支持了Ca2+电流在抵抗BrS心律失常发生中的潜在作用,并为未来的药物治疗提供了新的思路。
四、研究意义与未来展望
本研究通过利用患者特异性iPSC衍生的心肌细胞揭示了BrS表型严重程度差异的潜在机制。研究不仅证实了SCN5A突变在BrS发病机制中的关键作用,还发现了其他可能影响疾病表型的因素。此外,通过药物筛选和基因编辑技术,研究为BrS患者提供了新的治疗选择和潜在的治疗策略。
未来,研究人员可以进一步探索其他可能影响BrS表型的遗传因素和环境因素,以及这些因素与SCN5A突变之间的相互作用机制。同时,利用更先进的基因编辑技术和高通量药物筛选平台,研究人员可以加速新药物的研发进程,为BrS患者提供更多有效的治疗选择。此外,将研究成果转化为临床应用也是未来研究的重要方向之一。通过临床试验和长期随访研究,研究人员可以评估新药物和基因编辑技术的安全性和有效性,为患者提供更好的治疗服务。
综上所述,本研究为理解BrS的发病机制和治疗策略提供了新的视角和思路。通过深入探究SCN5A突变对心肌细胞电活动的影响以及不同个体间表型差异的潜在机制,研究人员为BrS患者提供了新的治疗选择和希望。未来,随着研究的深入和技术的不断进步,我们有理由相信BrS的治疗将更加个性化和有效。
| 名称 | 货号 | 规格 |
| Phospholamban (D9W8M) Rabbit mAb | 14562T | 20μl |
| alpha-Actinin (D6F6) XP ® Rabbit mAb | 6487S | 100ul |
| XEN907 | X-105-25mg | 25mg |
| XE991 | X-100-50mg | 50mg |