上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
两篇文章带你深入了解铁死亡!(上)
594 人阅读发布时间:2021-06-07 15:18
铁死亡(Ferroptosis)是一种铁离子依赖性的,区别于细胞凋亡、细胞坏死、细胞自噬的新型程序性细胞死亡形式。既然是一种程序性细胞死亡,这意味着它可以被调控。
从发生机制上讲铁死亡主要是在二价铁离子或酯氧合酶的作用下,催化细胞膜上高表达的不饱和脂肪酸,发生脂质体过氧化,从而诱导细胞死亡,还表现在抗氧化体系谷胱甘肽GSH和谷胱甘肽过氧化物酶4-GPX4的表达量降低。
铁死亡主要有以下几个特点:
(1)细胞形态方面:铁死亡会导致细胞线粒体变小,膜密度增高,嵴减少、消失,外膜破碎。细胞核中形态变化不明显。
(2)细胞成分方面:铁死亡表现为脂质过氧化增高,ROS升高。也有一些特征基因发生变化。

铁死亡通路图
从过去几年国家自然科学基金中标的项目我们发现,从2013年申请第一项关于“铁死亡”的项目,2017年增加到16项,到2019年增至76项,累计资助经费6008.2万,都说明了铁死亡研究不断受到科学家的重视,成为细胞死亡研究新的“宠儿”。

图1:关键词“铁死亡”检索国自然科学基金
(未包括关键词“Ferroptosis”)
“铁死亡”入选中国科学院2019生物科学领域TOP 10(图2)

图2:《2019研究前沿》生物科学领域TOP 10
第一篇是关于p53能够通过SLC7A11调节胱氨酸代谢,调控ROS应答并通过铁死亡抑制肿瘤生长,第二篇则是今年发表在nature research上的关于能量胁迫可以激活AMPK激活,从而抑制ACC并降低花生四烯酸这个多聚不饱和脂肪酸的合成,最终抑制铁死亡。
01
Ferroptosis as a p53-mediated
activity during tumour suppression
早在2015年细胞生物学领域著名华人科学家顾伟教授在nature在线发表了一篇关于经典肿瘤抑制因子p53介导铁死亡过程,抑制肿瘤生长的文章。接下来跟大家一起看看这篇文章研究思路吧。
p53是一个经典的肿瘤抑制基因,在所有恶性肿瘤中,50%以上会出现该基因的突变。p53介导的细胞周期停滞、衰老和凋亡对抑制肿瘤的发展具有重要作用,同时研究也表明p53对细胞代谢活性的调节在其发挥抗肿瘤作用中也十分重要。


图一、SLC7A11基因是p53的靶点
a、在经过doxycycline 诱导的细胞中,WB和RT-PCR结果显示p53的激活会伴随着SLC7A11水平的降低;
b、SLC7A11的基因序列也显示其上存在p53的结合位点;
c、EMSA实验也显示,重组全长人类野生型p53与含有该位点的放射性标记寡核苷酸探针孵育后,可以鉴定出p53–DNA复合物;
d、ChIP 实验也验证了p53和SLC7A11的DNA序列存在相互作用;
e、用nutlin-3处理细胞,使p53激活/干扰掉p53时,SLC7A11的蛋白质水平伴随着显着降低/升高。这组实验充分说明了SLC7A11基因是p53介导的转录抑制的靶点。
既然SLC7A11是P53的靶点,那p533KR作为p53蛋白的一种乙酰化缺陷突变形式,但是它对SLC7A11的表达有作用吗?
接下来的一组实验则说明了p533KR虽然不能够诱导细胞周期暂停,衰老和凋亡过程,但完全保留了对SLC7A11表达的调控能力,并能够促使细胞在ROS诱导的应激状态下发生"铁死亡"过程。
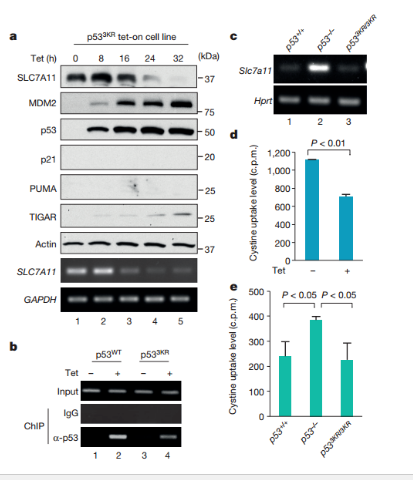
图二、p533KR可以调节SLC7A11基因的表达和细胞对半胱氨酸的摄取
a、在细胞中用四环素诱导p533KR的表达,发现p533KR能够激活TIGAR和MDM2的表达,但不能激活p21或PUMA的表达,但是在p533KR诱导后的不同时间点,SLC7A11的水平都大大降低了;
b、ChIP 实验也验证了p533KR可以和SLC7A11的DNA序列可以相互作用;
c、在源自p53+/+、p533KR/3KR和p53-/-小鼠的MEF中,相对于野生型MEF,SLC7A11在p53–/–的细胞中表达明显增加,然而在p533KR/3KR细胞中的SLC7A11转录水平仍然很低,这表明p533KR可以抑制SLC7A11的表达;
d、在四环素诱导的p533KR细胞中发现细胞对胱氨酸摄取能力下降;
e、在源自p53+/+、p533KR/3KR和p53-/-小鼠的MEF中,p53-/-实验组对胱氨酸的摄取增加到比p53+/+组高出约60%的水平,这证明p53的缺失促进了细胞对胱氨酸的摄取,但是在p533KR/3KR实验组中细胞对胱氨酸的摄取没有变化,这表明p533KR/3KR保留了抑制细胞摄取胱氨酸的能力。
这组实验说明了p533KR可以调节SLC7A11基因的表达。
SLC7A11是质膜转运蛋白的关键成分,它可以介导细胞Na+依赖性的对胞外胱氨酸的摄取,以换取胞内谷氨酸。为了探索p53对SLC7A11抑制的功能,研究进一步分析了p53的激活对细胞摄取L--胱氨酸的影响。
研究表明,SLC7A11的表达对于铁死亡也很关键,在特死亡发生的过程中涉及到代谢功能的异常。p53既然能够调控SLC7A11的表达,也能影响细胞对胱氨酸的摄取,那p53是否能够铁死亡呢?接下来进行了如下实验。

图三、p53对铁死亡的调控作用
a、用铁死亡诱导剂erastin 处理小鼠的MEF细胞8h,发现p53+/+、p533KR/3KR组的中细胞死亡率超过48%,但在p53-/-实验组中细胞死亡率保持在20%的低水平。这说明p53的缺失可以避免erastin诱导的铁死亡;
b、通过代谢动力学分析,在6小时后在p53+/+、p533KR/3KR组的MEF细胞中可以很容易就检测到细胞死亡;
c、在经过erastin处理的细胞中,我们观察到线粒体收缩,膜密度增加,但没有明显的DNA断裂;
d、用铁死亡特异性抑制剂ferrostatin-1处理细胞,结果发现ferr-1可以抑制p53+/+和p533KR/3KR组的ME细胞死亡,但是其他细胞死亡抑制剂,如自噬(3-甲基精胺),细胞凋亡(Z-VAD-FMK)和坏死病(necrostatin-1)的抑制剂,均不能抑制erastin诱导的细胞死亡。这组实验说明了p533KR可以调节细胞对胱氨酸的摄取和促进铁死亡。
有研究表明,SLC7A11在多种形式的人类癌症中均过表达,p53可以调节SLC7A11基因的表达,那p53可以通过SLC7A11来抑制肿瘤生长吗?
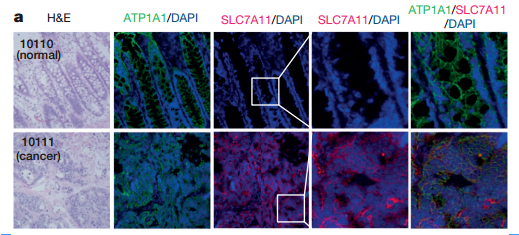

图四、SLC7A11的表达对抑制p533KR诱导的肿瘤生长的作用
a、HE染色表明,SLC7A11在成对的结肠癌的邻近正常组织上没有检测到,但成对的结肠癌的质膜上检测到明显的SLC7A11;
b-c、在用erastin诱导SLC7A11的质粒转染的p533KR H1299 细胞中发现,SLC7A11过表达可以减轻p533KR依赖的铁死亡;
d-e、异种移植肿瘤生长试验也表明,p53缺失的肿瘤组织生长显着降低,但是在SLC7A11过表达的情况下,的抑制作用被很大程度上被减弱。这些数据表明SLC7A11的表达对抑制p533KR诱导的肿瘤生长至关重要。
多项研究表明,p53在细胞凋亡,细胞生长停滞和衰老中的典型活性是导致p53+/+Mdm2-/-小鼠胚胎致死性的主要原因。为了进一步探究进行了如下实验。
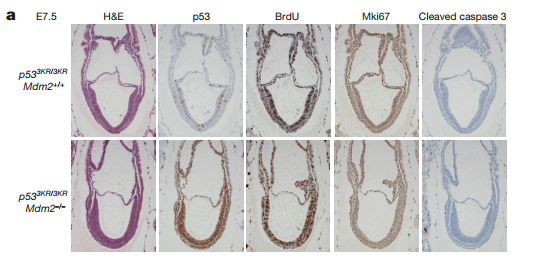
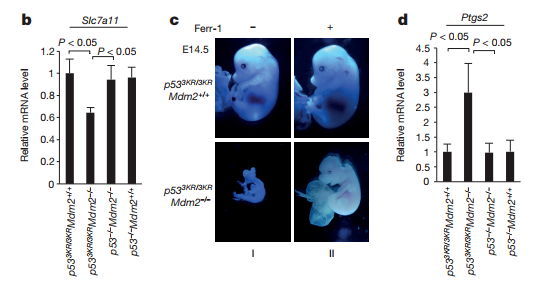
图五、p53介导的代谢调节胚胎发育的影响
a、检查了从p533KR/3KRMdm2+/-小鼠获得的胚胎,发现p53染色显着升高,但发育结构基本正常,这表明p533KR突变能够促进胚胎发育;
b、同时检测了p533KR/3KRMdm2+/-及其他实验组小鼠胚胎中Slc7a11 mRNA的量,发现p533KR/3KRMdm2-/-组的Slc7a11 mRNA明显下调;
c、经过ferr-1处理的p533KR/3KRMdm2-/-组胚胎在E14.5天(II)表现出明显的器官发生,例如眼部形成和四肢分化。而此时未经处理的p533KR/3KRMdm2-/-组胚胎却未成形,再重新经过ferr-1处理后胚胎也在长大,眼睛的结构得到了明显改善;
d、Ptgs2在p533KR/3KRMdm2-/-组胚胎中显着上调,但在p53-/-Mdm2-/-组胚胎不受影响,这表明p533KR/3KRMdm2-/-胚胎中Ptgs2的上调是p53依赖性的。
这组数据表明,p53介导的对代谢调节和铁死亡的影响对p533KR/3KRMdm2-/-胚胎发育至关重要。
通过对突变小鼠进行分析,研究人员发现这些p53的非经典活性能够促进胚胎发育以及与MDM2缺失相关的致死。同时,研究人员还发现SLC7A11在人类肿瘤中高表达。
为了在更佳的代谢条件下研究铁死亡,文章进一步分析了p533KR介导的铁死亡是否与ROS应激反应有关。最终发现,其过表达能够抑制ROS诱导的"铁死亡"并减弱p53 3KR介导的对肿瘤生长的抑制作用。

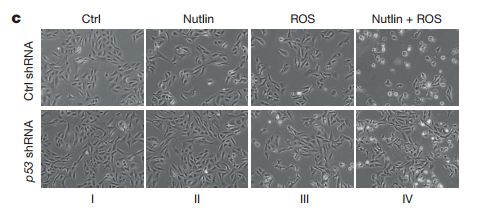
图六、p53介导的铁死亡对ROS应答的作用
a、仅分别通过p533KR诱导或ROS处理均未观察到明显的细胞死亡,但是同时经过p533KR诱导和ROS处理可诱导大量细胞死亡,而这种死亡可被ferr-1特异性抑制;
b、过表达SLC7A11也可以抑制经过p533KR诱导和ROS处理诱导的细胞死亡;
c、Nutlin-3对U2OS细胞进行处理,诱导了高水平的p53表达,而没有引起细胞死亡,而仅用ROS的处理组则没有诱导p53激活,也未能引起细胞死亡,但是在Nutlin-3和ROS共处理组出现了大量得到细胞死亡;
d、WB结果显示,相对于对照MEF组,Slc7a11-BAC组中的SLC7A11蛋白水平明显升高;
e、在野生型MEF中,用ROS或erastin处理均增强了铁死亡,但在Slc7a11-BAC组中铁死亡大大减弱。
这些数据表明,ROS特异性诱导了p53介导的铁死亡,而SLC7A11的水平对这一过程至关重要。
这项研究表明p53能够通过调节胱氨酸代谢,ROS应答和"铁死亡"抑制肿瘤生长的新模式,进一步拓展了人们对经典抗肿瘤因子p53的新认识,具有重要意义。
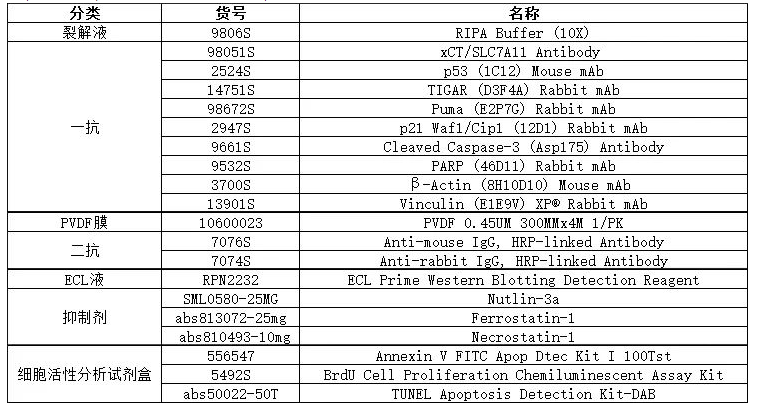
文章学习之后,小优给大家总结了本篇文章中涉及到的部分相关产品: