上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|m7G 修饰研究成果荟萃:多领域视角下的深度洞察与解析
567 人阅读发布时间:2025-02-14 14:47
1.QKI 转运内部 m7G 修饰转录本进入应激颗粒并调控 mRNA 代谢
于《Cell》杂志发表(IF = 64.5,2023.06)。N7 - 甲基鸟苷 (m7G) 修饰常见于 mRNA 5‘cap 或 tRNA /rRNAs,也现身于信使 RNA (mRNA) 内部。尽管 m7G - cap 对 mRNA 前体加工及蛋白质合成极为关键,但 mRNA 内部 m7G 修饰的确切功效仍待明确。本研究揭示 m7G 内部的 mRNA 可被 Quaking protein (QKIs) 特异性识别。借助转录组分析绘制内部 m7G 甲基组与 QKI 结合位点,确定了超 1000 个带有保守 “GANGAN (N = A/C/U/G)” 基序且高可信度的 m7G 修饰及 QKI 结合的 mRNA 靶标。令人瞩目的是,QKI7(通过 C 端)与应激颗粒 (SG) 核心蛋白 G3BP1 相互作用,并将内部 m7G 修饰的转录本转运至 SGs,以此调控 mRNA 在应激条件下的稳定性与翻译过程。具体而言,QKI7 降低了 Hippo 信号通路中关键基因的翻译效率,致使癌细胞对化疗更为敏感。总体而言,本研究将 QKIs 界定为 mRNA 内部 m7G 结合蛋白,其可调控靶 mRNA 代谢及细胞耐药性。
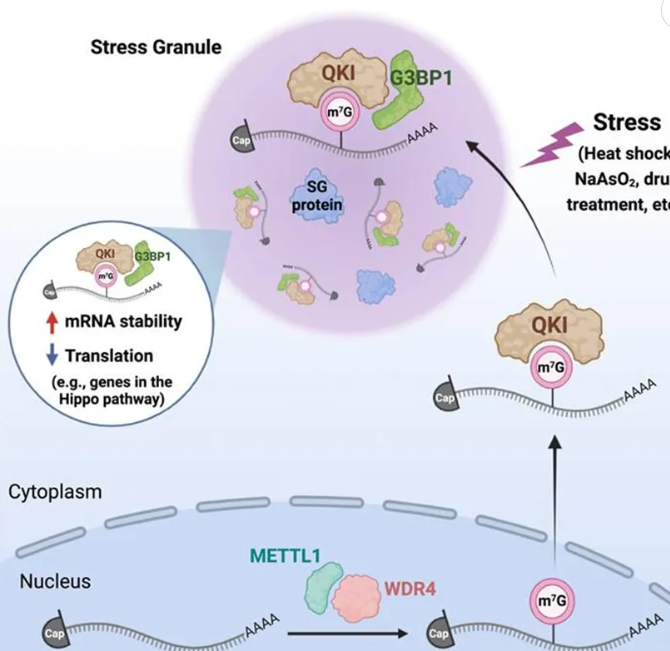
2.METTL1 通过前列腺癌中 tRNA 衍生片段的生物发生促进肿瘤发生
刊载于《Mol Cancer》(IF = 37.3,2023.06)。越来越多的全新证据凸显表转录组标记在众多癌症发展进程中的重要意义;然而,对于前列腺癌中表转录组沉积改变的作用与价值,人们知之甚少。在此研究中,发现转移 RNA N7 - 甲基鸟苷 (m7G) 转移酶 METTL1 在原发性及晚期前列腺肿瘤中呈现高表达态势。从机制层面来看,METTL1 的缺失会导致 m7G tRNA 甲基化缺失,并促进一类源自 5‘tRNA 片段的新型小非编码 RNA 的生物发生。这些 5’ tRNA 衍生的小 RNA 引导翻译控制,有利于肿瘤生长抑制、干扰素通路以及免疫效应器关键调节因子的合成。在前列腺癌临床前模型中,METTL1 的敲低促使促炎免疫细胞在肿瘤内的浸润增加,免疫治疗反应得以增强。综上所述,本研究成果揭示了 METTL1 导向的 m7G tRNA 甲基化在癌细胞翻译控制及肿瘤生物学中的治疗价值。
3.METTL1 - WDR4 调控 m7G tRNA 修饰的结构基础
发表于《Nature》(IF = 64.8,2023.01)。RNA 的化学修饰在诸多生物过程中发挥着核心作用。N7 - 甲基鸟苷 (m7G) 是 tRNAs4 - 7 大亚群完整性与稳定性所必需的。甲基转移酶 1 - WD 重复包含蛋白 4 (METTL1 - WDR4) 复合物是修饰某些 tRNA 可变环中 G46 的甲基转移酶,其失调会驱动多种癌症类型的肿瘤发生。WDR4 突变可引发包括小头畸形在内的人类发育表型。METTL1 - WDR4 如何修饰 tRNA 底物并进行调控依旧扑朔迷离。本研究通过对人 METTL1 - WDR4 的结构、生化及细胞研究表明,WDR4 作为 METTL1 与 tRNA T - arm 的支架,在 tRNA 结合后,METTL1 的 αC 区转变为螺旋,与 α6 螺旋一同固定 tRNA 可变环的两端。出乎意料的是,发现 METTL1 的无序 N 端区域是催化口袋的一部分,对甲基转移酶活性至关重要。此外,METTL1 N 端区域的 S27 磷酸化会通过局部破坏催化中心来抑制甲基转移酶的活性。本研究成果为 tRNA 底物识别以及磷酸化介导的 METTL1 - WDR4 调控提供了分子层面的理解,并揭示了 METTL1 紊乱的 N 端区域与甲基转移酶活性的关联。
4.METTL1 介导的 m7G tRNA 修饰促进肝细胞癌对仑伐替尼的耐药性
刊登在《Cancer Research》(IF = 11.2,2023.01)。酪氨酸激酶抑制剂仑伐替尼是治疗晚期肝细胞癌 (HCC) 的一线药物。然而,其疗效因耐药性而大打折扣。深入洞悉仑伐替尼耐药的分子机制可为改善并延长治疗反应提供崭新策略。本研究对亲本及仑伐替尼耐药的 HCC 细胞开展蛋白质组学筛选,发现 tRNA N7 - 甲基鸟苷 (m7G) 甲基转移酶复合物的两个关键组分 —— 甲基转移酶样蛋白 - 1 (METTL1) 和 WD 重复结构域 4 蛋白 (WDR4) 在耐药细胞中显著上调。敲低 METTL1 可通过降低肝癌细胞在仑伐替尼作用下的增殖能力并促进细胞凋亡来克服耐药性。此外,过表达野生型 METTTL1 而非其催化失活突变体可诱导仑伐替尼抗性。动物实验涵盖水动力注射、皮下植入及原位异种移植小鼠模型,进一步证实了 METTL1/WDR4 介导的 m7G tRNA 修饰在体内促进仑伐替尼耐药的关键作用。从机制上讲,METTL1 促进 EGFR 通路基因的翻译,从而引发耐药性。本研究揭示了 METTL1 介导的 m7G tRNA 修饰在促进仑伐替尼耐药中的重要作用,为耐药提供了颇具潜力的预测标记与干预靶点。
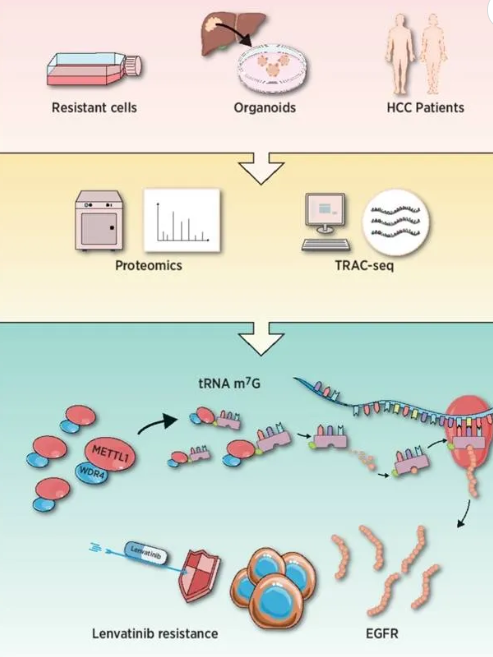
5.消除 METTL1 介导的多形核髓源性抑制细胞积累可预防射频消融术后肝细胞癌复发
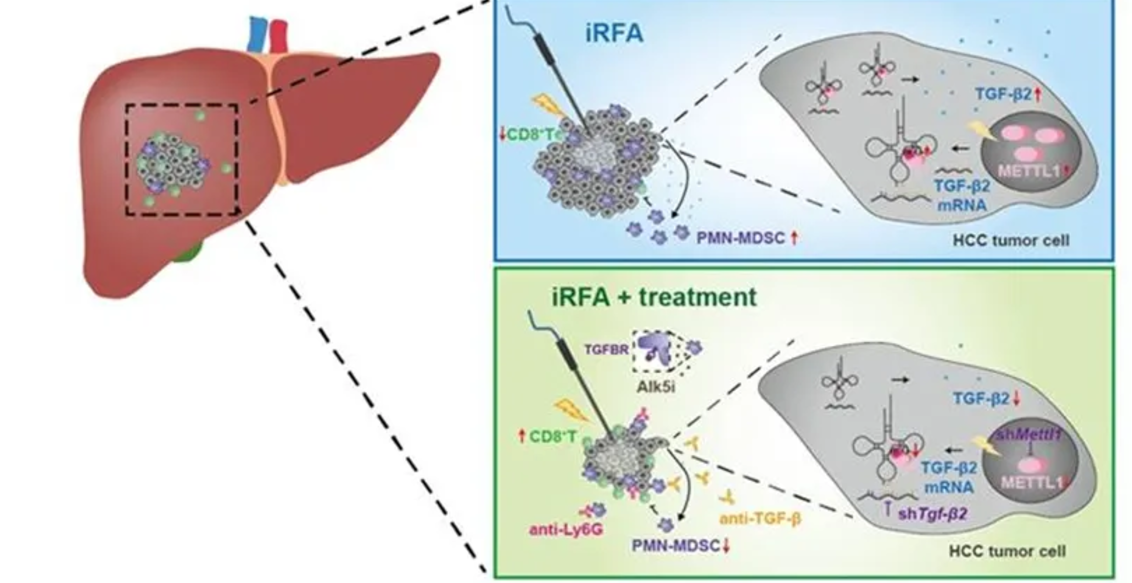
发表于《Hepatology》(IF = 13.5,2023.04)。背景与目的:射频消融术 (RFA) 是肝细胞癌 (HCC) 的一种重要治疗手段,但其复发率与其他 HCC 治疗方式相比依然居高不下。甲基转移酶 1 (METTL1) 是一种用于 m7G tRNA 修饰的酶,据报道可促进 HCC 的发展。本研究旨在评估 METTL1 在射频消融术不足 (iRFA) 后形成免疫抑制肿瘤微环境中的作用。方法与结果:通过免疫组织化学与多重免疫荧光 (mIF) 染色,发现 METTL1 表达在 RFA 后复发的 HCC 中增强,同时伴有 CD11b + CD15 + 多形核 - 髓源性抑制细胞 (PMN - MDSCs) 的增加以及 CD8 + T 细胞的减少。从机制上看,热介导的 METTL1 上调通过诱导髓源性抑制细胞增强 TGF - β2 的翻译,从而形成免疫抑制环境。肝脏特异性过表达或敲低 METTL1 显著影响 PMN - MDSCs 的积累,并随后影响 CD8 + T 细胞的浸润。完整 RFA 成功消除肿瘤,而与假手术相比,iRFA 处理的小鼠表现出肿瘤生长与转移增强,PMN - MDSC 积累增加,CD8 + T 细胞减少。通过抗 Ly6G 抗体阻断 METTL1 - TGF - β2 - PMN - MDSC 轴,或敲低肝癌固有的 METTL1 或 Tgfb2,或阻断 TGF - β 信号可显著缓解 iRFA 诱导的肿瘤进展,恢复 CD8 + T 细胞群。结论:本研究揭示了 METTL1 在调节免疫抑制微环境中的关键作用,并证明阻断 METTL1 - TGF - β2 - PMN - MDSC 轴可能是一种恢复抗肿瘤免疫并预防 RFA 治疗后 HCC 复发的治疗策略,值得开展进一步的临床研究。
| 名称 | 货号 | 规格 |
| m3G-cap, m7G-cap | 201011 | 100ug |
| m3G-cap, m7G-cap | 201001 | 100ul |
| CAP ANALOG(M7G(5‘)PPP(5‘)G)10 | AM8048 | A260U(40MM) |



































