上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|DNMT1在口腔鳞状细胞癌中的新角色:增强肿瘤抑制与规避毒性
173 人阅读发布时间:2025-02-26 13:18
近日,四川大学的周红梅与罗晶晶教授在Molecular Cancer期刊上发表了一项题为“DNMT1-targeting remodeling global DNA hypomethylation for enhanced tumor suppression and circumvented toxicity in oral squamous cell carcinoma”的重要研究。该研究揭示了DNA甲基转移酶1(DNMT1)在口腔鳞状细胞癌(OSCC)中全新的作用机制,为OSCC的治疗提供了新的潜在靶点。

OSCC作为一种起源于口腔上皮细胞的恶性肿瘤,具有高度的异质性。尽管近年来新治疗方法不断涌现,但OSCC患者在治疗后仍面临复发和转移的风险,尤其是晚期患者的生存率依然较低。为了改善OSCC患者的生存结果,科研人员一直在探索选择性靶向癌细胞中异常信号分子或蛋白质的新疗法。然而,这些靶向治疗的疗效常受到癌细胞中药物耐药性的限制,这可能与基因组不稳定、信号级联失调或药理学毒性等多种因素有关。
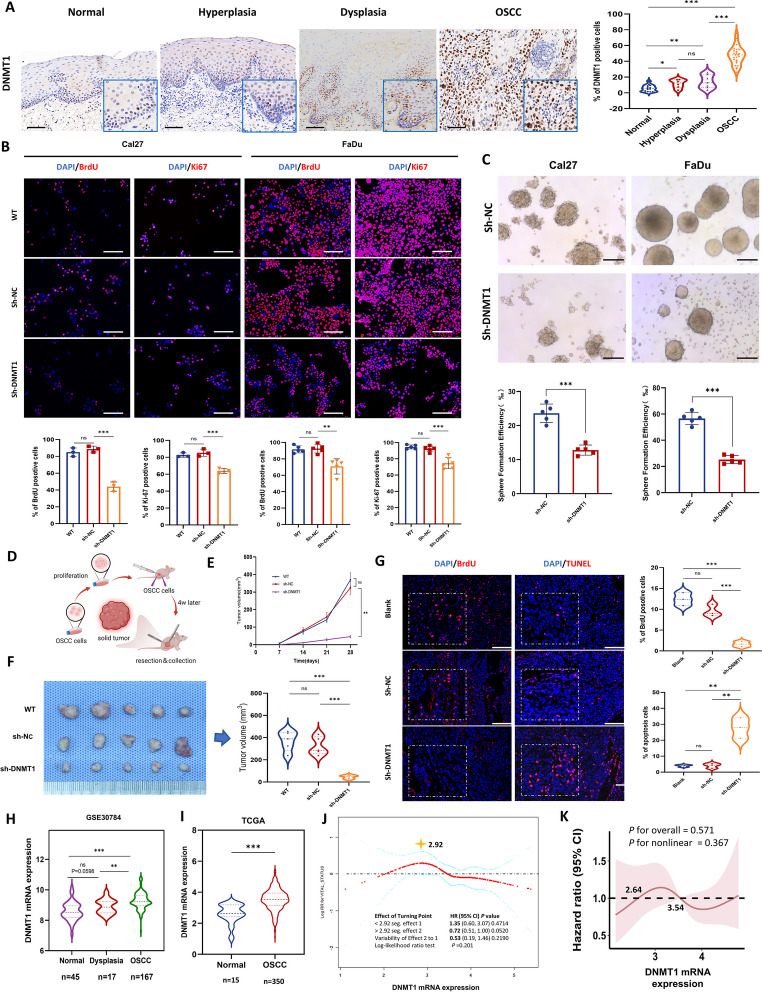
DNA甲基化作为一种关键的表观遗传修饰,在真核生物中扮演着控制基因表达模式、维持细胞类型特异性基因组稳定性和胚胎发育的重要角色。与OSCC的进展密切相关的是,癌细胞具有全基因组DNA低甲基化的特征,这种特征导致了癌细胞的不稳定和肿瘤的异质性。
DNMT1作为最常见的DNA甲基转移酶,在DNA复制过程中维持DNA甲基化稳态至关重要。早期研究已预测DNMT1可能是与OSCC进展相关的潜在靶点,且抑制DNMT1对多种类型的鳞癌具有正向的抗癌作用。然而,DNMT1通过DNA甲基化和信号转导调节OSCC发生和进展的具体机制仍不明确。
在这项研究中,周红梅与罗晶晶教授的研究团队整合了来自临床人类样本、异种移植小鼠模型的多层实验数据,以及独立的高通量DNA甲基化微阵列分析以及大量和单细胞转录组分析。他们发现,在人类口腔恶性转化过程中,DNMT1的表达呈现稳步提高的趋势。进一步的研究表明,在体外和异种移植的OSCC模型中,抑制DNMT1能显著降低致瘤性。
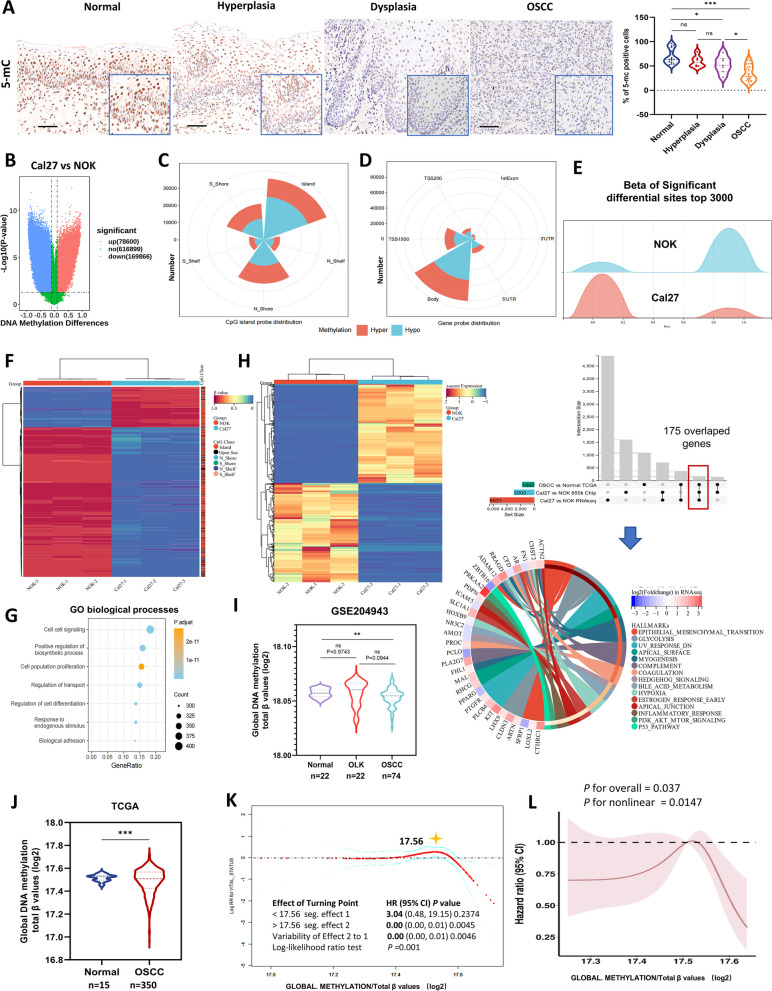
值得注意的是,在口腔癌发生过程中,DNMT1的过表达伴随着癌症特异性DNA低甲基化的积累。相反,当在癌细胞和异种移植肿瘤中敲低DNMT1时,会导致非典型的广泛的全基因组DNA低甲基化。这种新的DNMT1重塑的DNA低甲基化模式具有显著的生物学效应,它阻碍了PI3K-AKT和CDK2-Rb的双重激活,并协同失活了GSK3β。
在治疗OSCC小鼠的实验中,靶向DNMT1不仅获得了比PI3K抑制剂更大的抗癌效果,而且降低了PI3K抑制剂或PI3K与CDK抑制剂联合使用引起的血糖变化以及胰岛素不良反馈的毒性。这一发现表明,靶向DNMT1能够重塑一种新的全球DNA低甲基化模式,以促进抗癌功效,并通过平衡的信号协同作用将潜在的毒性作用降至最低。
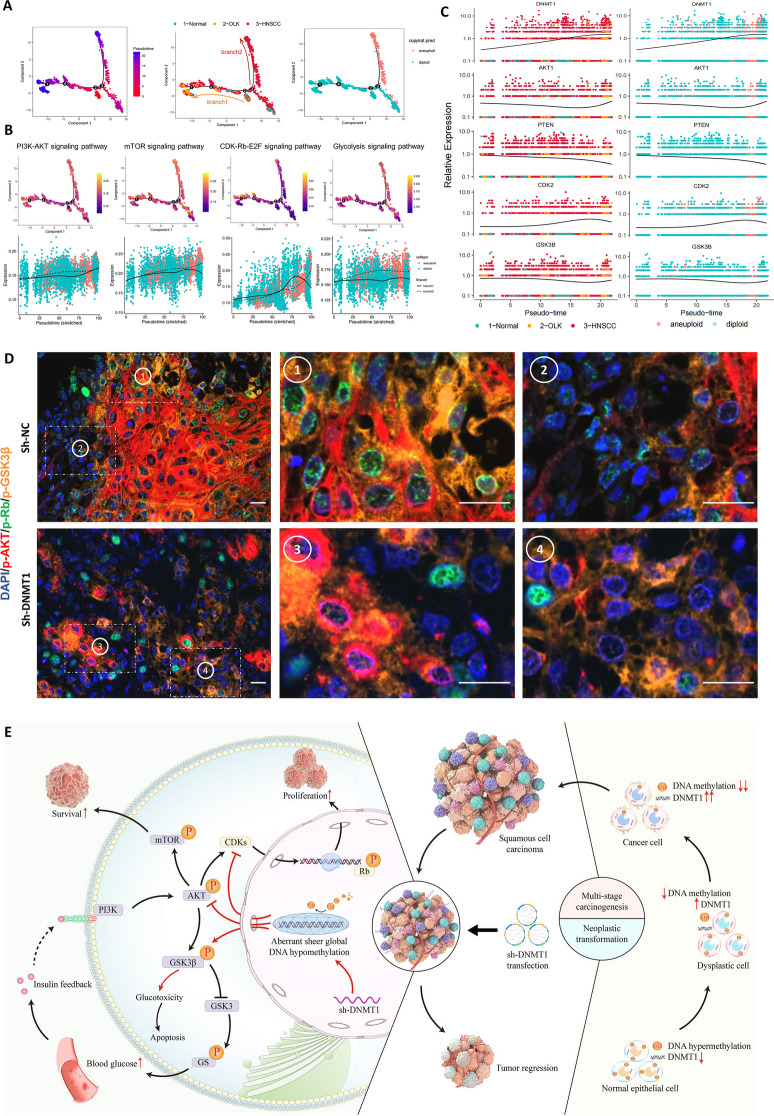
综上所述,这项研究揭示了DNMT1在OSCC中的新角色,它不仅是DNA甲基化的关键酶,还是控制OSCC命运和治疗结果的重要“看门人”。通过靶向DNMT1,科研人员为OSCC的治疗提供了新的策略,这不仅有望提高抗癌疗效,还能降低治疗过程中的毒性作用。随着对DNMT1及其相关信号通路研究的深入,未来可能会开发出更加有效且安全的OSCC治疗方法。
| 名称 | 货号 | 规格 |
| goat anti-rabbit IgG-HRP | abs20040ss | 50ul |
| Goat anti-Rabbit IgG-HRP Antibody | abs20040-500ul | 500ul |



































