上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|Verteporfin-介导的光开关功能协同治疗脉络膜血管疾病的最新研究进展
220 人阅读发布时间:2025-02-27 13:26
引言
脉络膜血管疾病,尤其是年龄相关性黄斑变性(AMD),是全球视力损害的主要原因之一。这些疾病的主要特征是病理性血管新生,即异常血管在视网膜下层的脉络膜中异常增生,从而导致视力下降甚至失明。当前,治疗脉络膜血管疾病的方法之一是使用维替泊芬介导的光动力疗法(PDT)。维替泊芬作为一种光敏剂,能够在光照条件下产生细胞毒性反应,从而选择性封闭脉络膜新生血管,达到治疗效果。然而,临床实践中常用的全身大剂量给药方式会增加全身不良反应的风险,如皮肤及浅表组织的光毒性反应。因此,开发一种更高效、安全的治疗方法,既能有效封闭脉络膜新生血管,又能减少全身不良反应,是当前研究的热点。

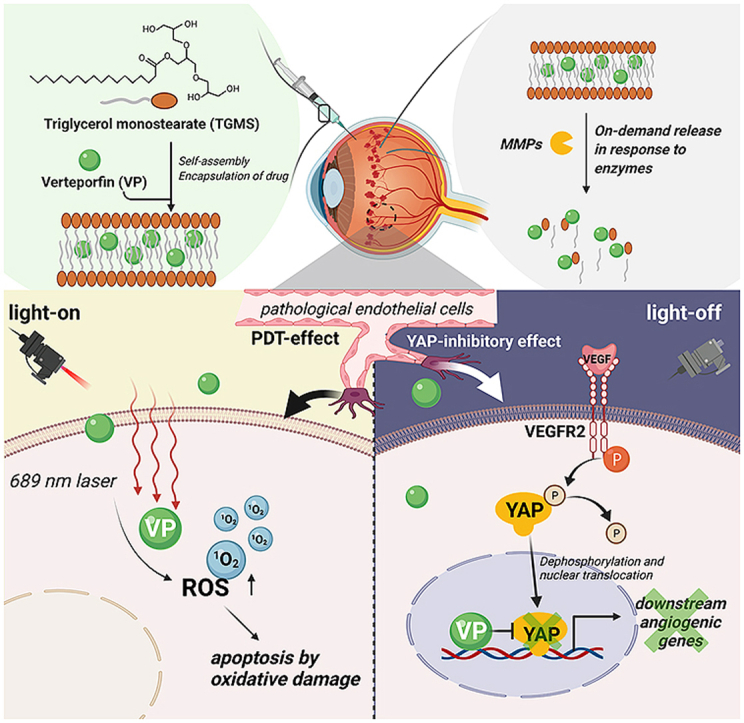
本文报道了一种创新的原位维替泊芬给药系统,该系统结合了光开关协同功能,能够在眼内炎症酶的作用下分解,实现药物的精准释放。该系统在光照条件下进行维替泊芬介导的光动力疗法,有效封闭血管;在无光照条件下,非光活性的维替泊芬则作为YAP(Yes-associated protein)抑制剂,负向调节血管内皮生长因子(VEGF)诱导的血管新生。这种双重作用机制为脉络膜血管疾病的治疗提供了新的策略,具有显著的抗血管新生协同效应。
脉络膜血管疾病与现有治疗方法
脉络膜血管疾病,包括年龄相关性黄斑变性(AMD)、脉络膜新生血管(CNV)等,严重影响患者的视力。这些疾病的发病机制复杂,涉及多种生长因子和炎症介质的相互作用,最终导致脉络膜中异常血管的形成和增殖。病理性血管新生不仅破坏了视网膜的正常结构,还影响了视觉信息的传递和处理,导致视力下降甚至失明。
目前,针对脉络膜血管疾病的治疗方法主要包括激光光凝、光动力疗法(PDT)、抗VEGF药物注射等。激光光凝通过破坏异常血管达到治疗目的,但可能损伤周围正常组织;抗VEGF药物注射能够抑制血管新生,但需要频繁注射,且存在耐药性和眼部不良反应的风险。光动力疗法(PDT)则结合了光敏剂和特定波长的光线,选择性破坏异常血管,具有较高的治疗精准度和安全性。然而,传统PDT治疗需要全身大剂量给药,增加了全身不良反应的风险,限制了其广泛应用。
维替泊芬介导的光动力疗法
维替泊芬是一种卟啉类光敏剂,能够在特定波长的光线照射下产生细胞毒性反应。在PDT治疗过程中,维替泊芬被注射到患者体内,随后通过眼底镜将特定波长的光线聚焦于脉络膜新生血管区域。光线激发维替泊芬分子,产生单线态氧和其他活性氧物质,导致血管内皮细胞损伤和血管封闭。这种治疗方法具有选择性高、创伤小、恢复快等优点,已成为治疗脉络膜血管疾病的重要手段之一。
然而,传统PDT治疗也存在一些局限性。首先,全身大剂量给药会增加全身不良反应的风险,如皮肤光敏反应、肝肾功能损害等。其次,光照条件受限,需要在暗室中进行,且光线照射时间和强度需要严格控制。此外,部分患者对PDT治疗反应不佳,存在复发和耐药性问题。
原位维替泊芬给药系统的设计与功能
为了克服传统PDT治疗的局限性,本文报道了一种创新的原位维替泊芬给药系统。该系统结合了光开关协同功能,能够在眼内炎症酶的作用下分解,实现药物的精准释放和有效利用。
系统设计与制备
该系统由维替泊芬分子、载体材料和响应性连接部分组成。维替泊芬分子作为光敏剂,能够在光照条件下产生细胞毒性反应;载体材料用于装载和稳定维替泊芬分子,同时提供药物释放的通道;响应性连接部分则能够识别眼内炎症酶,并在其作用下分解,从而释放维替泊芬分子。
在制备过程中,首先通过化学键将维替泊芬分子与响应性连接部分结合,形成维替泊芬-连接部分复合物。然后,将复合物装载到载体材料中,形成原位维替泊芬给药系统。该系统具有良好的稳定性和生物相容性,能够在眼内环境中保持较长时间不被降解。
光开关协同功能
该系统具有独特的光开关协同功能。在光照条件下,维替泊芬分子被激发并产生细胞毒性反应,导致脉络膜新生血管封闭。这种光动力疗法具有选择性高、创伤小等优点,能够有效抑制病理性血管新生。
在无光照条件下,非光活性的维替泊芬分子则作为YAP抑制剂发挥作用。YAP是一种重要的转录共激活因子,在血管新生过程中发挥关键作用。维替泊芬通过抑制YAP的活性,负向调节VEGF诱导的血管新生过程。这种双重作用机制使得该系统在抑制病理性血管新生方面具有显著的协同效应。
响应性释放机制
该系统还能够响应眼内炎症酶的作用,实现药物的精准释放。眼内炎症酶如基质金属蛋白酶(MMPs)等在脉络膜血管疾病中表达增加,能够识别并分解响应性连接部分,从而释放维替泊芬分子。这种响应性释放机制使得该系统能够在疾病部位精准释放药物,提高药物的治疗效果和生物利用度。
实验验证与结果分析
为了验证该系统的治疗效果和安全性,本文进行了多项实验研究。
体外实验
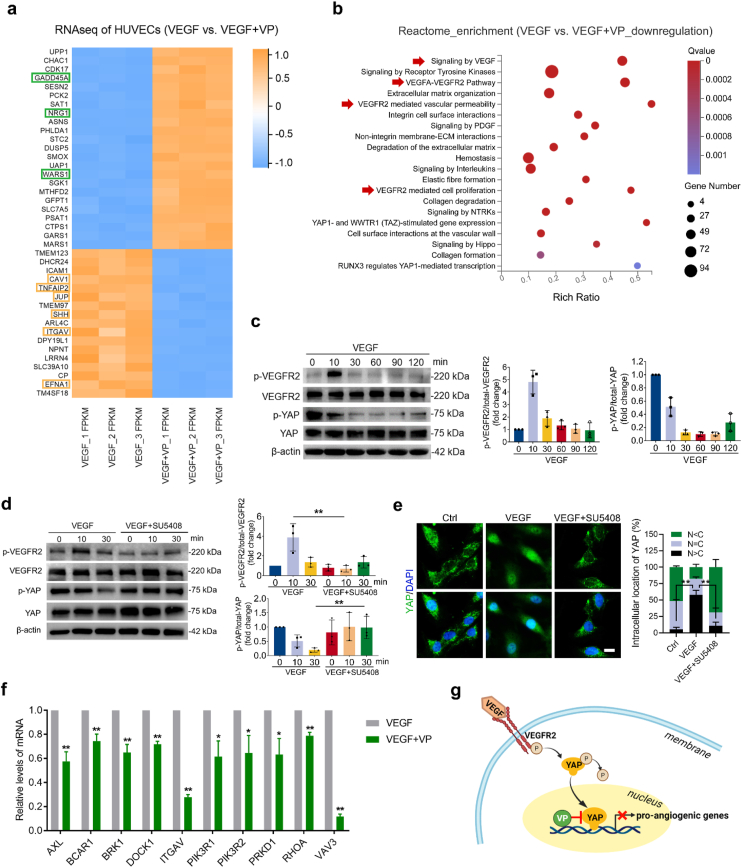
在体外实验中,通过模拟眼内环境,评估了该系统的稳定性和生物相容性。结果显示,该系统在模拟眼内环境中能够保持较长时间不被降解,且对细胞无明显毒性作用。此外,还通过细胞实验验证了该系统在光照和无光照条件下的双重作用机制。结果显示,在光照条件下,该系统能够有效抑制血管内皮细胞的增殖和迁移;在无光照条件下,则能够抑制VEGF诱导的血管新生过程。
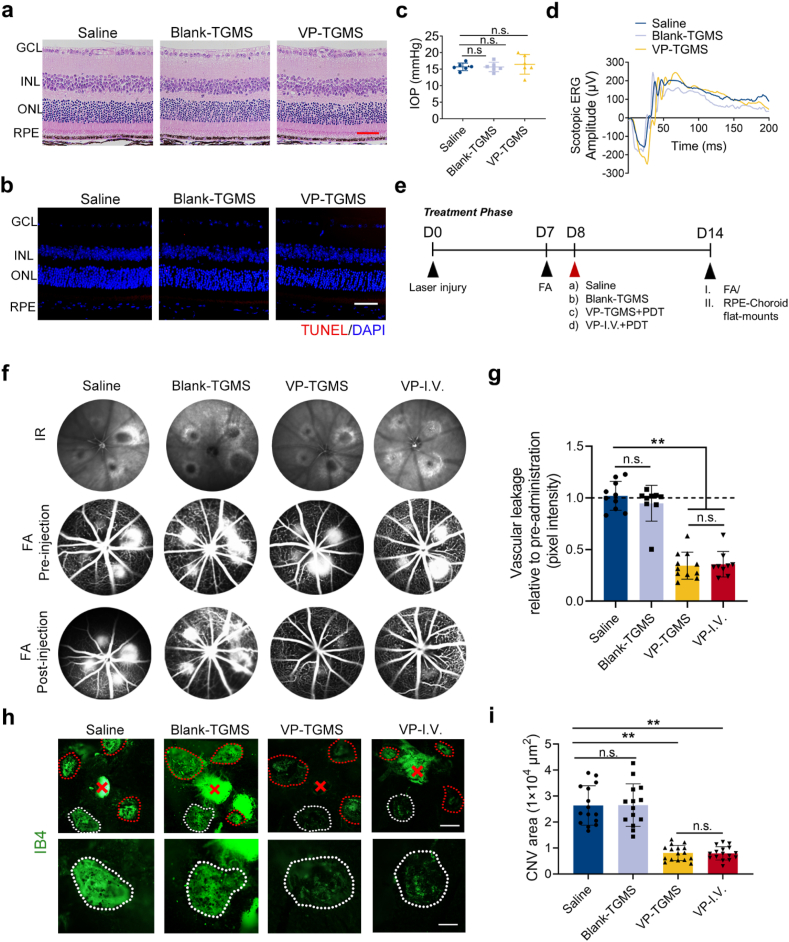
动物实验
在动物实验中,将该系统注射到脉络膜新生血管模型动物的眼内,并观察其治疗效果和安全性。结果显示,该系统能够显著抑制脉络膜新生血管的生长和增殖,减轻视网膜的损伤程度。同时,该系统对动物全身无明显毒性作用,具有较好的安全性和耐受性。
机制探讨
通过对该系统的作用机制进行深入研究,发现其通过光动力疗法和YAP抑制双重作用机制,协同抑制病理性血管新生过程。此外,该系统还能够响应眼内炎症酶的作用,实现药物的精准释放和有效利用。这些机制共同构成了该系统治疗脉络膜血管疾病的独特优势。
结论与展望
本文报道了一种创新的原位维替泊芬给药系统,该系统结合了光开关协同功能,能够在眼内炎症酶的作用下分解并释放药物。该系统在光照条件下进行光动力疗法有效封闭血管;在无光照条件下则作为YAP抑制剂负向调节血管新生过程。这种双重作用机制使得该系统在治疗脉络膜血管疾病方面具有显著的协同效应和治疗效果。
未来,我们将进一步优化该系统的设计和制备工艺,提高其稳定性和生物利用度。同时,将开展更大规模的临床试验,验证其治疗效果和安全性,并探索其在其他眼部疾病中的应用潜力。此外,还将深入研究其作用机制,为开发新型眼部药物递送系统提供理论依据和实践指导。
随着科学技术的不断进步和医疗水平的不断提高,相信未来会有更多创新的治疗方法和手段涌现出来,为脉络膜血管疾病等眼部疾病患者带来更好的治疗效果和生活质量。
| 名称 | 货号 | 规格 |
| rhMMP-9, CF (10 ug) | 911-MP-010 | 10ug |



































