上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|UPP1通过诱导免疫抑制微环境促进肺腺癌进展
246 人阅读发布时间:2025-03-04 13:43
引言
在全球范围内,肺癌导致的死亡在癌症相关死亡中占有显著比例,其中肺腺癌(LUAD)是最主要的类型之一。尽管随着免疫疗法的引入,LUAD的治疗取得了显著进展,但预后不良的情况仍然普遍存在。肿瘤微环境(TME)是一个复杂多样的细胞环境,包括肿瘤细胞、T细胞、B细胞和巨噬细胞等多种免疫细胞,以及内皮细胞和成纤维细胞。在这种环境中,肿瘤细胞与周围的免疫细胞和基质细胞进行复杂的相互作用,形成了免疫抑制环境,抑制了对肿瘤的免疫反应。复旦大学中山医院团队联合多单位在《Nature Communications》上发表了一篇题为“UPP1 promotes lung adenocarcinoma progression through the induction of an immunosuppressive microenvironment”的研究,该研究强调了尿苷磷酸化酶1(UPP1)在LUAD中的免疫抑制作用,为深入了解LUAD的分子特征和促进个性化治疗策略的发展提供了新的视角。
研究背景
肺癌作为恶性肿瘤的一种,在全球范围内具有很高的发病率和死亡率。在男性中,肺癌是发病率最高的癌症,而在女性中则仅次于乳腺癌和宫颈癌。对于肺癌,男性的发病率高于女性。在肺癌中,LUAD是最常见的类型之一,其治疗方法虽然取得了很大进展,但预后不良的情况仍然很多。TME作为肿瘤发生、发展和预后的关键环境,包含多种类型的细胞,其中肿瘤细胞与免疫细胞的相互作用尤为重要。这些相互作用不仅影响肿瘤的生长和转移,还决定了肿瘤对治疗的敏感性。因此,研究TME中的分子机制,尤其是与免疫抑制相关的机制,对于提高LUAD的治疗效果具有重要意义。
研究方法
单细胞RNA测序(scRNA-seq)数据分析
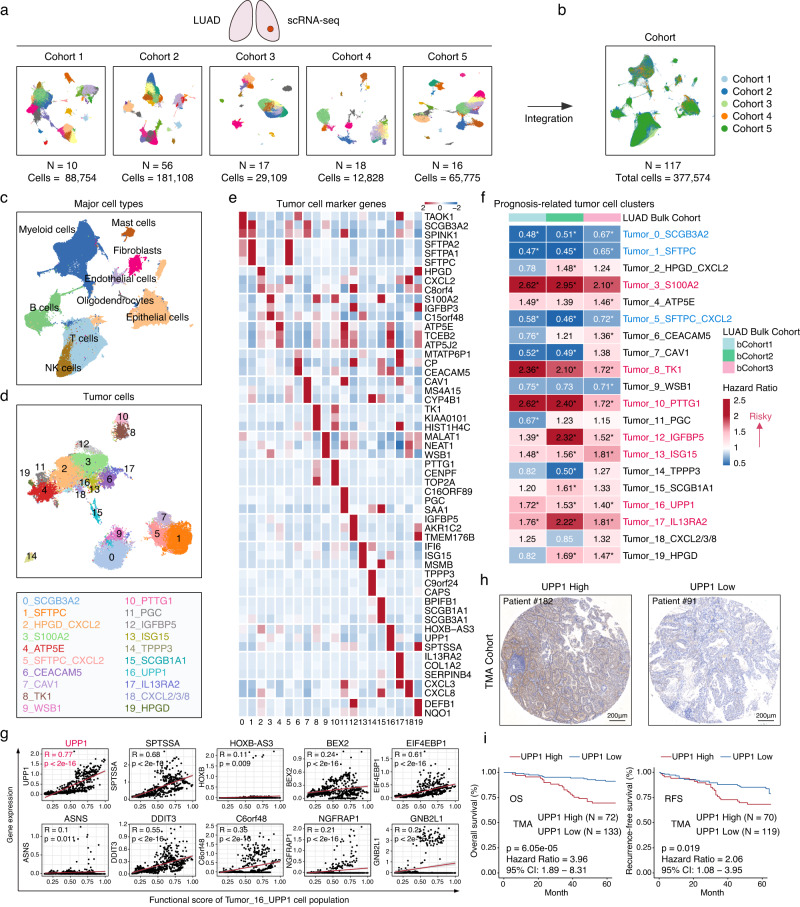
为了深入研究LUAD的TME特征,作者对117例LUAD患者的377,574个细胞进行了综合单细胞RNA测序(scRNA-seq)数据分析。通过将scRNA-seq数据与大量基因表达数据联系起来,作者确定了一组与预后相关的UPP1高表达肿瘤细胞。这一发现为后续的研究提供了重要的基础数据。
多重免疫荧光染色(mIHC)
为了进一步验证scRNA-seq的结果,作者对来自LUAD的患者样本进行了多重免疫荧光染色(mIHC)。通过这种方法,作者发现UPP1高表达的肿瘤细胞主要位于肿瘤的侵袭性前沿,并且与FOXP3+ Tregs(调节性T细胞)、MMP11+成纤维细胞、LAG3+PDCD1+CD8+耗竭T细胞和SPP1+巨噬细胞在空间距离上更接近。这一发现表明,UPP1高表达的肿瘤细胞与免疫抑制成分之间的关联更强,进一步支持了UPP1在诱导免疫抑制微环境中的作用。
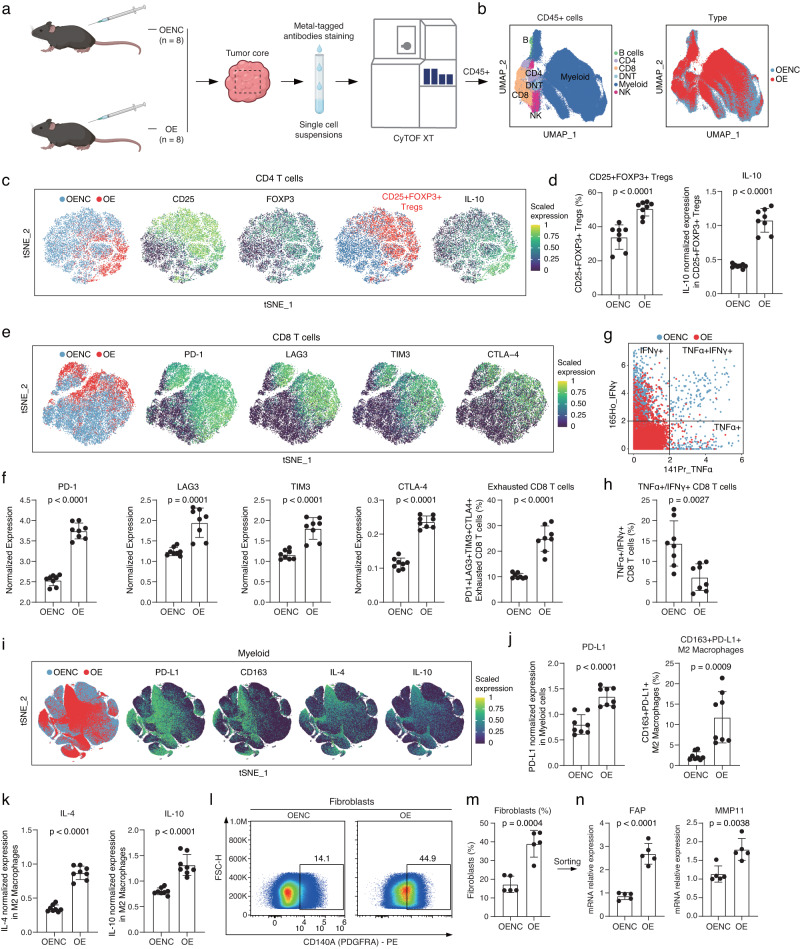
CyTOF分析
为了更深入地了解TME中各种细胞之间的相互作用,作者还进行了CyTOF分析。这种技术通过飞行时间质谱仪同时检测多个细胞表面和内部的蛋白质标志物,能够更精确地描绘出TME中的细胞组成和相互作用网络。CyTOF分析的结果为UPP1在形成免疫抑制性TME中的作用提供了进一步的证据。
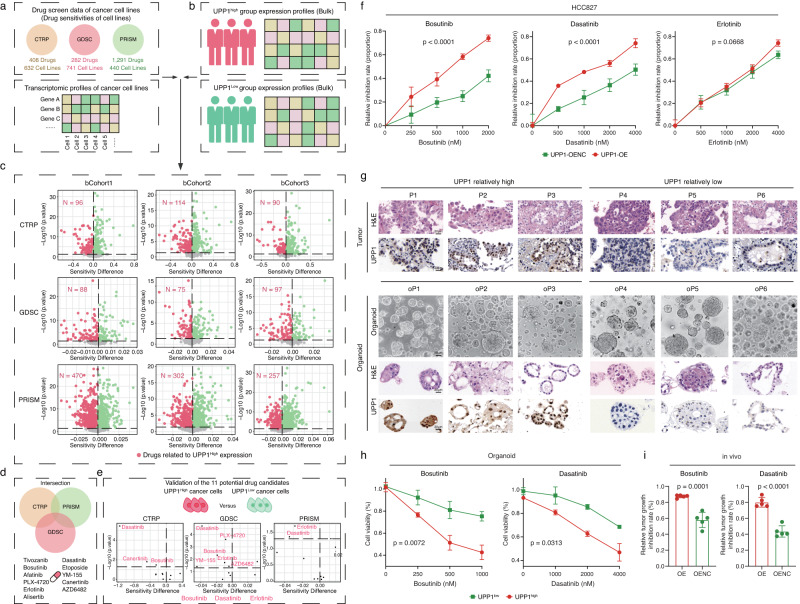
类器官和小鼠实验
为了验证UPP1在LUAD中的功能,作者还建立了6例LUAD患者来源的类器官,并进行了小鼠实验。这些实验发现,UPP1高的肿瘤对波苏替尼和达沙替尼的敏感性相对增加,这表明UPP1可能成为LUAD治疗的新靶点。
主要发现
UPP1与肿瘤侵袭和免疫抑制相关
通过scRNA-seq数据分析,作者发现了一组与预后相关的UPP1高表达肿瘤细胞。进一步的功能富集分析显示,这些肿瘤细胞与肿瘤侵袭、PI3K/AKT/mTOR信号通路、MAPK通路等显著相关。这些通路又与炎症反应和免疫反应调节有关,表明UPP1在LUAD中的功能可能与肿瘤侵袭和免疫抑制密切相关。
UPP1高表达的肿瘤细胞位于肿瘤侵袭前沿
通过多重免疫荧光染色,作者发现UPP1高表达的肿瘤细胞主要定位于肿瘤的侵袭前沿。这些肿瘤细胞与FOXP3+ Tregs、MMP11+成纤维细胞、LAG3+PDCD1+CD8+耗竭T细胞和SPP1+巨噬细胞在空间距离上更接近。这一发现进一步支持了UPP1在诱导免疫抑制微环境中的作用,并提示UPP1高表达的肿瘤细胞可能通过与其他免疫抑制成分的相互作用,促进肿瘤的侵袭和转移。
UPP1上调影响免疫抑制细胞因子和PD-L1的表达
作者使用抗体阵列技术对过表达UPP1的LUAD细胞系中细胞因子表达的变化进行了评估。结果显示,多种细胞因子的表达显著上调,包括TGF-β1、GM-CSF、IL-1β、IL-6、IGFBP-3、CXCL5、CCL20和VEGF,其中TGF-β1升高最为显著。随后的ELISA实验证实,UPP1上调后肿瘤细胞的TGF-β1分泌水平也显著增加。此外,作者还发现UPP1在肿瘤细胞中的表达水平与PD-L1呈正相关,共培养及流式分析表明UPP1诱导的PD-L1表达可能影响CD8+T细胞的杀伤能力。这一发现表明,UPP1不仅通过调节细胞因子释放来影响免疫抑制微环境,还可能通过调节PD-L1的表达来影响T细胞的杀伤功能。
UPP1通过PI3K/AKT/mTOR通路调节PD-L1表达
为了明确PD-L1的表达机制,作者对已知调节UPP1高肿瘤细胞中PD-L1的六种经典信号通路进行了富集分析。结果显示,PI3K/AKT/mTOR通路在UPP1高肿瘤细胞中最活跃。进一步的实验表明,抑制UPP1可以下调PD-L1的表达,而激活PI3K/AKT/mTOR通路可以逆转这种下调效应。这表明UPP1通过激活PI3K/AKT/mTOR通路来调节PD-L1的表达,进而影响T细胞的杀伤功能。
CyTOF分析为UPP1在免疫抑制中的作用提供证据
CyTOF分析为UPP1在形成免疫抑制性TME中的作用提供了进一步的证据。通过CyTOF技术,作者能够更精确地描绘出TME中的细胞组成和相互作用网络。结果显示,UPP1高表达的肿瘤细胞与多种免疫抑制成分之间存在密切的相互作用关系,进一步支持了UPP1在诱导免疫抑制微环境中的作用。
类器官和小鼠实验验证UPP1的功能
为了验证UPP1在LUAD中的功能,作者建立了6例LUAD患者来源的类器官,并进行了小鼠实验。这些实验发现,UPP1高的肿瘤对波苏替尼和达沙替尼的敏感性相对增加。这表明UPP1可能成为LUAD治疗的新靶点,为未来的个性化治疗策略提供了潜在的新途径。
研究意义
本研究首次揭示了UPP1在LUAD中的免疫抑制作用,并阐明了其通过诱导免疫抑制微环境促进肿瘤进展的机制。这些发现不仅有助于深入了解LUAD的分子特征,还为未来的个性化治疗策略提供了新的视角和潜在靶点。具体来说,本研究的意义体现在以下几个方面:
-
揭示新的肿瘤免疫抑制机制:本研究发现UPP1通过调节肿瘤细胞对糖酵解抑制剂的敏感性、影响免疫抑制细胞因子的释放和PD-L1的表达等方式,诱导免疫抑制微环境,进而促进LUAD的进展。这一发现为揭示新的肿瘤免疫抑制机制提供了重要依据。
-
为LUAD治疗提供新靶点:本研究发现UPP1高的肿瘤对波苏替尼和达沙替尼的敏感性相对增加,这表明UPP1可能成为LUAD治疗的新靶点。未来的研究可以进一步探索针对UPP1的抑制剂或药物组合,以提高LUAD的治疗效果。
-
促进个性化治疗策略的发展:本研究强调了UPP1在LUAD中的重要作用,为未来的个性化治疗策略提供了潜在的新途径。通过结合患者的基因型和分子特征,可以制定更加精准的治疗方案,提高LUAD的预后和生存率。
结论与展望
本研究通过scRNA-seq、mIHC、CyTOF分析以及类器官和小鼠实验等多种技术手段,揭示了UPP1在LUAD中的免疫抑制作用及其机制。这些发现不仅有助于深入了解LUAD的分子特征,还为未来的个性化治疗策略提供了新的视角和潜在靶点。未来的研究可以进一步探索UPP1的调控机制、与其他分子的相互作用关系以及针对UPP1的抑制剂或药物组合等,以期提高LUAD的治疗效果并改善患者的预后。此外,随着免疫疗法的不断发展和完善,未来的研究还可以探索将UPP1作为免疫治疗的靶点之一,以进一步提高LUAD的治疗效果和生存率。
综上所述,本研究为LUAD的治疗提供了新的思路和策略,为未来的研究奠定了坚实的基础。随着技术的不断进步和研究的深入,相信未来会有更多关于LUAD分子机制和个性化治疗策略的发现和突破。
| 名称 | 货号 | 规格 |
| InVivoMAb anti-mouse PD-L1 (B7-H1) | BE0101-50MG | 50mg |
| InVivoMAb anti-mouse PD-L1 (B7-H1) | BE0101-100MG | 100mg |
| FICOLL PAQUE PLUS 6X500 ML | 17144003 | 6×500ml |
| Collagenase, Type 4 | LS004188 | 1gm |