上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|诱导“自噬性铁死亡”——天津大学合作发现肝癌治疗新靶点
354 人阅读发布时间:2025-03-04 13:45
引言
肝癌是全球癌症相关死亡的第三大原因,其中肝细胞癌(HCC)占所有肝癌病例的75%-85%。近年来,随着对肝癌发病机制的深入研究,激活的Wnt/β-catenin通路被证实是肝癌发生发展的关键遗传事件。然而,尽管Wnt/β-catenin信号通路抑制剂在肝癌治疗中的潜力被广泛研究,但由于它们通常靶向β-catenin复合体或β-catenin上游通路,导致在正常细胞中不可避免地产生靶毒性,这些抑制剂均未获得临床批准。因此,迫切需要对β-catenin下游可作为药物靶点的效应分子进行研究,以寻找更有效的肝癌治疗方法。
近日,天津大学与夏威夷大学的研究人员在国际权威期刊《Nature Communications》上发表了一篇题为“SLC13A3 is a major effector downstream of activated β-catenin in liver cancer pathogenesis”的研究论文。该研究发现了SLC13A3是肝癌中β-catenin下游的一个重要效应因子,其表达升高与β-catenin的激活密切相关,并且抑制SLC13A3可显著抑制β-catenin驱动的肝癌发生,为肝癌治疗提供了新的靶点。本文将对该研究进行详细的文献解析。

研究背景
肝癌的发病机制
肝癌的发生和发展是一个复杂的过程,涉及多种遗传和表观遗传改变。其中,Wnt/β-catenin信号通路的异常激活被认为是肝癌发生发展的关键遗传事件之一。Wnt/β-catenin信号通路在胚胎发育、组织修复和细胞增殖等过程中发挥着重要作用。然而,当该通路被异常激活时,会导致细胞增殖失控,进而促进肿瘤的发生和发展。
CTNNB1是编码β-catenin的基因,在80%以上的儿童肝癌和20%-40%的成人肝癌中检测到CTNNB1的功能获得性(GOF)突变。这些突变导致β-catenin在细胞内积累,并持续激活Wnt/β-catenin信号通路,从而促进肝癌的进展和转移。
Wnt/β-catenin抑制剂的局限性
鉴于Wnt/β-catenin信号通路在肝癌中的关键作用,研究人员一直致力于开发针对该通路的抑制剂。然而,目前开发的抑制剂主要靶向β-catenin复合体或β-catenin上游通路,这导致在正常细胞中不可避免地产生靶毒性,限制了它们的临床应用。因此,迫切需要寻找新的药物靶点,以实现对肝癌的精准治疗。
溶质载体(SLC)转运体的研究前景
溶质载体(Solute carrier, SLC)转运体是一类调节多种溶质、代谢物、离子和药物跨细胞膜输入和流出的蛋白质。在包括肝癌在内的多种癌症中,SLC转运蛋白的表达模式发生了显著变化。这些变化不仅影响癌症细胞的代谢和增殖,还可能为癌症治疗提供新的靶点。因此,研究SLC转运体在肝癌中的作用机制具有重要意义。
研究方法
研究对象的确定
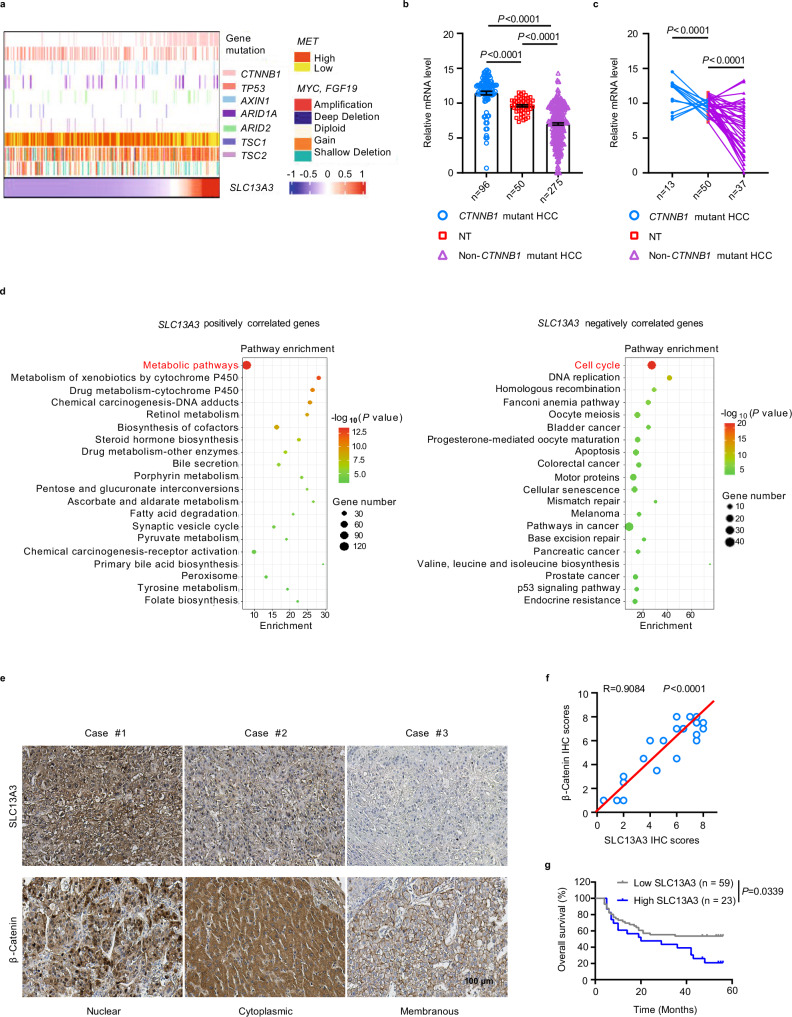
研究人员首先通过对TCGA-LIHC数据集的综合分析,确定了三种HCC亚型(iHCC1-3)。他们发现,在这些亚型中,SLC13A3 mRNA在CTNNB1突变发生率高的iHCC2亚型中显著高表达。这表明SLC13A3可能与β-catenin的激活密切相关。
实验设计与实施
为了进一步研究SLC13A3在肝癌中的作用机制,研究人员进行了以下实验:
- 细胞实验:研究人员使用人肝癌细胞系HepG2和SNU398,通过基因沉默和小分子抑制剂处理,观察SLC13A3对细胞增殖、克隆形成能力和存活率的影响。
- 动物实验:研究人员构建了β-catenin驱动的肝癌小鼠模型,并通过腹腔注射小分子抑制剂ACA,观察其对肝癌生长和转移的影响。
- 分子生物学实验:通过蛋白质免疫印迹实验、IHC分析和脂质ROS检测等方法,研究人员探讨了ACA抑制肝癌细胞生长的潜在机制。
研究结果
SLC13A3在肝癌中的表达与功能
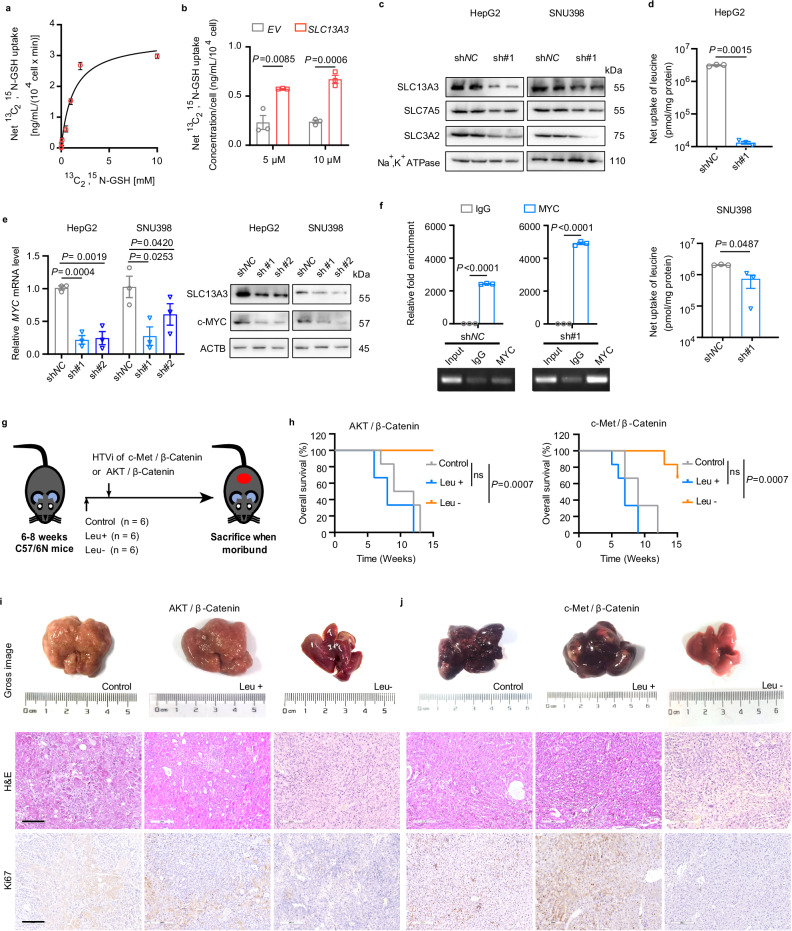
研究结果表明,SLC13A3在β-catenin编码基因CTNNB1(GOF突变)的人肝癌样本中表达升高。β-catenin的激活上调了SLC13A3的表达,导致内源性SLC13A3底物在细胞内蓄积。进一步的研究发现,SLC13A3被鉴定为谷胱甘肽(GSH)的低亲和力转运蛋白。沉默SLC13A3通过c-MYC信号通路下调亮氨酸转运蛋白SLC7A5,导致亮氨酸消耗和mTOR失活。此外,在β-catenin激活的肝癌细胞中,沉默SLC13A3可减少GSH并诱导自噬性铁死亡。
小分子抑制剂ACA的抗癌作用
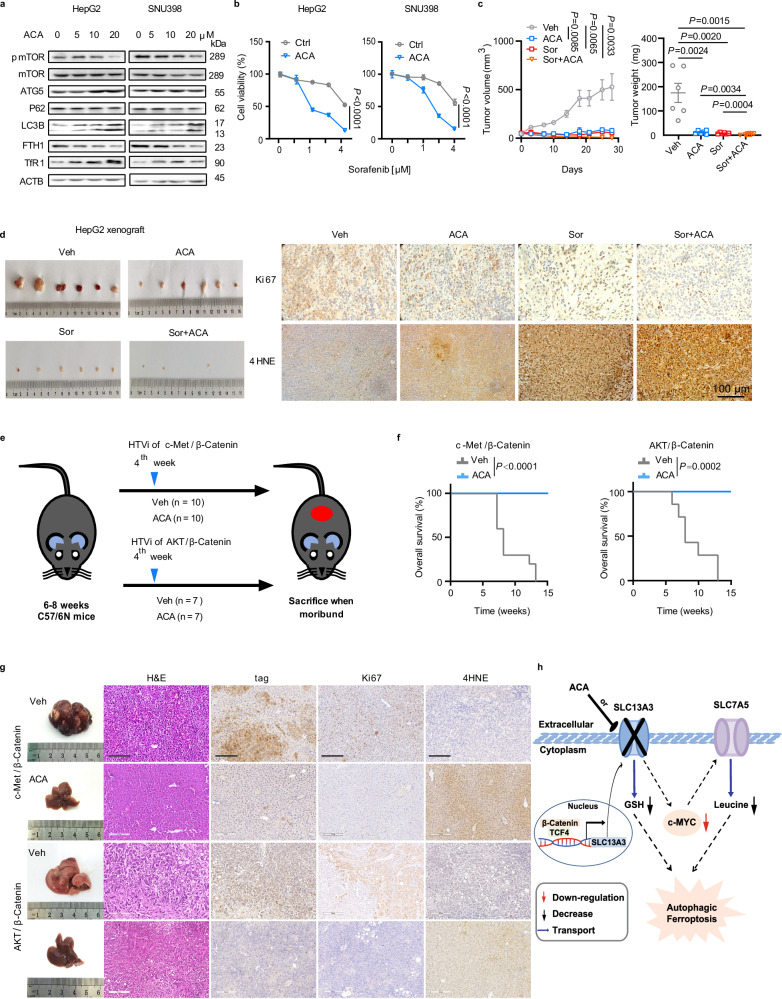
研究人员发现,小分子抑制剂ACA可以显著抑制人肝癌细胞HepG2和SNU398的增殖和克隆形成能力。ACA以剂量依赖的方式降低了SLC13A3的mRNA和蛋白质水平,并诱导了自噬和铁死亡。尽管ACA也抑制了其他SLC转运体(如SLC13A2和SLC13A5),但肝脏组织中SLC13A2的表达较低,且在肝癌细胞中几乎检测不到其表达。此外,尽管HepG2和Huh7细胞中SLC13A5的mRNA高度表达,但在其他HCC细胞中(包括β-连环激活的细胞)几乎检测不到SLC13A5的表达。这表明SLC13A3是ACA抑制肝癌细胞生长的主要靶点。
除了SLC13A转运体外,研究人员还发现ACA可以抑制PLA2、TRPM2和AP2M1。然而,在肝癌细胞中几乎检测不到TRPM2的表达,且抑制PLA2和AP2M1已被证明可抑制自噬。尽管如此,ACA却在HCC细胞中诱导了自噬。这些发现表明,ACA至少部分通过抑制SLC13A3来抑制HCC细胞活力。
为了确定ACA是否与SLC13A3基因抑制具有相似的作用,研究人员分析了ACA介导的细胞生长抑制的潜在机制。他们发现,ACA对细胞凋亡没有显著影响,但其生长抑制作用可以通过抑制自噬和铁死亡来缓解。ACA诱导的铁死亡进一步通过升高脂质ROS得到证实。蛋白质免疫印迹实验分析显示,ACA以剂量依赖的方式诱导自噬和铁死亡的生物标志物。此外,ACA与索拉非尼在HepG2和SNU398细胞的细胞存活和克隆形成方面显示出协同作用。
ACA在体内对小鼠肝癌的抑制作用
研究人员进一步研究了ACA在体内对小鼠肝癌的作用。他们发现,在正常C57BL/6 N或裸小鼠BALB/C中,ACA未引起明显的毒性反应。在裸小鼠BALB/C中,ACA(30 mg/kg,每隔一天腹腔注射)有效地抑制了皮下HepG2异种移植物的生长,并与索拉非尼呈协同作用。蛋白质免疫印迹实验和IHC分析显示,ACA在HepG2异种移植物中诱导了自噬和铁死亡。
为了进一步研究ACA对β-连环蛋白驱动的肝癌的影响,研究人员从注射c-Met/β-连环蛋白和AKT/β-连环蛋白质粒的第4周开始,将30 mg/kg的ACA腹腔注射给C57BL/6 N小鼠。IHC和蛋白质免疫印迹实验分析显示,ACA诱导了自噬和铁死亡。这些发现表明,ACA对β-连环蛋白激活的肝癌具有与基因抑制SLC13A3相似的作用。
研究结论与展望
本研究强调了SLC13A3在β-catenin激活的肝癌中调节铁死亡的重要性。研究人员认为,β-catenin激活的肝癌对SLC13A3抑制表现出特异性敏感性。因此,抑制SLC13A3是一种有前景的靶向肝癌β-catenin信号通路的策略,且不会产生明显的不良反应。
未来的研究可以进一步探讨SLC13A3在肝癌中的具体作用机制,以及开发针对SLC13A3的特异性抑制剂。此外,还可以研究SLC13A3与其他信号通路(如自噬和铁死亡相关通路)的相互作用,以更全面地了解其在肝癌发生和发展中的作用。这些研究将有助于为肝癌患者提供更有效的治疗策略,提高患者的生存率和生活质量。
文献解析总结
本文详细解析了天津大学与夏威夷大学研究人员在《Nature Communications》上发表的研究论文“SLC13A3 is a major effector downstream of activated β-catenin in liver cancer pathogenesis”。该研究发现了SLC13A3是肝癌中β-catenin下游的一个重要效应因子,其表达升高与β-catenin的激活密切相关。通过基因沉默和小分子抑制剂处理,研究人员发现抑制SLC13A3可显著抑制β-catenin驱动的肝癌发生。进一步的研究表明,小分子抑制剂ACA可以通过抑制自噬和铁死亡来抑制肝癌细胞的生长,并在小鼠模型中显示出显著的抗癌效果。
本研究不仅为肝癌治疗提供了新的靶点,还揭示了SLC13A3在肝癌发生和发展中的重要作用。未来的研究可以进一步探讨SLC13A3的具体作用机制,以及开发针对该靶点的特异性抑制剂,为肝癌患者提供更有效的治疗策略。同时,该研究也为其他癌症的治疗提供了新的思路和启示,有望推动癌症精准治疗的发展。
| 名称 | 货号 | 规格 |
| ISOPLATE-96 /50W | 6005040 | EA |
| InVivoMAb anti-mouse PD-L1 (B7-H1) | BE0101-100MG | 100mg |
| FICOLL PAQUE PLUS 6X500 ML | 17144003 | 6×500ml |
| Collagenase, Type 4 | LS004188 | 1gm |