上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|探索肌红蛋白负载的钆纳米德克萨斯菲林:氧气协同与成像引导放疗增敏的新纪元
118 人阅读发布时间:2025-04-15 10:49
一、引言
在临床肿瘤治疗中,放疗作为重要的治疗手段之一,其疗效往往受限于肿瘤组织的乏氧状态。乏氧环境不仅降低了放疗对肿瘤细胞的直接杀伤效果,还促进了肿瘤细胞的放疗抵抗性。因此,如何改善肿瘤乏氧状态,提高放疗效果,一直是肿瘤治疗领域的研究热点。近期,一篇题为“Myoglobin-loaded Gadolinium Nanotexaphyrins for Oxygen Synergy and Imaging-Guided Radiosensitization Therapy”的研究文章为我们提供了一个创新性的解决方案。

二、研究背景
钆(Gd3+)配位的德克萨斯菲林(Texaphyrin,简称Tex)作为一种潜在的放疗增敏剂,已经进入了临床试验阶段。然而,由于其放疗增敏效果不足,该药物的临床应用暂时受阻。传统的改善方法大多聚焦于药物化学结构的优化,而对于利用纳米载体提高药物疗效的研究则相对较少。本研究在此基础上,提出了一种新的策略:将Gd-Tex转化为构建块“Gd-Tex-lipids”,进而自组装成纳米囊泡——钆纳米德克萨斯菲林(Gadolinium Nanotexaphyrins,简称Gd-NTs)。这种纳米结构不仅实现了Gd-Tex在单个纳米囊泡中的高密度堆积,还提高了其在肿瘤组织中的积聚,为改善放疗效果提供了可能。
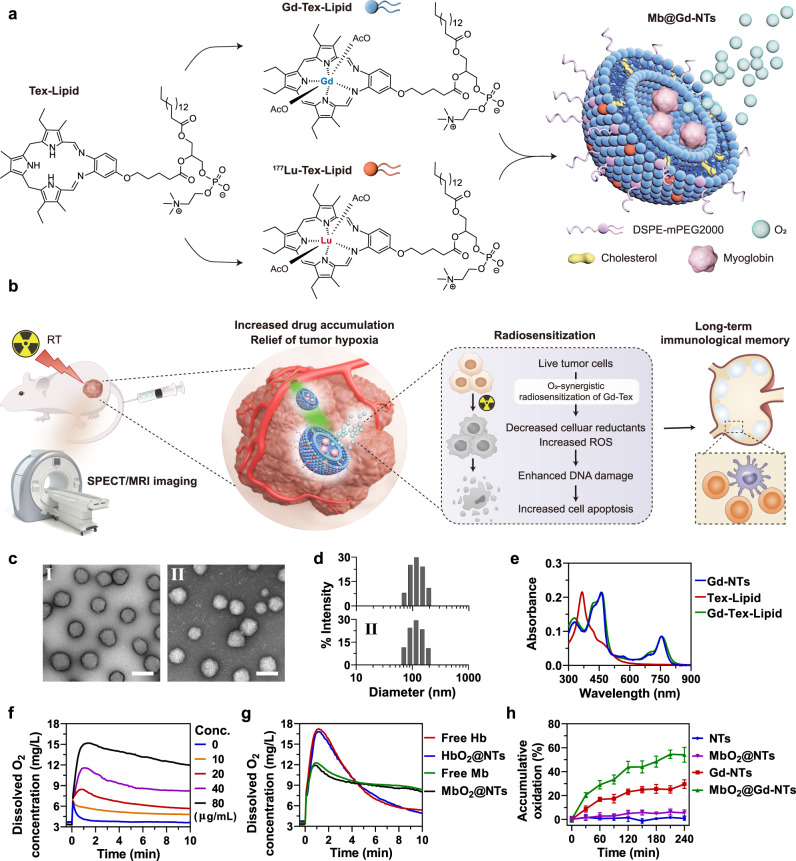
三、研究方法
- Gd-NTs的制备与表征
研究者首先通过化学反应将Gd-Tex转化为Gd-Tex-lipids,然后利用这些脂质分子自组装成纳米囊泡Gd-NTs。通过透射电子显微镜(TEM)和动态光散射(DLS)等技术,对Gd-NTs的形貌、大小和稳定性进行了表征。结果表明,Gd-NTs具有均匀的球形结构,大小适中,且具有良好的稳定性。
- Mb@Gd-NTs的制备与性能评估
为了进一步提高Gd-NTs的放疗增敏效果,研究者将肌红蛋白(Myoglobin,简称Mb)载入Gd-NTs中,形成了Mb@Gd-NTs。Mb作为一种高效的氧载体,能够显著缓解肿瘤组织的乏氧状态。通过光谱分析和氧释放实验,研究者对Mb@Gd-NTs的氧携带和释放能力进行了评估。结果显示,Mb@Gd-NTs具有较高的氧携带量,且能够在需要时快速释放氧气。
- 体外放疗增敏效果评估
研究者利用培养的肿瘤细胞,对Mb@Gd-NTs的体外放疗增敏效果进行了评估。通过比较不同处理组(单纯放疗组、Gd-NTs+放疗组、Mb@Gd-NTs+放疗组)的细胞存活率,研究者发现Mb@Gd-NTs能够显著提高放疗对肿瘤细胞的杀伤效果。这一结果初步证实了Mb@Gd-NTs的放疗增敏作用。
- 体内成像与放疗增敏效果评估
为了验证Mb@Gd-NTs在体内的成像和放疗增敏效果,研究者进行了小动物MRI/SPECT/CT成像实验。通过比较不同时间点的成像结果,研究者发现Mb@Gd-NTs能够准确地靶向肿瘤组织,并在肿瘤组织中积聚。同时,研究者还利用肿瘤小鼠模型,对Mb@Gd-NTs的体内放疗增敏效果进行了评估。结果表明,Mb@Gd-NTs能够显著抑制肿瘤的生长,并延长小鼠的生存时间。
- 放疗增敏机制的初步探讨
为了深入了解Mb@Gd-NTs的放疗增敏机制,研究者进行了一系列生物学实验。通过检测肿瘤组织中的氧浓度、ROS水平、DNA损伤程度等指标,研究者发现Mb@Gd-NTs能够通过缓解肿瘤乏氧状态,增加ROS的产生,进而加重DNA损伤,从而提高放疗效果。
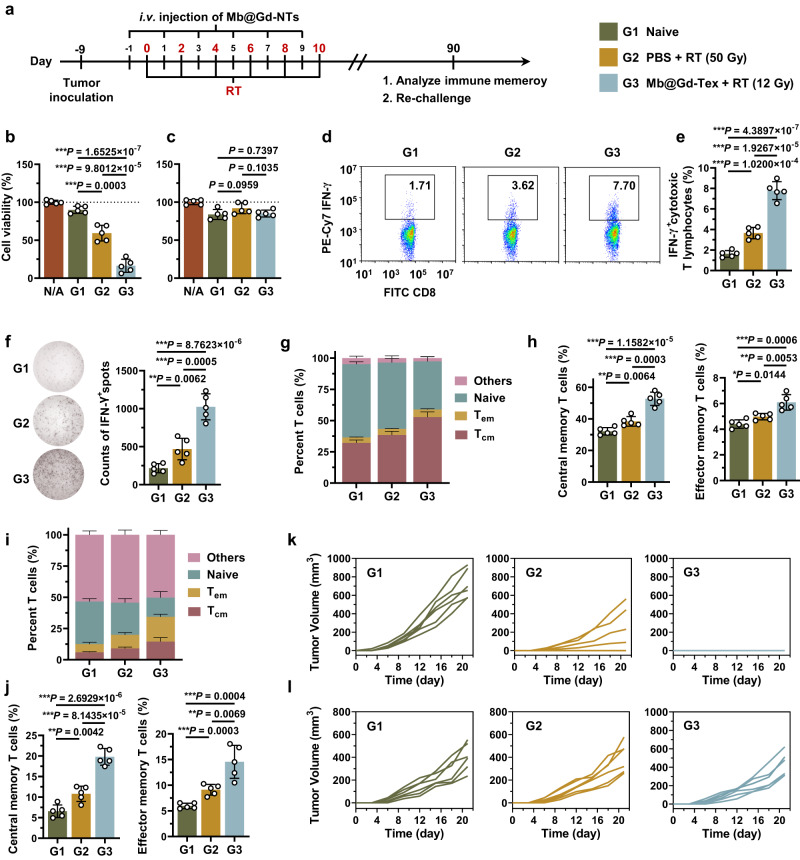
四、研究结果与讨论
- Gd-NTs作为纳米载体的优势
本研究通过将Gd-Tex转化为Gd-Tex-lipids,并自组装成纳米囊泡Gd-NTs,实现了Gd-Tex在单个纳米囊泡中的高密度堆积。这种纳米结构不仅提高了Gd-Tex在肿瘤组织中的积聚,还降低了其被机体清除的可能性,从而提高了药物的生物利用度和疗效。
- Mb@Gd-NTs的放疗增敏效果
本研究通过将Mb载入Gd-NTs中,形成了Mb@Gd-NTs。Mb作为一种高效的氧载体,能够显著缓解肿瘤组织的乏氧状态,从而提高了放疗对肿瘤细胞的杀伤效果。实验结果表明,Mb@Gd-NTs能够显著提高放疗的敏感性,抑制肿瘤的生长,并延长小鼠的生存时间。
3.SPECT/MRI双模态成像的应用价值
本研究还利用SPECT/MRI双模态成像技术,对Mb@Gd-NTs在体内的分布和代谢进行了实时监测。这种成像技术不仅能够提供准确的肿瘤定位信息,还能够反映药物的代谢过程,为药物的临床应用提供了有力的支持。
- 放疗增敏机制的初步揭示
本研究通过一系列生物学实验,初步揭示了Mb@Gd-NTs的放疗增敏机制。结果表明,Mb@Gd-NTs能够通过缓解肿瘤乏氧状态,增加ROS的产生,进而加重DNA损伤,从而提高放疗效果。这一机制的揭示为我们深入理解放疗增敏药物的疗效提供了新的视角。
五、结论与展望
本研究通过将Gd-Tex转化为纳米囊泡Gd-NTs,并载入Mb形成了Mb@Gd-NTs,实现了一种新的放疗增敏策略。实验结果表明,Mb@Gd-NTs能够显著提高放疗的敏感性,抑制肿瘤的生长,并延长小鼠的生存时间。同时,SPECT/MRI双模态成像技术的应用也为药物的临床应用提供了有力的支持。未来,我们将进一步深入研究Mb@Gd-NTs的放疗增敏机制,优化其制备工艺和给药方式,以期为其临床应用提供更为坚实的理论基础和实践指导。



































