上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|肾脏YY1-KIM1-DR5轴在急性肾损伤进展中的关键调控作用
171 人阅读发布时间:2025-04-15 10:50
引言
急性肾损伤(AKI)作为一种全球性的健康问题,每年影响着超过1000万人的健康,并导致约170万人死亡。其高发病率和高死亡率使其成为医学界亟待解决的重要课题。AKI的诱因多种多样,包括临床手术中的缺血再灌注、尿道梗阻,以及多种药物如铂类化疗药物、降血压药物、抗生素和造影剂等的使用。AKI不仅会导致肾脏的急性功能障碍,还可能引发长期的慢性肾脏疾病(CKD),并最终可能发展成为终末期肾病。尽管AKI的严重性不容忽视,但其复杂的发病机制以及缺乏有效的药物治疗策略,使得对该疾病的防控和治疗充满挑战。
近期,武汉大学郑凌教授和华中科技大学同济药学院黄昆教授、陈红副教授的合作研究,在Nature Communications上发表了一篇题为“A renal YY1-KIM1-DR5 axis regulates the progression of acute kidney injury”的文章。该研究揭示了肾损伤分子KIM1在AKI中的重要作用机制,并通过干预靶点设计出了拮抗肽,为AKI的治疗提供了新的思路。

肾损伤分子KIM1与AKI
肾损伤分子KIM1是一种跨膜糖蛋白,主要在肾脏中表达,且生理状态下表达水平较低。然而,在AKI发生时,KIM1的表达会迅速上调,并能够灵敏、特异地反映肾脏的损伤程度。因此,KIM1被美国食品药品监督管理局(FDA)批准作为多种肾脏疾病的早期生物标志物。
除了作为生物标志物外,KIM1还参与多种生理病理活动。由于其表达于上皮细胞,KIM1能够介导多种胞内外信号的传递,从而发挥多种效应。例如,KIM1被报道参与病毒入侵、免疫应答、组织损伤与修复以及肿瘤的发生发展等过程。然而,关于KIM1在AKI发展中的具体角色和分子作用机制,尚有待深入研究。
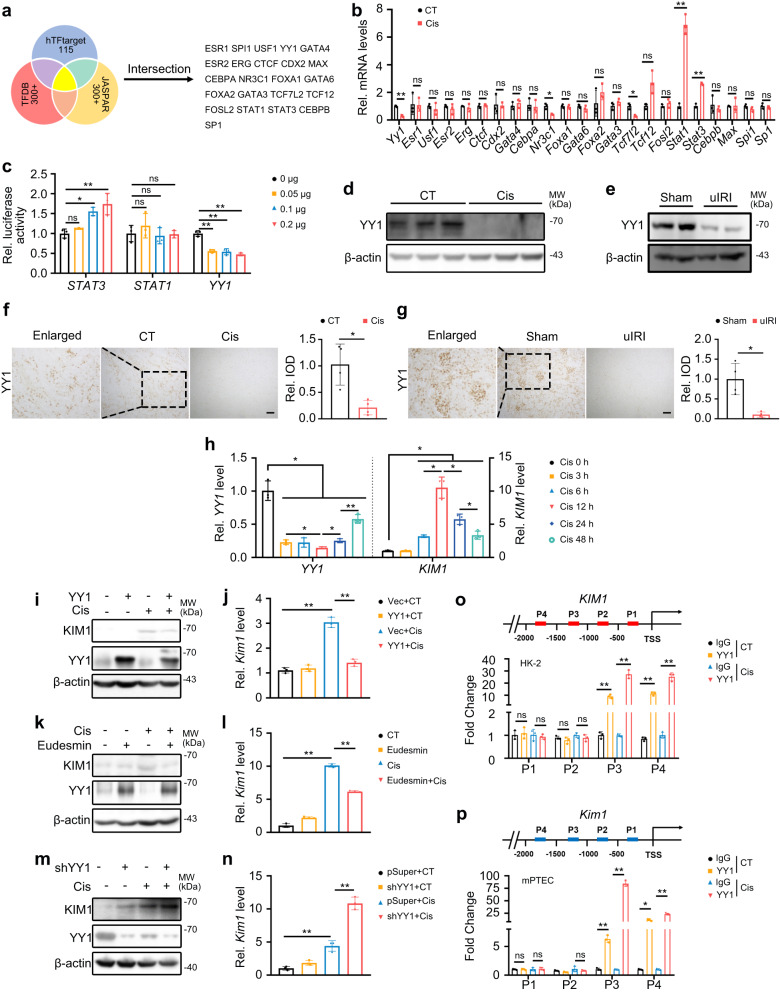
在本研究中,研究人员首先发现KIM1在AKI模型中显著上调。通过进一步的研究,他们发现KIM1过表达的肾小管上皮细胞在受到顺铂刺激时,会促进细胞凋亡和炎症因子上调。相反,KIM1敲除则可以缓解顺铂所诱导的细胞凋亡,并抑制炎症因子的表达。这些结果表明,KIM1在AKI中可能通过促进细胞凋亡来加重肾脏损伤。
KIM1与DR5的结合及其作用机制
为了深入探究KIM1在AKI中的作用机制,研究人员进一步研究了KIM1的下游效应分子。他们发现,KIM1能够与DR5结合,并在损伤条件下,这种结合有增强的趋势。DR5是一种重要的凋亡相关分子,其上调与肾损伤密切相关。
通过Co-IP和FRET实验,研究人员证明了KIM1与DR5间确实存在结合。进一步的研究发现,KIM1过表达会促进顺铂诱导的DR5寡聚化,而KIM1敲除则抑制这一过程。DR5的寡聚化是凋亡信号传导的关键步骤之一,能够激活Caspase级联反应,诱导细胞凋亡。
研究人员还通过构建肾小管特异性敲除Kim1的小鼠(Kim1Ksp-KO),进一步验证了KIM1在AKI中的作用。实验结果显示,Kim1Ksp-KO小鼠在顺铂诱导的AKI模型中,其血清肌酐和尿素氮水平均低于野生型(WT)小鼠,肾小管上皮细胞脱落及管腔扩张等现象也减少,表明Kim1Ksp-KO小鼠的损伤较轻。此外,肾小管特异性敲除Kim1还抑制了Caspase3、8、9的活化,表明DR5下游信号通路被抑制。这些结果进一步证实了KIM1在AKI中通过促进DR5寡聚化和凋亡信号传导来加重肾脏损伤的作用。
YY1-KIM1-DR5轴的提出与验证
在本研究中,研究人员还利用转录因子预测数据库和蛋白质组学手段,揭示了肾损伤状态下KIM1的上游调控网络。他们发现,生理状态下,转录因子YY1维持在较高水平,对KIM1起到转录抑制作用,此时KIM1表达水平较低。然而,在肾损伤状态下,YY1下调,其对KIM1的转录抑制被部分解除,导致KIM1水平上调。
上调的KIM1随后与DR5结合,促进其寡聚化,并激活Caspase级联反应,诱导凋亡,从而加重AKI。这一发现首次提出了“YY1-KIM1-DR5”轴可能在AKI发生发展中扮演重要角色的观点。
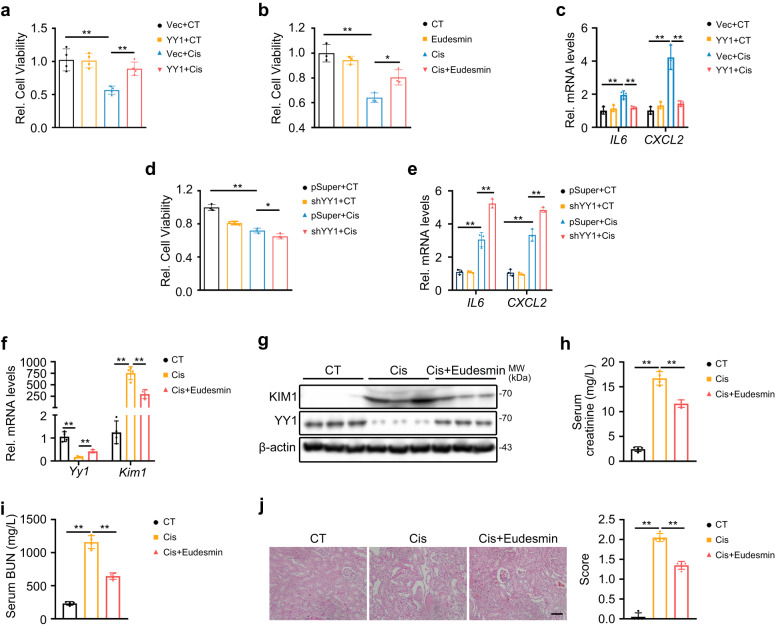
为了验证这一观点,研究人员进行了多项实验。他们发现,在AKI小鼠模型中,肾小管特异性敲除Kim1能够显著抑制DR5的寡聚化和凋亡信号传导,从而改善AKI。此外,他们还利用AlphaFold2构建了拮抗肽筛选体系,并获得了一种特异性阻滞KIM1-DR5互作的拮抗肽P2。在顺铂诱导的AKI小鼠模型中,P2尾静脉注射显著改善了肾功能和肾脏病理损伤,并抑制了Caspase3、8、9的激活和凋亡的发生。这些结果进一步证实了YY1-KIM1-DR5轴在AKI中的关键作用,并为AKI的治疗提供了新的靶点。
拮抗肽P2的设计与应用
针对KIM1与DR5的结合位点,研究人员利用AlphaFold2和Human KIM1-DR5 PPI进行了拮抗肽的筛选。通过细胞验证,他们获得了一种具有特异性阻滞KIM1-DR5互作的拮抗肽P2。
在顺铂诱导的AKI小鼠模型中,P2的尾静脉注射显著改善了肾功能和肾脏病理损伤。通过进一步的研究,研究人员发现P2能够抑制顺铂导致的损伤相关分子表达以及Caspase3、8、9的活化,并促进抗凋亡分子的表达。此外,5’(6) FAM标记的P2在顺铂诱导的AKI小鼠模型中与KIM1和DR5有良好的共定位,表明P2能够到达KIM1与DR5互作部位并发挥阻滞作用。这些结果充分证明了P2在AKI治疗中的潜在应用价值。
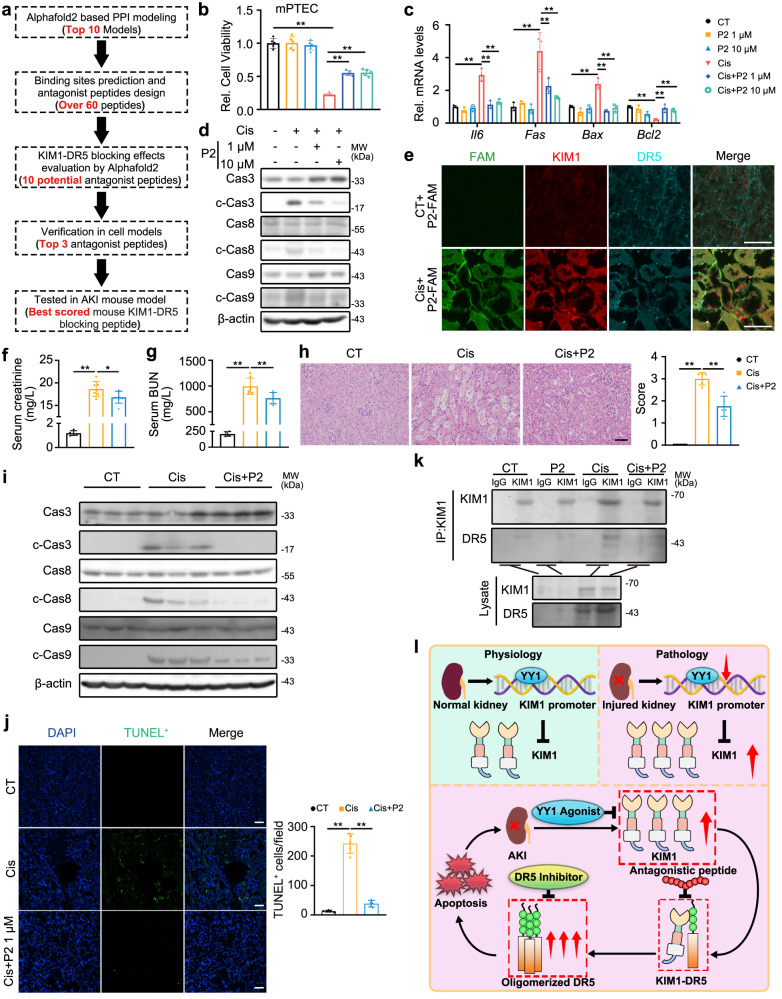
结论与展望
本研究首次揭示了YY1-KIM1-DR5轴在AKI发生发展中的关键作用,并为AKI的治疗提供了新的思路和靶点。通过构建肾小管特异性敲除Kim1的小鼠和特异性阻滞KIM1-DR5互作的拮抗肽P2,研究人员在动物水平上验证了YY1-KIM1-DR5轴的作用机制,并展示了P2在AKI治疗中的潜在应用价值。
然而,尽管本研究取得了重要的进展,但仍有许多问题有待进一步探讨。例如,YY1如何调控KIM1的转录?KIM1与DR5的结合是否还受到其他分子的调控?P2在人体内的安全性和有效性如何?这些问题都需要在未来的研究中进行深入探讨和验证。
| 名称 | 货号 | 规格 |
| YY1 (D5D9Z) Rabbit mAb | 46395T | 20μl |
| F4/80 (D2S9R) XP ® Rabbit mAb | 70076S | 100ul |
| PARP (46D11) Rabbit mAb | 9532S | 100ul |
| DR5 (D-6) | sc-166624 | 200ug/ml |



































