上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|乳腺癌原位及淋巴结转移癌免疫微环境抑制的单细胞特征
223 人阅读发布时间:2025-04-16 10:55
引言
乳腺癌作为全球女性最常见的恶性肿瘤之一,其发生和发展过程中涉及复杂的生物学机制。淋巴结作为重要的外周免疫器官,往往是乳腺癌转移的前哨站。淋巴结转移癌的免疫微环境在癌细胞的生长、进一步远端转移以及对治疗的反应中扮演着至关重要的角色。然而,乳腺癌淋巴结转移癌与原位癌在免疫微环境上的差异一直未能得到清晰的揭示。
近日,本人有幸参与了北京大学医学部张宏权教授团队的一项重要研究,该团队与哈尔滨医科大学肿瘤医院乳腺外科的李志高教授等合作,在Nature Communications期刊上发表了一篇题为“Single cell profiling of primary and paired metastatic lymph node tumors in breast cancer patients”的研究论文。该研究通过单细胞RNA测序、T细胞表面受体测序以及空间转录组测序技术,系统地探讨了乳腺癌原位癌(PT)及淋巴结转移癌(LNMT)在免疫微环境方面的特征和差异,为理解乳腺癌的免疫逃逸机制以及开发新的免疫治疗策略提供了重要的见解。

研究方法
本研究共纳入了8例发生淋巴结转移的非三阴乳腺癌患者。研究团队在分别获取患者的原位癌组织及配对的淋巴结转移癌组织后,采用了多种高通量测序技术进行深入分析。
-
单细胞RNA测序:该技术允许研究人员在单个细胞水平上分析基因表达模式,从而揭示不同细胞类型及其功能状态。在本研究中,单细胞RNA测序被用于构建乳腺癌原位癌和淋巴结转移癌的免疫微环境单细胞图谱。
-
T细胞表面受体测序:T细胞在抗肿瘤免疫中起着核心作用,而T细胞表面受体(TCR)的多样性决定了T细胞识别抗原的能力。通过T细胞表面受体测序,研究团队分析了原位癌和淋巴结转移癌中T细胞的克隆性和活化状态。
-
空间转录组测序:该技术能够在组织原位上捕获基因表达信息,揭示基因表达的空间分布模式。本研究利用空间转录组测序技术,进一步验证了单细胞RNA测序的结果,并揭示了免疫微环境在肿瘤组织中的空间分布特征。
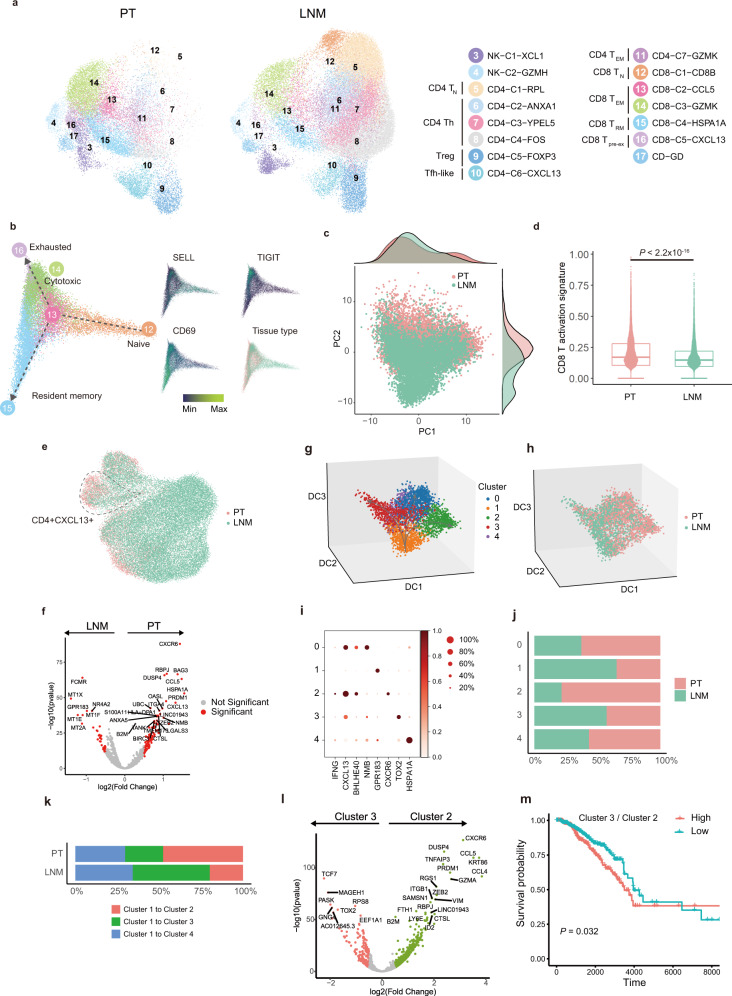
研究结果
通过对原位癌和淋巴结转移癌的深入分析,研究团队发现了两者之间在免疫微环境上的显著差异。
-
T细胞亚群的差异:与原位癌相比,淋巴结转移癌中幼稚型的T细胞比例更多。此外,CD8+和CD4+T细胞的活化和细胞毒性在淋巴结转移癌中受到抑制,其扩增和转变能力也更弱。特别是CD4+CXCL13+T细胞,在淋巴结转移中更倾向于分化为耗竭型,这进一步削弱了抗肿瘤免疫的效能。
-
髓系细胞的免疫抑制作用:研究团队进一步探索了髓系细胞在淋巴结转移癌中的免疫抑制作用。激活的LAMP3+树突状细胞虽然在淋巴结转移癌中的富集度高于原位癌,但它们高表达了更易募集Tregs(调节性T细胞)的趋化因子CCL17和CCL22,并且呈现出更低的T细胞启动和激活能力。这部分解释了淋巴结转移癌中T细胞活性受到抑制的原因。
-
癌相关成纤维细胞的作用:研究团队还鉴定出一种特异性表达PLA2G2A的癌相关成纤维细胞(CAF)。这种CAF细胞可以与免疫细胞相互作用,并在HER2+乳腺癌中富集,促进免疫浸润。这一发现揭示了CAF细胞在乳腺癌免疫微环境中的重要角色。
-
癌细胞抗原呈递分子的下调:在转移性淋巴结中的癌细胞中,多种重要的抗原呈递分子下调,而这种下调与CNV克隆无关。这表明转移至淋巴结的癌细胞可能在转录层面降低肿瘤相关抗原的暴露,从而发生免疫逃逸。这一发现解释了T细胞在有癌转移的淋巴结里更不易激活的原因。
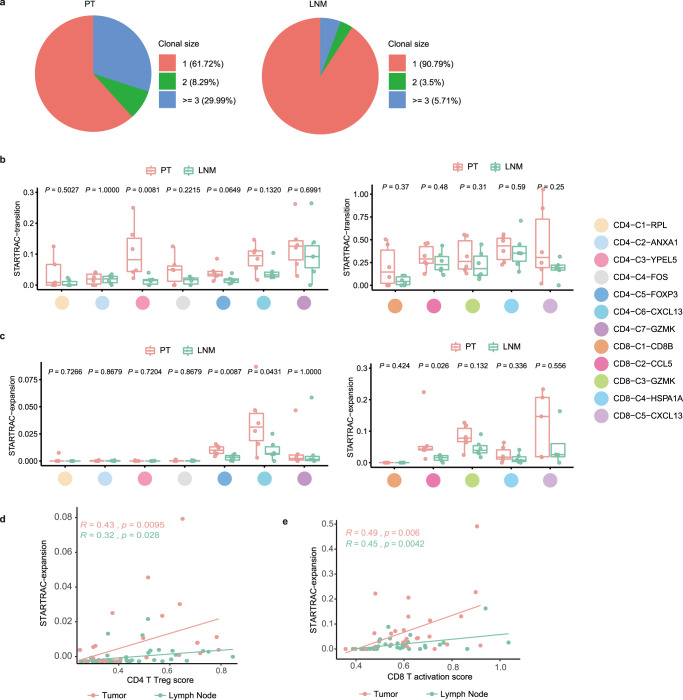
研究意义
本研究不仅构建了乳腺癌原位和淋巴结转移免疫微环境的单细胞图谱,还系统揭示出淋巴结转移癌的免疫微环境特征及其抑制机制。这些发现为理解乳腺癌的免疫逃逸机制提供了新的视角,并为靶向乳腺癌原位或淋巴结转移免疫微环境的治疗提供了新的思路。
-
免疫治疗策略的优化:通过揭示T细胞在淋巴结转移癌中的抑制状态和机制,研究团队为优化免疫治疗策略提供了重要依据。例如,针对T细胞耗竭和髓系细胞免疫抑制的靶点开发新的免疫药物,可能有助于提高免疫治疗的疗效。
-
肿瘤疫苗的开发:本研究发现转移至淋巴结的癌细胞在转录层面降低肿瘤相关抗原的暴露,这提示了开发新型肿瘤疫苗的可能性。通过诱导机体产生针对这些抗原的特异性免疫反应,可能有助于控制肿瘤的转移和复发。
-
个体化治疗的探索:随着单细胞测序技术的不断发展,未来有可能实现对每位患者的乳腺癌组织进行个体化的免疫微环境分析。这将有助于为患者制定更加精准和有效的治疗方案。
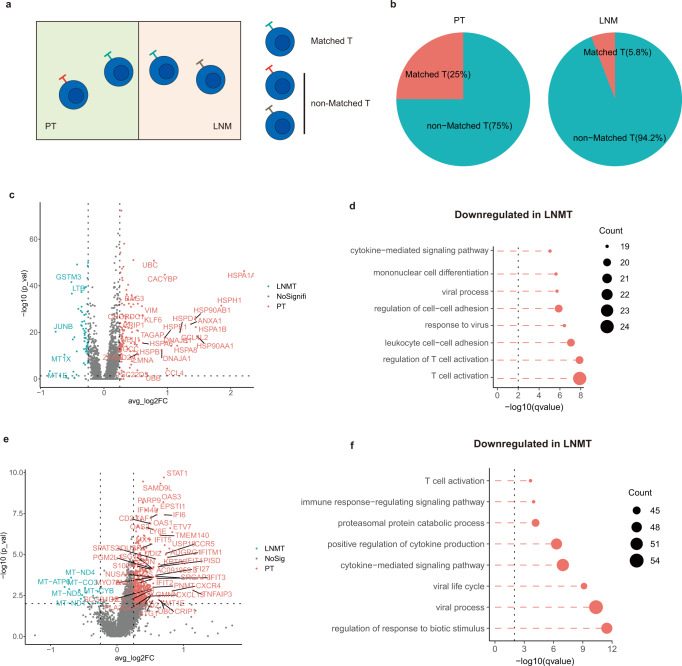
未来展望
尽管本研究取得了重要的进展,但仍有许多问题需要进一步探讨。例如,如何准确评估免疫治疗的疗效和预后?如何进一步优化免疫治疗策略以提高患者的生存率和生活质量?此外,随着单细胞测序技术的不断进步和成本的降低,未来有望将这项技术应用于更多的乳腺癌患者,为个体化治疗提供更加全面的信息支持。
在未来的研究中,我们还可以从以下几个方面进行拓展:
-
多组学数据的整合分析:结合基因组、转录组、蛋白质组和代谢组等多组学数据,可以更全面地揭示乳腺癌免疫微环境的复杂性和异质性。
-
动物模型的研究:通过建立乳腺癌动物模型,可以进一步验证本研究中发现的免疫抑制机制和免疫治疗策略的有效性。
-
临床转化的探索:与临床医生紧密合作,将本研究中的发现转化为临床实践,为患者提供更加精准和有效的治疗方案。
结语
本研究通过单细胞测序技术系统地揭示了乳腺癌原位癌和淋巴结转移癌在免疫微环境方面的特征和差异,为理解乳腺癌的免疫逃逸机制以及开发新的免疫治疗策略提供了重要的见解。未来,我们将继续深化这一领域的研究,为乳腺癌患者带来更加美好的治疗前景。同时,我们也期待与全球的科研人员合作,共同推动乳腺癌研究的进步和发展。
| 名称 | 货号 | 规格 |
| Rabbit anti-MRC1 Polyclonal Antibody | abs125294-50ul | 50ul |
| CD31 (PECAM-1) (D8V9E) XP ® Rabbit mAb | 77699T | 20ul |
| Purified NA/LE Hamster Anti-Mouse CD28(37.51) | 553294 | 500ug |
| Purified NA/LE Hamster Anti-Mouse CD3e(145-2C11) | 553057 | 500ug |



































