上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|aFGF调节星形胶质细胞外泌体治疗阿尔茨海默病的新机制
146 人阅读发布时间:2025-05-08 14:35
引言
阿尔茨海默病(Alzheimer's Disease, AD)是一种慢性、进行性发展的神经系统退行性疾病,主要影响老年人的认知功能,给患者的家庭和社会带来了沉重的负担。尽管医学界对AD的研究已经持续多年,但目前仍缺乏有效的治疗手段能够逆转其病理进程。因此,寻找新的治疗方法和策略显得尤为重要。近日,暨南大学生物医药研究院的黄亚东教授和张齐好教授团队在《Theranostics》杂志上发表了一项题为“Extracellular vesicles derived from astrocyte-treated with haFGF14-154 attenuate Alzheimer phenotype in AD mice”的研究论文,揭示了酸性成纤维细胞生长因子(Acidic fibroblast growth factor, aFGF)通过调节星形胶质细胞外泌体(Extracellular vesicles, EVs)中的关键分子,为阿尔茨海默病的治疗提供了新的思路。

研究背景
AD的病理特征主要包括β-淀粉样蛋白(Aβ)沉积形成的老年斑、神经纤维缠结以及神经元丢失等。这些病理变化导致大脑皮层和海马区的神经元功能受损,进而引发记忆障碍、认知功能下降等症状。近年来,越来越多的研究开始关注细胞外囊泡(EVs)在神经系统疾病中的作用。EVs作为细胞间通讯的重要介质,能够携带多种生物活性分子,如蛋白质、脂质和核酸等,参与调控细胞的稳态和功能。因此,EVs在疾病的发生、发展以及治疗中具有巨大的潜力。
研究目的
本研究旨在探讨aFGF如何通过调节星形胶质细胞EVs中的关键分子,影响AD的病理进程,并评估其作为潜在治疗手段的可行性。
研究方法
-
细胞培养与处理:研究团队首先建立了永生化的人主动脉瓣间质细胞(im-hVICs)模型,用于模拟主动脉瓣钙化的病理过程。同时,他们还培养了星形胶质细胞,并用aFGF进行处理,以观察其对EVs的影响。
-
EVs的分离与鉴定:通过差速离心法等方法,从处理后的星形胶质细胞培养基中分离出EVs,并进行表征和鉴定。
-
动物实验:利用小鼠建立AD模型,通过尾静脉注射或鼻腔滴注等方式给予EVs,观察其对AD病理进程的影响。
-
分子生物学实验:采用RNA测序、Western Blotting、免疫荧光等技术,检测EVs中关键分子的表达水平,以及其对神经元功能和Aβ沉积的影响。
研究结果
-
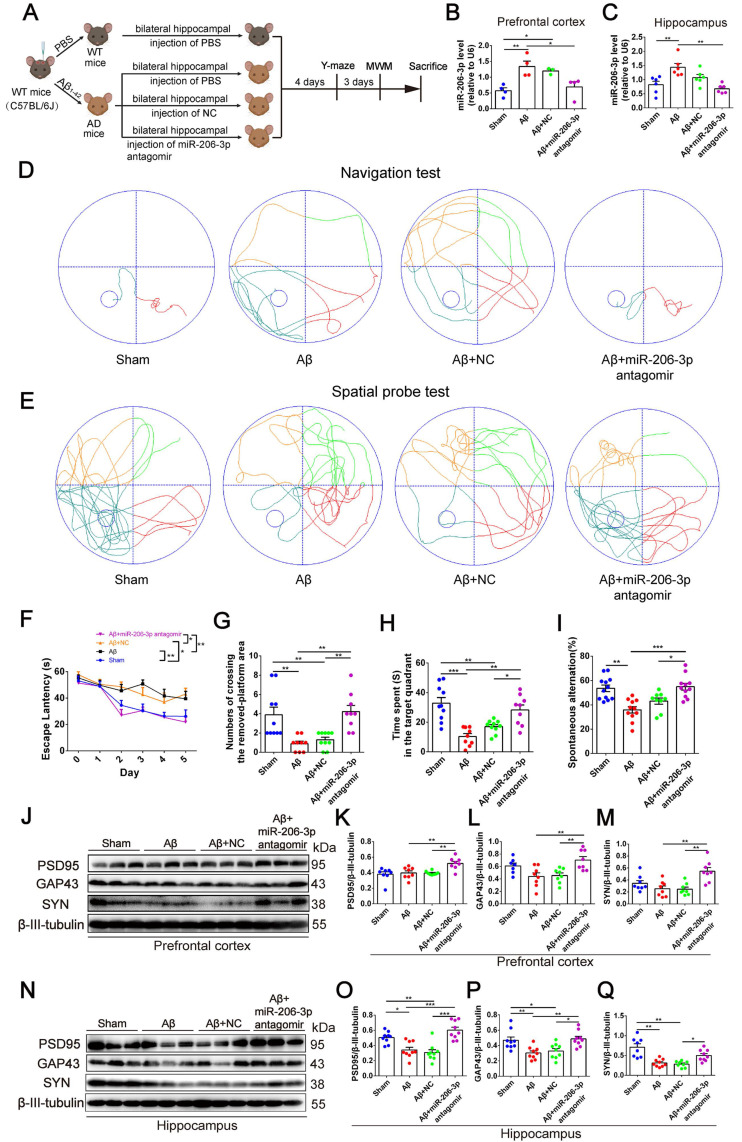
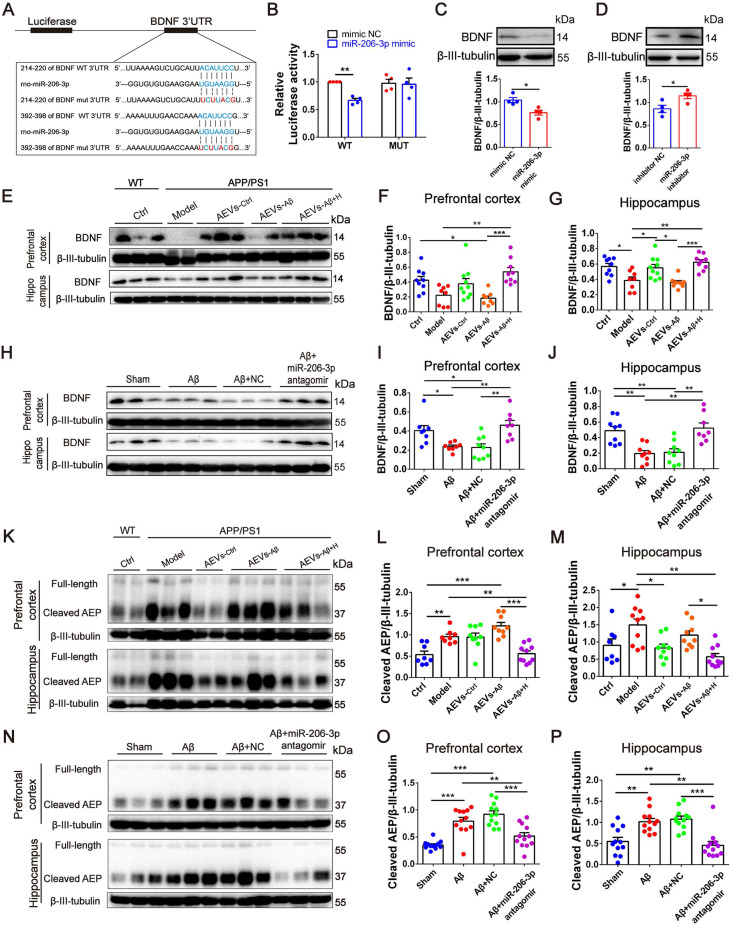
aFGF抑制星形胶质细胞EVs中关键分子的表达:研究发现,aFGF处理后的星形胶质细胞分泌的EVs中,关键调节分子miR-206-3p的表达水平显著降低。这一变化进一步影响了EVs对下游神经元的影响。
-
上调脑源性神经营养因子和突触相关蛋白的表达:通过分子生物学实验,研究团队发现,给予aFGF处理后的星形胶质细胞EVs能够显著上调脑源性神经营养因子(BDNF)和突触相关蛋白的表达水平。这些蛋白在神经元的生长、发育和修复过程中发挥着重要作用。
-
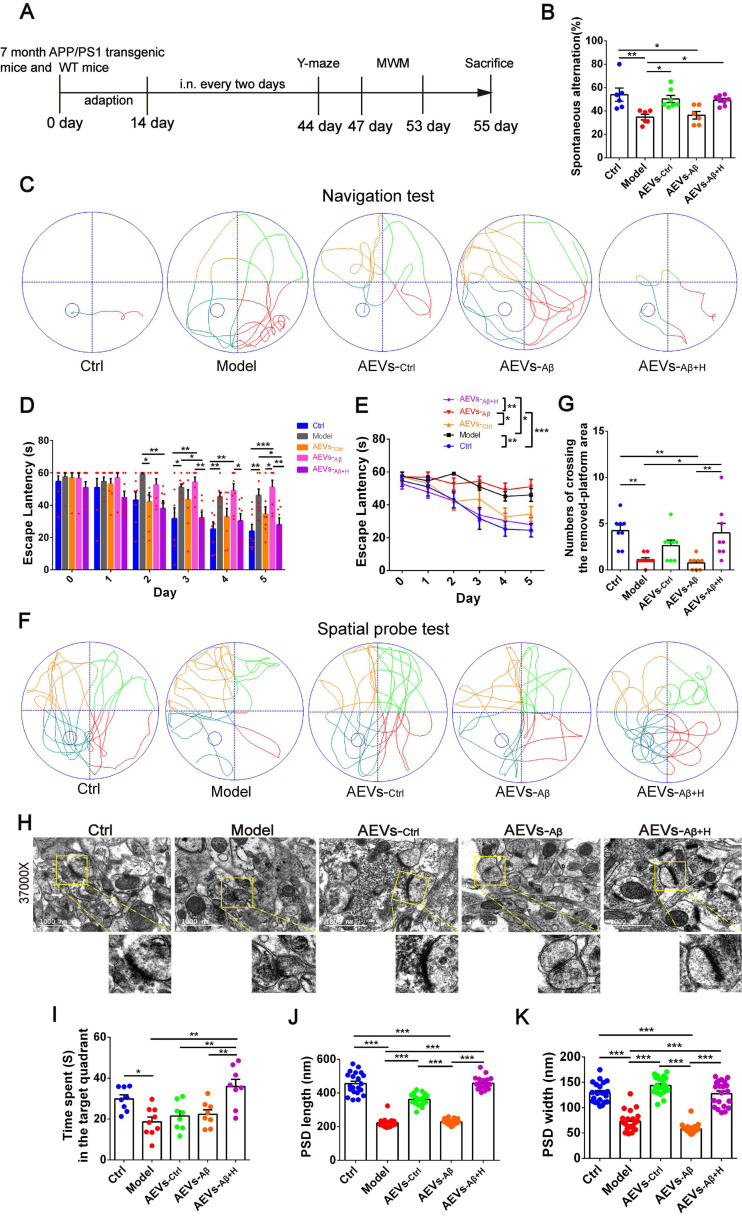
减少Aβ沉积并促进神经元修复:在AD小鼠模型中,给予aFGF处理后的星形胶质细胞EVs能够显著减少脑内Aβ的沉积,同时促进神经元的修复和再生。这一结果通过免疫荧光和组织病理学实验得到了验证。
-
改善学习记忆能力:行为学实验表明,给予aFGF处理后的星形胶质细胞EVs能够显著改善AD小鼠的学习记忆能力。这一结果进一步证实了aFGF在AD治疗中的潜在价值。
-
miR-206-3p可能成为AD早期诊断的候选生物标记物:研究团队还进一步检测了临床AD患者血浆中miR-206-3p的表达水平。结果发现,AD患者血浆中miR-206-3p的水平显著高于年龄匹配的正常受试者。同时,相比于帕金森病和精神分裂症患者,AD患者血浆中miR-206-3p的表达更具有特异性。因此,miR-206-3p有望成为AD早期诊断的候选生物标记物。
研究意义
-
为AD治疗提供新思路:本研究揭示了aFGF通过调节星形胶质细胞EVs中的关键分子,影响AD病理进程的新机制。这一发现为AD的治疗提供了新的思路和方法。
-
推动EVs在神经系统疾病治疗中的应用:本研究进一步证实了EVs在神经系统疾病治疗中的潜力。通过调节EVs中的关键分子,可以实现对神经元功能的调控和修复,为神经系统疾病的治疗提供新的策略。
-
促进神经退行性疾病的研究:本研究不仅为AD的治疗提供了新的思路,还为其他神经退行性疾病的研究提供了参考和借鉴。通过深入研究EVs在神经系统疾病中的作用机制,有望为更多神经系统疾病的治疗提供新的突破点。
展望
尽管本研究取得了令人瞩目的成果,但仍存在一些问题和挑战需要解决。例如,aFGF调节星形胶质细胞EVs的具体分子机制仍需进一步阐明;EVs在体内的稳定性和靶向性仍需优化;以及aFGF治疗AD的安全性和有效性还需在更大规模的临床试验中进行验证等。未来,研究团队将继续深入探索aFGF和EVs在AD治疗中的作用机制,并努力推动相关研究成果的临床转化和应用。
结论
本研究揭示了aFGF通过调节星形胶质细胞EVs中的关键分子,影响AD病理进程的新机制。通过给予aFGF处理后的星形胶质细胞EVs,能够显著上调BDNF和突触相关蛋白的表达水平,减少Aβ沉积并促进神经元修复,从而显著改善AD小鼠的学习记忆能力。这一发现为AD的治疗提供了新的思路和方法,有望为更多神经系统疾病的治疗提供新的突破点。同时,本研究也进一步证实了EVs在神经系统疾病治疗中的潜力和价值,为未来的研究提供了更多的可能性和方向。
随着对aFGF和EVs在AD治疗中作用机制的深入研究,我们期待未来能够开发出更加有效、安全的治疗手段,为AD患者带来福音。同时,我们也期待更多的科研团队能够加入到这一领域的研究中来,共同推动神经退行性疾病的治疗和研究取得更大的进展和突破。
| 名称 | 货号 | 规格 |
| Rabbit anti-Calnexin Polyclonal Antibody | abs131462-50ug | 50ug |
| Legumain (D6S4H) Rabbit mAb | 93627T | 20μl |
| Legumain (D6S4H) Rabbit mAb | 93627S | 100ul |
| Goat anti-Mouse IgG (H+L) Cross-Adsorbed Secondary Antibody, Alexa Fluor 594 | A11005 | 1MG |