上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|副干酪乳酪杆菌sh2020诱导抗肿瘤免疫与增强抗PD-1治疗效果的研究解析
154 人阅读发布时间:2025-05-13 11:59
引言
随着现代生物技术的飞速发展,肠道微生物群在人体健康与疾病中的作用逐渐受到科学家们的重视。特别是在癌症治疗领域,肠道微生物的调节作用被视为潜在的突破性方向。近期,一篇题为《Lacticaseibacillus paracasei sh2020 induced antitumor immunity and synergized with anti-programmed cell death 1 to reduce tumor burden in mice》的研究论文在知名期刊上发表,揭示了副干酪乳酪杆菌sh2020(Lacticaseibacillus paracasei sh2020)在诱导抗肿瘤免疫及与抗PD-1协同减少小鼠肿瘤负荷方面的独特作用。本文将对该研究进行详细解析和描述,以期为相关领域的研究人员和临床工作者提供有价值的参考。

文献背景
肠道微生物群作为人体内一个复杂的生态系统,与宿主之间存在着密切且复杂的相互作用。近年来,越来越多的研究表明,肠道微生物不仅参与营养物质的吸收和代谢,还在调节宿主免疫应答、预防疾病发生和发展等方面发挥着重要作用。特别是在癌症领域,肠道微生物群的调节作用被视为潜在的治疗靶点。
抗PD-1治疗作为目前癌症免疫疗法的重要组成部分,通过阻断PD-1受体与其配体PD-L1的结合,恢复T细胞的抗肿瘤活性,已在多种癌症治疗中显示出显著疗效。然而,抗PD-1治疗的效果在不同患者之间存在较大差异,这可能与肠道微生物群的组成和功能状态密切相关。
研究目的
本研究旨在探究副干酪乳酪杆菌sh2020对小鼠肠道微生物群的调节作用,以及其与抗PD-1协同减少肿瘤负荷的潜在机制。通过深入分析该菌株在诱导抗肿瘤免疫方面的作用,为癌症免疫治疗提供新的思路和方法。
材料与方法
- 实验动物:选用健康小鼠作为实验对象,通过移植不同来源的肠道微生物群(健康个体和结直肠癌患者)构建实验模型。
- 菌株筛选与鉴定:通过16S rRNA基因测序技术,从对抗PD-1反应良好的小鼠肠道中筛选出具有显著抗肿瘤免疫作用的副干酪乳酪杆菌sh2020。
- 抗肿瘤实验:将副干酪乳酪杆菌sh2020单独或与抗PD-1抗体联合应用于小鼠结直肠癌模型中,观察其抗肿瘤效果。
- 机制探究:通过检测肿瘤组织内CXCL10趋化因子的表达、CD8+ T细胞的招募和活化情况,以及肠道微生物群的组成变化,探讨副干酪乳酪杆菌sh2020诱导抗肿瘤免疫的机制。
结果与分析
- 副干酪乳酪杆菌sh2020的筛选与鉴定:通过16S rRNA基因测序技术,研究人员从对抗PD-1反应良好的小鼠肠道中成功筛选出副干酪乳酪杆菌sh2020。该菌株在体外实验中表现出良好的生长性能和稳定性,为后续实验提供了可靠的材料。
- 抗肿瘤效果评估:将副干酪乳酪杆菌sh2020单独或与抗PD-1抗体联合应用于小鼠结直肠癌模型中,结果显示该菌株单独使用时即可显著抑制肿瘤生长,与抗PD-1抗体联合使用时则表现出更强的抗肿瘤效果。这一结果提示副干酪乳酪杆菌sh2020可能与抗PD-1具有协同作用。
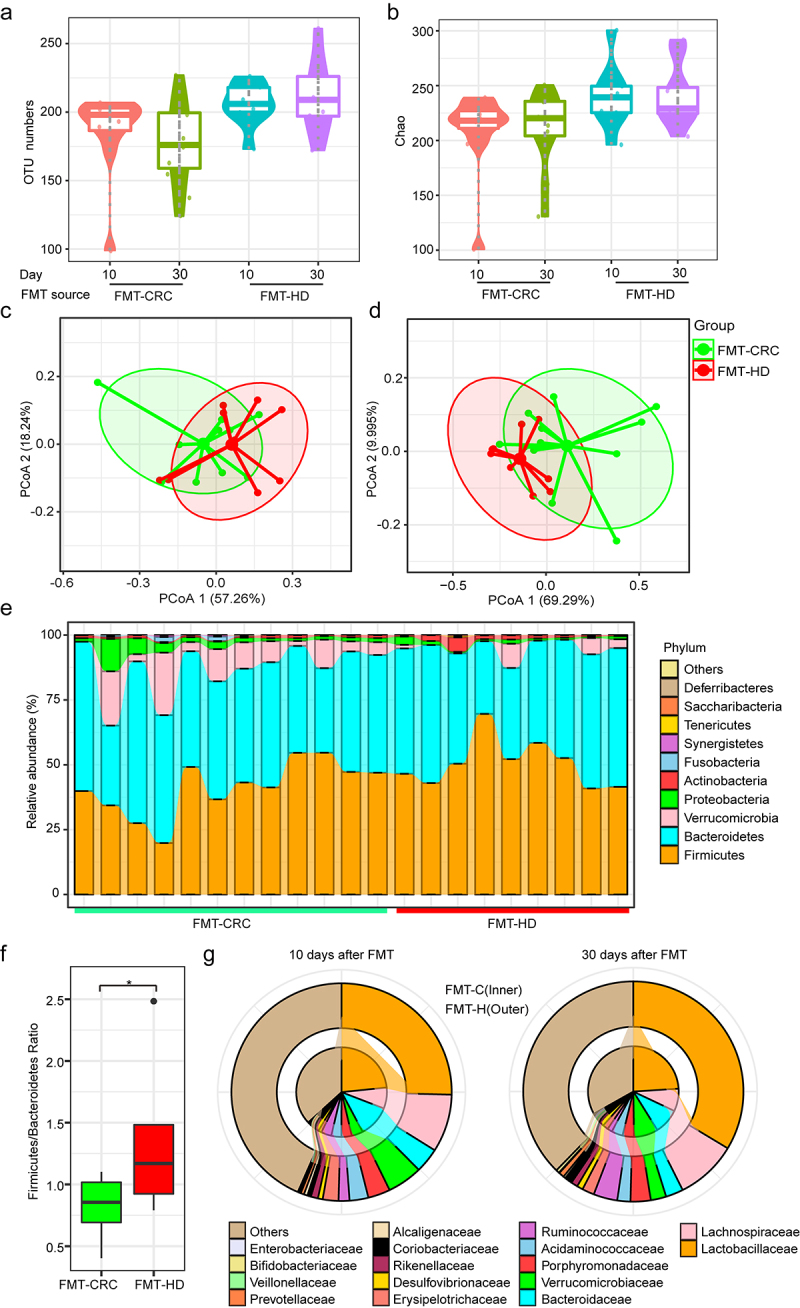
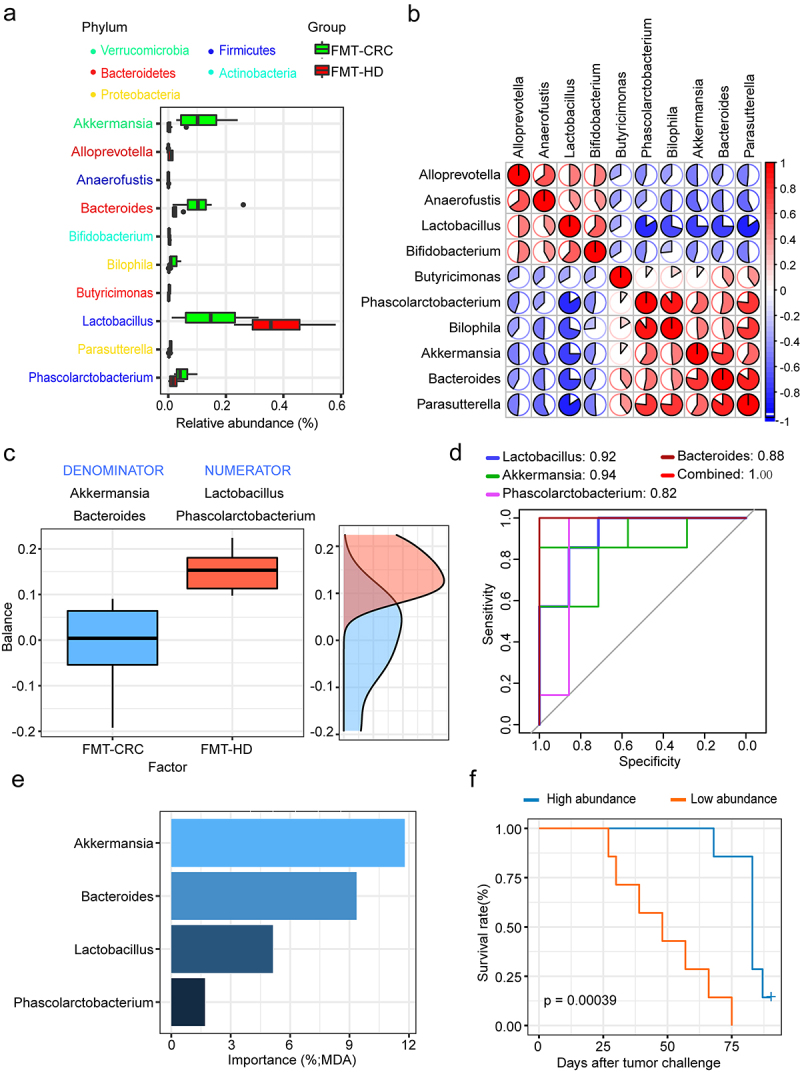
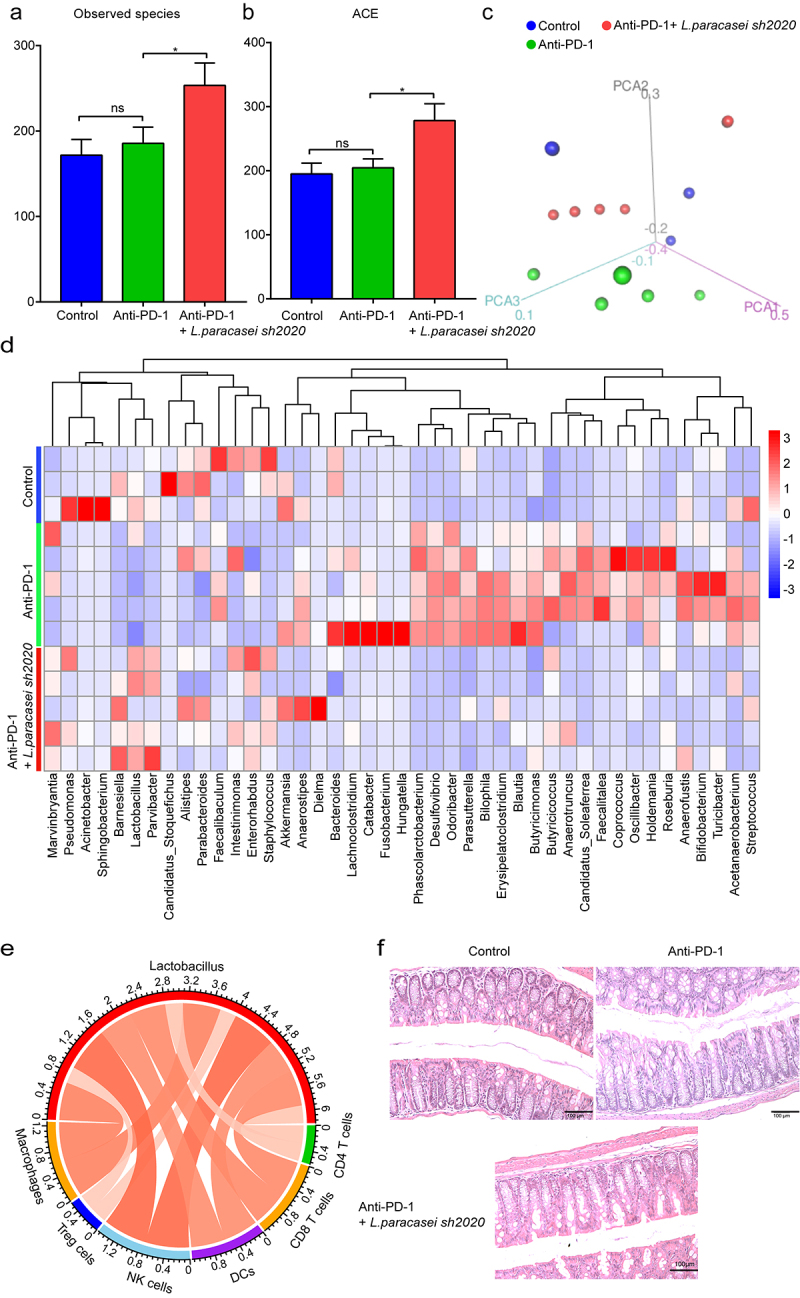
- 机制探究:进一步的研究发现,副干酪乳酪杆菌sh2020能够诱导肿瘤组织内CXCL10趋化因子的表达上调,进而促进CD8+ T细胞的招募和活化。同时,该菌株还能够调节肠道微生物群的组成,增强其抗肿瘤功能和肠道屏障功能。这些结果揭示了副干酪乳酪杆菌sh2020诱导抗肿瘤免疫的潜在机制。
- 安全性评估:在实验中,研究人员还观察了副干酪乳酪杆菌sh2020对小鼠的毒性作用。结果显示,该菌株在小鼠体内未引起明显的毒性反应,表明其具有良好的安全性。
讨论
本研究首次揭示了副干酪乳酪杆菌sh2020在诱导抗肿瘤免疫及与抗PD-1协同减少小鼠肿瘤负荷方面的独特作用。通过深入分析该菌株的作用机制,我们发现其能够调节肠道微生物群的组成和功能状态,进而诱导肿瘤组织内CXCL10趋化因子的表达上调和CD8+ T细胞的招募及活化。这些发现不仅为癌症免疫治疗提供了新的思路和方法,也为后续的临床应用提供了有力的支持。
此外,本研究还提示我们,在癌症免疫治疗中应充分考虑肠道微生物群的调节作用。通过优化肠道微生物群的组成和功能状态,可能能够进一步提高免疫治疗的疗效和安全性。因此,未来的研究应进一步深入探究肠道微生物群与免疫治疗之间的相互作用关系,为癌症患者提供更加精准和有效的治疗方案。
结论
本研究通过构建小鼠结直肠癌模型,成功筛选出具有显著抗肿瘤免疫作用的副干酪乳酪杆菌sh2020。该菌株能够诱导肿瘤组织内CXCL10趋化因子的表达上调和CD8+ T细胞的招募及活化,进而与抗PD-1抗体协同减少小鼠肿瘤负荷。同时,该菌株还具有良好的安全性和稳定性。这些发现为癌症免疫治疗提供了新的思路和方法,有望为癌症患者提供更加精准和有效的治疗方案。
未来研究方向
尽管本研究取得了初步的成果,但仍有许多问题有待进一步探讨。例如,副干酪乳酪杆菌sh2020在人体内的作用机制是否与小鼠一致?该菌株是否适用于其他类型的癌症?如何优化肠道微生物群的组成和功能状态以进一步提高免疫治疗的疗效?这些问题将是未来研究的重要方向。
总之,本研究为癌症免疫治疗提供了新的思路和方法,有望为癌症患者带来福音。我们期待在未来的研究中能够进一步深入探究肠道微生物群与免疫治疗之间的相互作用关系,为癌症治疗领域的发展做出更大的贡献。
| 名称 | 货号 | 规格 |
| Rabbit anti-CXCL10 Polyclonal Antibody | abs135937-100ug | 100ug |
| mIP-10 MAb (Cl 13401 (25 ug) | MAB466-SP | 25ug |
| Rabbit anti-CXCL10 Polyclonal Antibody | abs135937-50ug | 50ug |
| InVivoMAb anti-mouse CD8α | BE0117-5MG | 5MG |