上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2

斯达特
抗体/ELISA 试剂盒/试剂
已认证品牌介绍

Absin
生物化学/抗体
已认证品牌介绍

LabEx
技术服务
已认证品牌介绍

Cytiva
实验室仪器 / 设备/试剂/耗材/细胞库 / 细胞培养
已认证品牌介绍

Novus
抗体/试剂
已认证品牌介绍

Sigma-Aldrich
实验室仪器 / 设备/试剂/耗材
已认证品牌介绍

Thermo Fisher
试剂/实验室仪器 / 设备/耗材
已认证品牌介绍

Horizon Discovery
细胞库 / 细胞培养/技术服务/动物模型
已认证品牌介绍

Enzo
实验室仪器 / 设备/试剂
已认证品牌介绍

BiosPacific
抗体
已认证品牌介绍

Cayman
抗体/试剂
已认证品牌介绍

Bio X Cell
抗体/试剂
已认证品牌介绍

R&D Systems
试剂
已认证品牌介绍

Tocris bioscience
试剂
已认证品牌介绍

Innova Biosciences
抗体
已认证品牌介绍

Cell Signaling Technology
抗体
已认证品牌介绍

Biovision
试剂
已认证品牌介绍

Fitzgerald
试剂
已认证品牌介绍

LifeSpan BioSciences
抗体/试剂
已认证品牌介绍

AnaSpec
试剂
已认证品牌介绍

Sengenics
试剂/技术服务
已认证品牌介绍

Cytoskeleton
蛋白质/抗原/多肽/试剂
已认证品牌介绍

Synaptic Systems
试剂
已认证品牌介绍

USBiological
抗体/试剂
已认证品牌介绍

Agrisera
抗体
已认证品牌介绍

Meridian
抗体/试剂
已认证品牌介绍

Miltenyi Biotec
实验室仪器 / 设备/试剂
已认证品牌介绍

Alomone Labs
试剂
已认证品牌介绍

斯达特
抗体/ELISA 试剂盒/试剂
已认证品牌介绍

Absin
生物化学/抗体
已认证品牌介绍

LabEx
技术服务
已认证品牌介绍

Cytiva
实验室仪器 / 设备/试剂/耗材/细胞库 / 细胞培养
已认证品牌介绍
- 上海优宁维生物科技股份有限公司
- >技术资料
- >
文献解析 | 克隆池策略加速单克隆抗体药物临床前开发
技术资料/正文
文献解析 | 克隆池策略加速单克隆抗体药物临床前开发
183 人阅读发布时间:2025-02-10 17:20
一篇BMS发布的文献,其核心议题聚焦于临床前研究阶段的一个创新策略:采用克隆池技术加速毒理批次的制备流程,随后精选出最佳克隆进行GMP合规的临床级材料及临床前试验品的生产,以此策略显著加速了药物开发周期。

核心理念阐述
在标准临床前研究路径中,为保持与后续临床用材料的一致性,毒理批次常源自先导克隆。然而,BMS创新性地引入了“克隆池”概念,旨在缩短这一关键阶段的耗时,实验表明,该策略可促使临床前早期开发提速约四个月。BMS依托其专属的细胞系库、培养基配方及培养技术体系,成功验证了此策略的有效性。
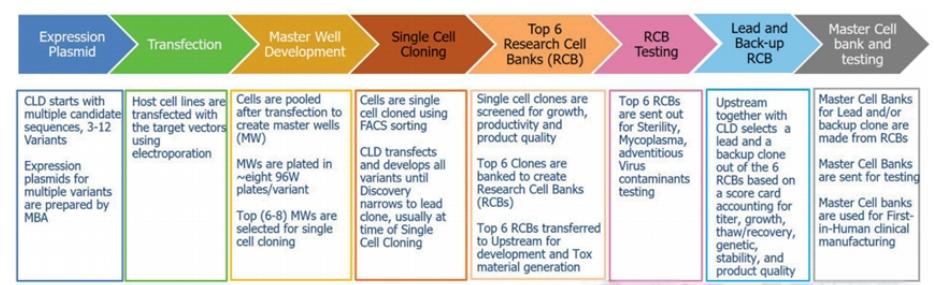
研究设计概览
研究的核心步骤包括:
- 整合六个克隆构建毒理批生产所需的克隆池;
- 为每个克隆单独构建研究细胞库(RCB);
- 通过筛选RCB,甄选出最优克隆作为临床材料生产的基石;
- 选取六种单抗(Mab-A至Mab-F)作为实验对象,全面评估上述策略在工艺性能、产品表达效率及质量属性上的表现。
工艺性能与表达效率分析
实验结果揭示了Tox批次与FIH(前导克隆临床材料)批次间细胞活力的细微差异,大多数FIH批次展现出高于60%的收获活力,且工艺杂质水平评估进一步确认了这些差异对产品质量影响甚微。
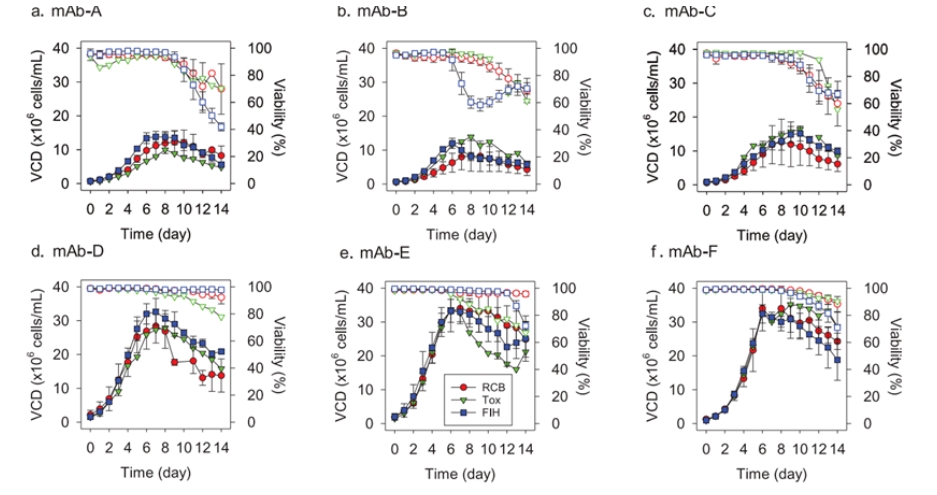
工艺性能
在表达滴度方面,克隆池Tox批次的滴度与单一克隆平均滴度相近(特别是对于mAb-A至-F中的多数),而针对特定单抗(如mAb-D),则通过短期稳定性测试确保了所选克隆的稳定性和生产潜力。
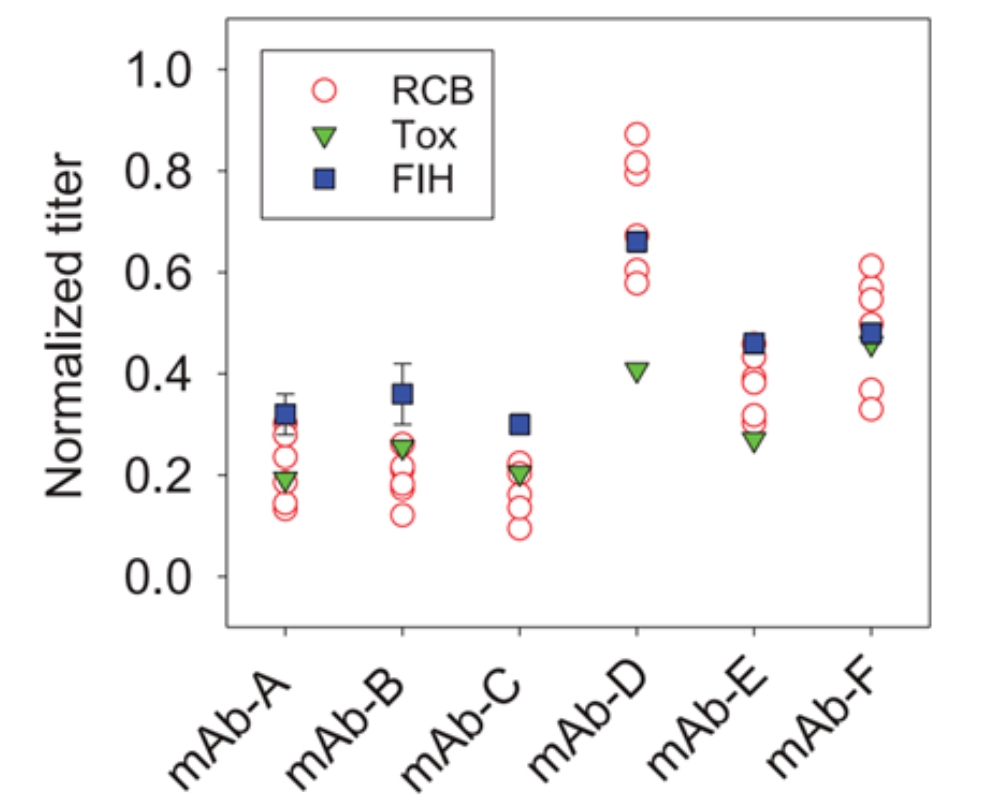
表达滴度
产品质量综合评估
电荷变体、糖型分布、纯度及工艺相关杂质等多维度分析显示,无论是来自RCB、Tox批次还是FIH批次的材料,均展现出高度一致性和可比性。具体而言,电荷变体分布的微小差异在可接受范围内,糖型水平符合行业标准,纯度及效价测试结果也相互印证,表明该策略在不同生产阶段均能保持产品的关键质量属性。
总结与展望
本文献深入探讨了利用多克隆池策略优化毒理批次生产的可行性与优势,通过详尽的数据支持了其在保证细胞培养性能及产品质量方面的可靠性。采用此策略不仅拓宽了克隆选择范围,还显著降低了因单一克隆依赖可能带来的质量风险。因此,克隆池技术在加速单克隆抗体类药物早期开发进程中展现出巨大潜力,值得在更广泛的研发实践中推广应用。
| 名称 | 货号 | 规格 |
| Mouse Anti-rabbit IgG (Conformation Specific) (L27A9) mAb | 3678S | 100ul |
| Mouse Anti-rabbit IgG (Light-Chain Specific) (D4W3E) mAb | 45262S | 100ul |
6526739279089788881[1].jpg
在线沟通
我的询价







