上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|IL-2的酸性适应性增强,免疫效能显著提升
285 人阅读发布时间:2025-02-17 14:16
IL-2
免疫治疗作为肿瘤临床治疗的新兴领域,已经紧随手术、放疗和化疗之后,成为第四大治疗手段,并且在多模式联合治疗中占据了举足轻重的地位。在这一领域中,高剂量的白细胞介素-2(IL-2)疗法已获准应用于转移性肾细胞癌和转移性黑色素瘤的治疗。然而,IL-2对调节性T细胞(Treg)和效应T细胞的功能特性具有双重作用,这在一定程度上限制了其在抗肿瘤免疫中的疗效。具体来说,IL-2既能激活具有抗肿瘤活性的效应T细胞,同时也能促进具有免疫抑制功能的Treg细胞的增殖和活化,从而削弱了其抗肿瘤效果。
此外,高剂量的IL-2疗法还伴随着一系列严重的毒性反应,包括血管漏综合征(VLS)、肺水肿、低血压和心脏毒性等,这些副作用极大地限制了其在临床上的广泛应用。近期,由剑桥大学的Rahul Roychoudhuri、邓迪大学的Ignacio Moraga以及里尔大学的Suman Mitra共同领导的研究团队,在权威期刊《Science Immunology》上发表了一项针对高剂量IL-2疗法的改进研究。他们发现,肿瘤微环境的酸性特征会严重破坏IL-2的信号传导和生物活性,这是导致其疗效有限的关键因素。

为了克服这一难题,研究团队开发了一种IL-2的工程化突变体蛋白,命名为Switch-2。这种突变体蛋白在酸性环境中能够保持高活性,而在正常生理环境下则活性较低。这种特性使得Switch-2能够更精准地靶向肿瘤微环境,从而在减少全身毒性的同时,展现出更强大的抗肿瘤效果。这一发现为IL-2疗法的优化提供了新的思路,有望在未来推动肿瘤免疫治疗的发展。
肿瘤免疫抑制的微环境,以其乏氧、酸性的特性,并充斥着大量的炎性细胞和细胞因子,成为了影响免疫治疗疗效的关键因素之一。这种特殊的环境条件不仅直接削弱了CD8+T细胞的代谢活性,还促进了包括Treg在内的多种免疫抑制细胞的功能,进而诱导了免疫系统的全面抑制。
鉴于酸性肿瘤微环境(TME)对T细胞功能的显著影响,以及IL-2作为T细胞的重要激动剂的角色,肿瘤的酸性微环境是否也会对IL-2的疗效产生负面影响呢?
为了深入探究这一问题,研究人员巧妙地设计了实验,利用盐酸和乳酸来模拟肿瘤内部的酸性环境,进而观察在这种条件下IL-2对CD8+T细胞的激活作用。实验结果显示,相较于正常环境,IL-2在酸性条件下的活性明显减弱。进一步的分析指出,这种活性的降低源于酸性条件下IL-2与其受体IL-2Rα的结合能力显著下降。这一发现不仅揭示了酸性肿瘤微环境对IL-2疗效的潜在抑制作用,也为后续优化免疫治疗策略提供了重要的理论依据。通过改善肿瘤微环境的酸性特征,或开发能够在酸性环境中保持高活性的IL-2变体,或许能够显著提升免疫治疗的疗效,为肿瘤患者带来新的治疗希望。
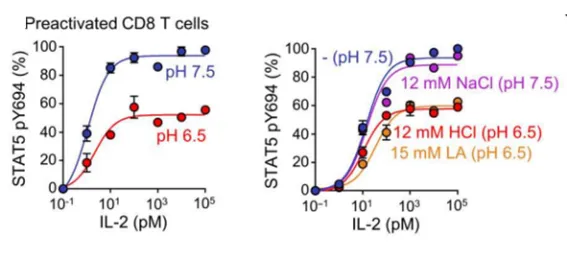
尽管先前的研究已在体外实验中观察到酸性肿瘤微环境(TME)对白细胞介素-2(IL-2)疗效的削弱作用,但这种影响在体内是否同样存在仍是一个未解之谜。
为了深入探究这一问题,研究人员精心设计了体内实验。他们首先构建了携带B16黑素瘤细胞的荷瘤小鼠模型,随后采用了两种策略来干预肿瘤微环境的酸性特征:一是通过碳酸氢钠治疗来消耗TME中已生成的乳酸,并辅助IL-2治疗;二是通过接种乳酸脱氢酶A/B(LDHA/B)双敲除的肿瘤细胞来减少TME中乳酸的产生,并同样给予IL-2治疗。
实验结果显示,无论是通过碳酸氢钠消耗乳酸还是通过接种LDHA/B双敲除细胞减少乳酸产生,都能有效减弱TME的酸性特征。这一改变不仅促进了IL-2对肿瘤浸润CD8+T细胞的激活,增强了其效应功能,还显著降低了T细胞的耗竭程度。最终,这些干预措施显著增强了IL-2的抗肿瘤效力,并有效延长了荷瘤小鼠的生存期。
这一发现不仅证实了酸性肿瘤微环境在体内同样会削弱IL-2的疗效,而且为通过改善肿瘤微环境来优化免疫治疗策略提供了有力的实验证据。未来,基于这一发现,我们可以探索更多针对肿瘤微环境干预的治疗手段,以期进一步提升免疫治疗的疗效,造福更多肿瘤患者。
鉴于IL-2在酸性pH条件下难以发挥有效的抗肿瘤作用,研究人员萌生了一个创新性的想法:是否有可能设计并制备出一个在酸性pH下仍能保持高活性的IL-2突变体?
为了将这一想法付诸实践,研究人员采用了定向进化策略来筛选IL-2的突变体。经过一系列精心设计的筛选过程,他们成功获得了一株名为Switch-2的IL-2突变体。这一突变体在低pH条件下与IL-2受体α亚基(IL-2Rα)的结合能力显著增强,而在中性pH下的结合能力则相对较低。
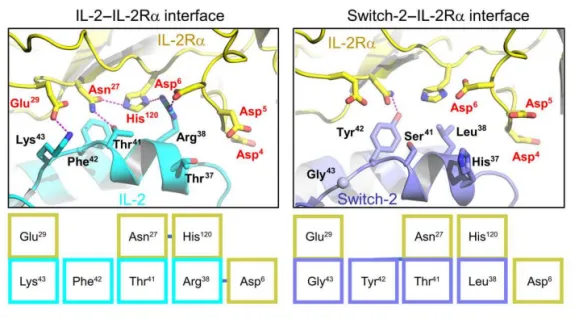
为了深入探究Switch-2在酸性条件下保持高活性的结构基础,研究人员进一步模拟了pH 6和pH 7两种情况下IL-2/IL-2Rα复合物和Switch-2/IL-2Rα复合物的结构稳定性。通过对比分析,他们发现,在酸性条件下,IL-2Rα的120位组氨酸会发生质子化,这一变化损害了其与IL-2的38位精氨酸之间的结合。而Switch-2则在结合位点附近存在一个独特的37位组氨酸,这个组氨酸在酸性条件下会发生质子化,从而取代了IL-2Rα的120位组氨酸的质子化作用,进而加强了Switch-2/IL-2Rα复合物在酸性条件下的稳定性。
这一发现不仅揭示了Switch-2在酸性条件下保持高活性的分子机制,也为未来设计和开发针对酸性肿瘤微环境的免疫治疗药物提供了新的思路。通过进一步优化和改造Switch-2等类似的突变体,我们有望开发出更加高效、低毒的免疫治疗方法,为肿瘤患者带来更好的治疗效果和生存质量。
在进一步验证IL-2与Switch-2的功能差异时,研究人员采用了预活化的CD8+T细胞,并在pH 6.5和pH 7.5的条件下分别用两者进行刺激。实验结果显示,Switch-2在酸性条件下展现出了更强的激活T细胞STAT5信号通路的能力,这直接证明了Switch-2在酸性环境中对T细胞的激活效果优于IL-2。
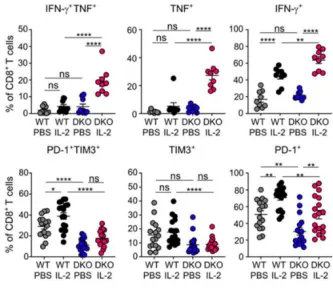
此外,研究人员还深入探究了在不同pH条件下,IL-2与Switch-2对CD8+T细胞细胞因子分泌的影响。他们发现,在中性条件下,IL-2能够刺激T细胞分泌一定数量的细胞因子,如IFN-γ等,这些细胞因子与T细胞的效应功能密切相关。然而,在酸性条件下,IL-2的这种刺激作用明显减弱,而Switch-2则能够保持对T细胞的强刺激作用,促使其大量分泌效应细胞因子。
为了从基因层面进一步验证这一发现,研究人员采用了基因集富集分析的方法。他们发现,在酸性条件下(pH 6.5),IL-2刺激CD8+T细胞激活和效应功能的基因表达能力显著下降,而Switch-2则呈现出镜像般的增强作用,这再次证实了Switch-2在酸性环境中对T细胞的优越激活效果。
尽管体外实验已经充分展示了Switch-2的优势,但其在体内的抗肿瘤疗效仍需进一步验证。为此,研究人员构建了MC38(小鼠结直肠癌)、4T1(小鼠三阴乳腺癌)和B16-SIY三种肿瘤模型,并分别用IL-2和Switch-2进行治疗。结果显示,Switch-2在这三种肿瘤模型中均展现出了显著的抗肿瘤效果,不仅有效抑制了肿瘤的生长,还显著延长了小鼠的生存期。更为令人振奋的是,在对Switch-2治愈的MC38荷瘤小鼠进行MC38再接种的实验中,研究人员发现这些小鼠完全免疫了MC38的生长。这表明Switch-2不仅能够抑制肿瘤的生长,还能够诱导长效的抗肿瘤免疫记忆,为未来的肿瘤免疫治疗提供了新的可能。
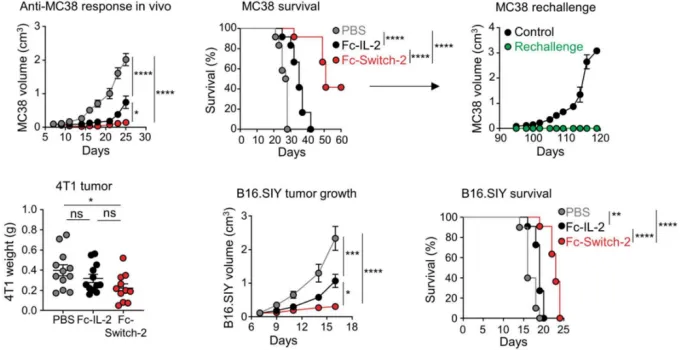
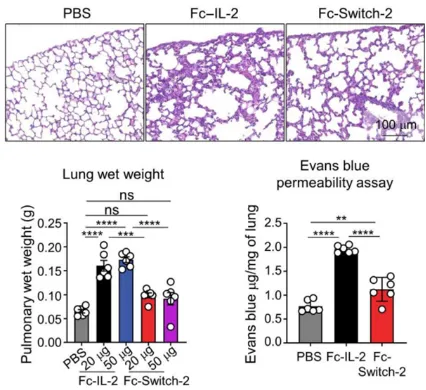
在探究Switch-2能否克服IL-2疗法全身毒性高的关键问题上,研究人员采取了高剂量给药的方式对小鼠进行实验。他们发现,给予高剂量的IL-2会导致小鼠出现明显的肺水肿症状,这是IL-2疗法全身毒性高的一个典型表现。然而,当给予相同高剂量的Switch-2时,小鼠所表现出的肺水肿和血管通透性症状却显著减轻。
这一发现不仅进一步证实了Switch-2在体内具有偏好酸性pH组织环境激活的特性,还揭示了其相较于IL-2在降低全身毒性方面的显著优势。由于肿瘤微环境通常呈酸性,Switch-2能够更精准地靶向肿瘤部位,激活肿瘤浸润的T细胞,从而发挥强大的抗肿瘤活性。同时,由于其在外周组织中的激活程度较低,因此能够显著减少全身毒性的发生。综上所述,Switch-2作为一种创新的IL-2突变体,不仅解决了IL-2在酸性条件下对T细胞刺激能力下降的问题,还显著降低了IL-2疗法的全身毒性。这一发现为未来的肿瘤免疫治疗提供了新的思路和策略,有望为肿瘤患者带来更加安全、有效的治疗选择。
综上所述,该研究团队针对IL-2疗法在高剂量使用时疗效受限及副作用显著的问题,创造性地设计并制备了一种在酸性pH条件下具有卓越性能的IL-2突变体蛋白——Switch-2。该突变体能够在体内酸性pH的组织环境中被有效激活,进而展现出强大的抗肿瘤活性,显著遏制了肿瘤的进展。尤为重要的是,与IL-2的高剂量疗法相比,Switch-2能够大幅度降低全身毒性的发生。
这一研究成果不仅标志着对IL-2疗法的重大改进,而且其展现出的pH敏感性特征也为优化其他细胞因子的疗效提供了宝贵的参考模板。此外,该研究还为我们理解细胞外其他物理化学特征对健康与患病组织中细胞因子活性和功能的影响奠定了坚实的基础。这些发现有望为未来的细胞因子疗法开辟新的道路,推动肿瘤免疫治疗领域取得更加显著的进展。
| 名称 | 货号 | 规格 |
| IL-2 Protein, Mouse | UA040171-10μg | 10μg |
| IL-2 Protein, Rat | UA040229-1mg | 1mg |
| mIL-2 MAb (Cl 142206 (25 ug) | MAB402-SP | 25ug |
| Human IL-2 | S0A4037-10ug | 10ug |



































