上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|SARS-CoV-2 包膜蛋白导致急性呼吸窘迫综合征样病理损伤并构成抗病毒靶点
120 人阅读发布时间:2025-02-26 13:17
研究背景
自2019年底新型冠状病毒(SARS-CoV-2)感染暴发以来,全球公共卫生领域面临了前所未有的挑战。细胞因子风暴和多器官衰竭是SARS-CoV-2感染导致死亡的主要原因,但SARS-CoV-2引发过度损伤的具体机制仍不明确。一项新的研究揭示了SARS-CoV-2包膜(2-E)蛋白在导致急性呼吸窘迫综合征(ARDS)样病理损伤中的关键作用,并指出其可能作为抗病毒治疗的靶点。

研究方法
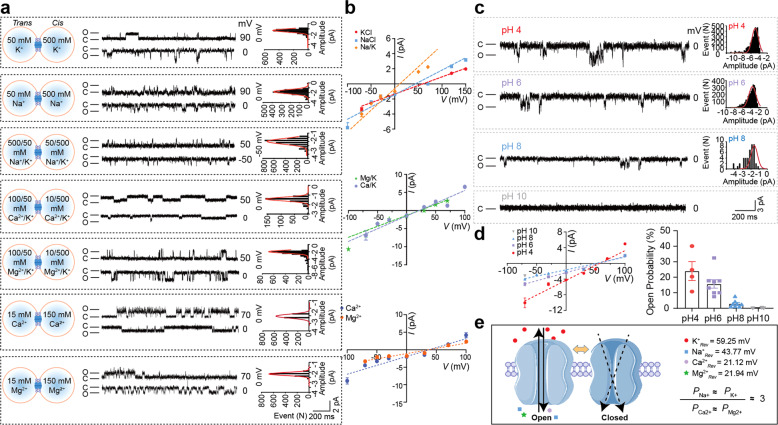
在这项研究中,科学家们发现SARS-CoV-2的2-E蛋白能够在体内和体外单独导致ARDS样病理损伤。研究团队首先观察到,2-E蛋白在双层脂质膜中形成了一种pH敏感的阳离子通道。在SARS-CoV-2感染的细胞中,2-E通道的异源表达诱导了多种易感细胞的快速死亡,并在巨噬细胞中引发了细胞因子和化学因子的强烈分泌。此外,向小鼠静脉注射纯化的2-E蛋白导致肺部和脾脏出现ARDS样病理损伤。
研究结果
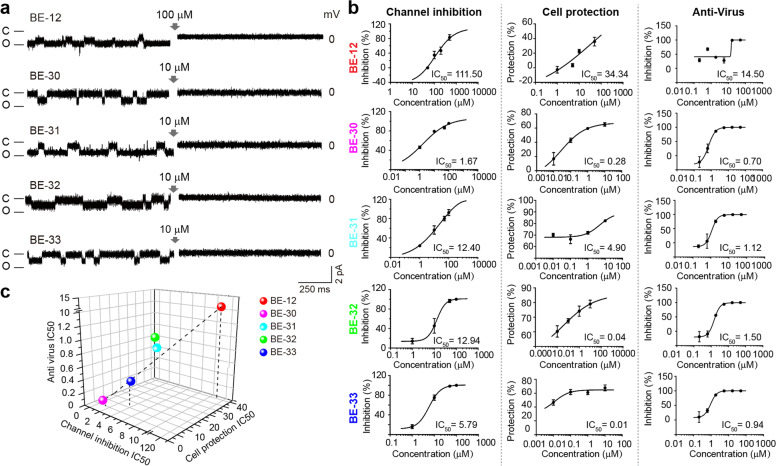
研究团队进一步发现,一种降低2-E通道活性的显性负性突变能够减轻细胞死亡和SARS-CoV-2的产生。这表明2-E蛋白的通道活性与其致病性密切相关。随后,科学家们鉴定出了一种新的通道抑制剂,该抑制剂在体外显示出强大的抗SARS-CoV-2活性和优异的细胞保护作用,且这些活性与抑制2-E通道的能力呈正相关。重要的是,在预防性和治疗性给予通道抑制剂后,SARS-CoV-2感染的表达人类血管紧张素转换酶2(hACE-2)的转基因小鼠的肺部病毒载量和炎症细胞因子分泌均有效降低。
研究意义
这项研究不仅揭示了SARS-CoV-2包膜蛋白导致ARDS样病理损伤的新机制,还为开发针对SARS-CoV-2的抗病毒药物提供了新的靶点。2-E蛋白作为潜在的药物靶点,具有广阔的研究前景和应用价值。通过抑制2-E通道活性,可以降低病毒复制和细胞死亡,从而减轻疾病症状并降低死亡率。
研究展望
尽管这项研究取得了重要的进展,但仍有许多工作有待进一步开展。例如,需要深入探索2-E蛋白通道活性的具体调节机制,以及开发更多针对2-E通道的有效抑制剂。此外,还需要评估这些抑制剂在临床试验中的安全性和有效性,以确保其能够成为有效的抗病毒治疗手段。
综上所述,SARS-CoV-2包膜蛋白导致急性呼吸窘迫综合征样病理损伤的研究不仅增进了我们对SARS-CoV-2致病机制的理解,还为开发新的抗病毒药物提供了重要线索和潜在靶点。未来,随着研究的深入和技术的进步,我们有理由相信能够开发出更加安全、有效的抗病毒药物来应对SARS-CoV-2感染带来的挑战。
| 名称 | 货号 | 规格 |
| HA-Tag(C29F4)Rabbit mAb | 3724-5ml | 5ml |
| HA-Tag(C29F4)Rabbit mAb | 3724T | 20ul |
| HA-Tag(C29F4)Rabbit mAb | 3724-2ml | 2ml |
| Mouse IL-2 ELISA Kit | abs520002-96T | 96T |



































