上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|活性氧介导的M1型巨噬细胞依赖性纳米药物重塑骨关节炎炎症微环境
159 人阅读发布时间:2025-02-27 13:24
摘要
骨关节炎(OA)是一种常见的慢性炎症性疾病,其特征是关节软骨的退化和伴随的炎症反应。当前的治疗手段在缓解OA关节炎症方面仍显不足,缺乏针对性和有效性。蛋白酶体抑制剂硼替佐米(BTZ)能够有效抑制促炎细胞因子,但在炎症组织中的积累较差。为克服BTZ递送的缺陷并提高OA治疗效果,本研究设计了一种新型纳米药物(命名为BTZ@PTK),通过ROS裂解的硫缩酮(TK)键将BTZ与一种两亲共聚物(PTK)共组装而成。在OA位点过量的ROS作用下,BTZ@PTK中的TK单元被裂解,触发BTZ的受控释放,从而实现精确递送和炎症微环境的重塑。本研究表明,BTZ@PTK在脂多糖(LPS)激活的RAW264.7巨噬细胞或LPS/IFN-γ处理的原代巨噬细胞中抑制ROS生成和促炎细胞因子,同时促进M1型巨噬细胞凋亡,其效果优于单独的BTZ。在OA小鼠模型中,BTZ@PTK被动积聚在炎症关节中,减轻疼痛敏感性和步态异常。重要的是,BTZ@PTK治疗通过抑制滑膜中M1型巨噬细胞极化和促进M1型巨噬细胞凋亡,成功减轻滑膜炎,减少滑膜增生和滑膜炎评分,从而延缓软骨损伤。综上所述,BTZ@PTK通过激活M1型巨噬细胞凋亡和抑制M1型巨噬细胞介导的炎症反应,有效调节OA炎症微环境,促进OA消退。

引言
骨关节炎(OA)作为一种退行性关节疾病,在全球范围内影响着大量人口的生活质量。OA的主要病理特征包括关节软骨的逐渐退化和滑膜的慢性炎症。这种慢性炎症微环境不仅加速了软骨的破坏,还促进了疼痛、僵硬和功能障碍等症状的发展。因此,有效调节OA关节中的炎症微环境对于OA的治疗至关重要。
M1型巨噬细胞作为炎症反应的关键参与者,通过分泌促炎细胞因子和趋化因子,进一步促进炎症反应和组织损伤。在OA中,M1型巨噬细胞的极化和积累加剧了关节炎症和软骨破坏。因此,靶向M1型巨噬细胞并调节其功能是OA治疗的一个重要策略。
活性氧(ROS)作为细胞有氧代谢的产物,在维持生理稳态和信号转导中起着重要作用。然而,过量的ROS会导致氧化应激和细胞损伤,从而加剧炎症反应和组织损伤。在OA中,ROS的水平显著升高,成为促进炎症和软骨退化的重要因素。因此,开发能够响应ROS并靶向M1型巨噬细胞的纳米药物,为OA的治疗提供了新的思路。
本研究旨在设计一种新型纳米药物(BTZ@PTK),通过ROS裂解的硫缩酮(TK)键将蛋白酶体抑制剂硼替佐米(BTZ)与两亲共聚物(PTK)共组装而成。该纳米药物能够响应OA关节中过量的ROS,实现BTZ的受控释放,从而抑制M1型巨噬细胞的极化和功能,重塑OA炎症微环境,促进OA的消退。
材料与方法
材料
- 硼替佐米(BTZ)
- 两亲共聚物(PTK)
- 脂多糖(LPS)
- 干扰素γ(IFN-γ)
- RAW264.7巨噬细胞
- OA小鼠模型
方法
- BTZ@PTK纳米药物的制备:通过共组装方法,将BTZ与PTK通过ROS裂解的TK键连接,形成BTZ@PTK纳米药物。
- 纳米药物的表征:利用透射电子显微镜(TEM)、动态光散射(DLS)和傅里叶变换红外光谱(FTIR)等方法对BTZ@PTK纳米药物的形貌、粒径和化学结构进行表征。
- ROS响应性释放实验:在模拟OA关节微环境的高ROS条件下,评估BTZ@PTK纳米药物的ROS响应性释放性能。
- 细胞实验:利用RAW264.7巨噬细胞和LPS/IFN-γ处理的原代巨噬细胞,评估BTZ@PTK纳米药物对M1型巨噬细胞极化和功能的影响,包括ROS生成、促炎细胞因子分泌和细胞凋亡等。
- 动物实验:建立OA小鼠模型,通过关节注射给予BTZ@PTK纳米药物,评估其在OA治疗中的疗效和安全性,包括疼痛敏感性、步态异常、滑膜炎评分和软骨损伤程度等。
结果
BTZ@PTK纳米药物的表征
TEM和DLS结果显示,BTZ@PTK纳米药物呈球形,粒径均匀,平均粒径约为100nm。FTIR光谱确认了BTZ与PTK之间通过TK键的成功连接。
ROS响应性释放实验
在高ROS条件下,BTZ@PTK纳米药物中的TK键被裂解,触发BTZ的受控释放。释放曲线表明,BTZ的释放速率与ROS浓度呈正相关,证明了BTZ@PTK纳米药物的ROS响应性释放性能。
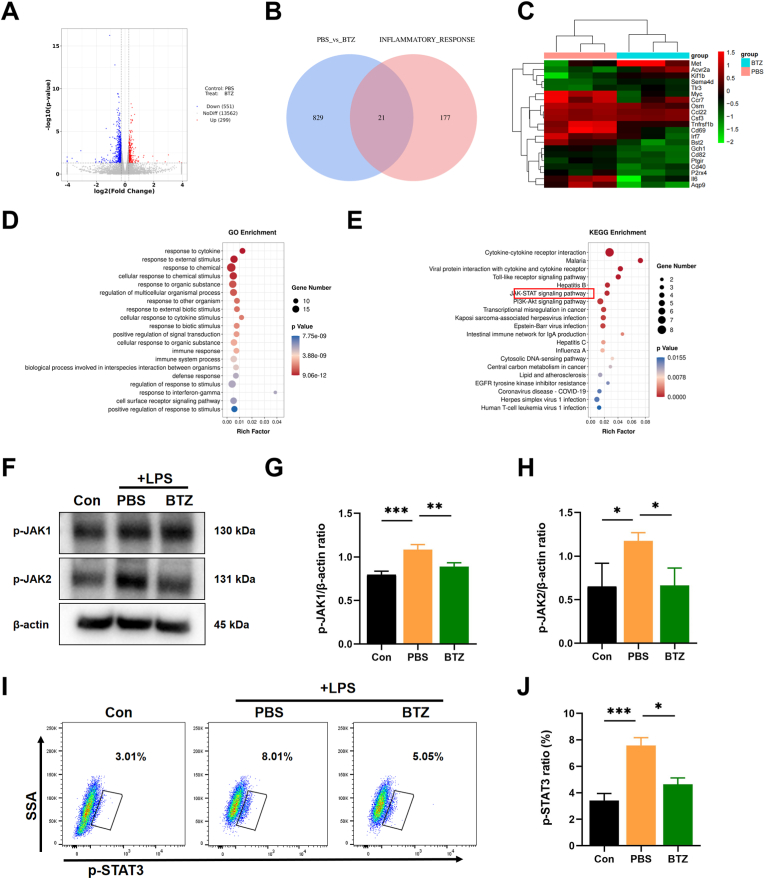
细胞实验
在RAW264.7巨噬细胞和LPS/IFN-γ处理的原代巨噬细胞中,BTZ@PTK纳米药物显著抑制了ROS的生成和促炎细胞因子的分泌,同时促进了M1型巨噬细胞的凋亡。与单独的BTZ相比,BTZ@PTK纳米药物表现出更强的抗炎和促凋亡作用。
动物实验
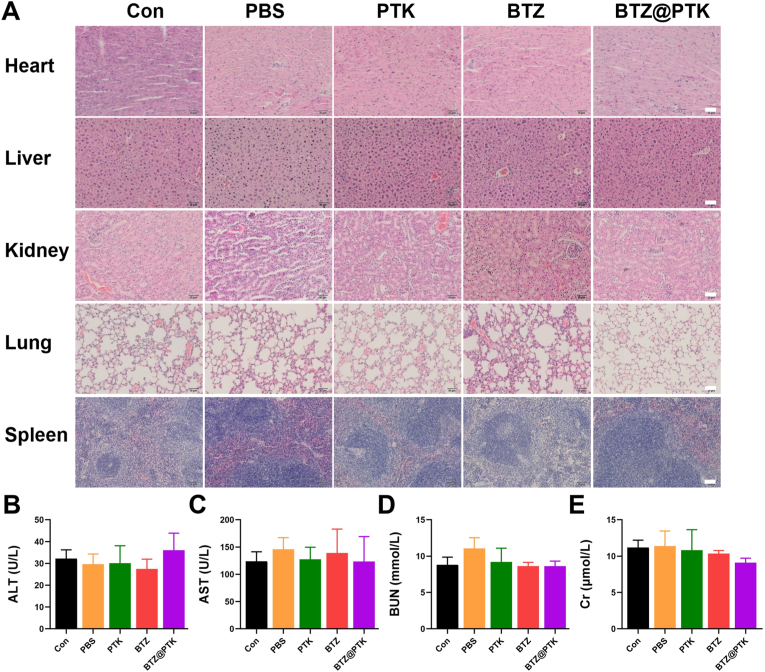
OA小鼠模型实验结果显示,BTZ@PTK纳米药物被动积聚在炎症关节中,显著减轻了疼痛敏感性和步态异常。通过组织学分析和滑膜炎评分,发现BTZ@PTK纳米药物治疗组小鼠的滑膜增生和滑膜炎程度明显降低。此外,BTZ@PTK纳米药物还通过抑制滑膜中M1型巨噬细胞的极化和促进M1型巨噬细胞的凋亡,延缓了软骨的损伤进程。
讨论
本研究成功设计了一种新型纳米药物(BTZ@PTK),该药物能够响应OA关节中过量的ROS,实现BTZ的受控释放,从而抑制M1型巨噬细胞的极化和功能,重塑OA炎症微环境。细胞实验和动物实验结果表明,BTZ@PTK纳米药物具有显著的抗炎和促凋亡作用,能够有效减轻OA小鼠的疼痛敏感性和步态异常,降低滑膜炎程度和软骨损伤程度。
BTZ@PTK纳米药物的ROS响应性释放性能是其实现精确递送和高效治疗的关键。在高ROS条件下,TK键被裂解,触发BTZ的受控释放。这种释放机制确保了BTZ在炎症关节中的有效积累,并避免了全身性副作用。
此外,BTZ@PTK纳米药物对M1型巨噬细胞的抑制作用也是其治疗OA的重要机制之一。M1型巨噬细胞在OA炎症微环境中起着关键作用,通过分泌促炎细胞因子和趋化因子,进一步促进炎症反应和组织损伤。BTZ@PTK纳米药物通过抑制M1型巨噬细胞的极化和功能,减少了促炎细胞因子的分泌,从而降低了炎症反应和组织损伤程度。
然而,本研究仍存在一些局限性。例如,BTZ@PTK纳米药物在体内的代谢和排泄机制尚不清楚,需要进一步研究以评估其长期安全性和生物相容性。此外,BTZ@PTK纳米药物的疗效和安全性在不同OA患者中的差异也需要进一步探索,以优化治疗策略并提高治疗效果。
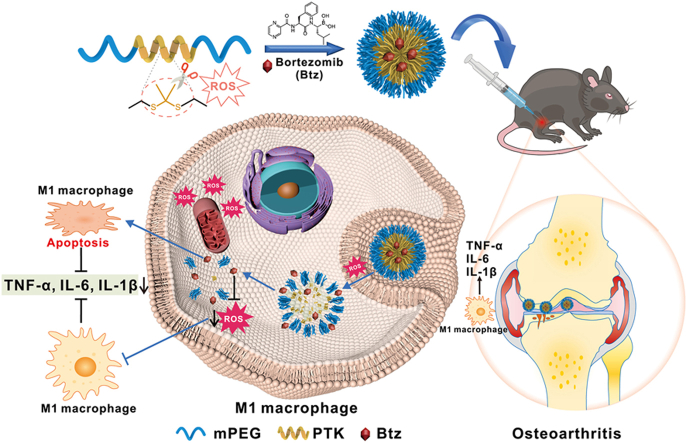
结论
本研究设计了一种新型纳米药物(BTZ@PTK),通过ROS裂解的TK键将BTZ与PTK共组装而成。该纳米药物能够响应OA关节中过量的ROS,实现BTZ的受控释放,从而抑制M1型巨噬细胞的极化和功能,重塑OA炎症微环境。细胞实验和动物实验结果表明,BTZ@PTK纳米药物具有显著的抗炎和促凋亡作用,能够有效减轻OA小鼠的疼痛敏感性和步态异常,降低滑膜炎程度和软骨损伤程度。本研究为OA的治疗提供了新的思路和方法,具有广阔的临床应用前景。
| 名称 | 货号 | 规格 |
| beta-Catenin (D10A8) XP ® Rabbit mAb | 8480S | 100ul |
| Perm Buffer III | 558050 | 125mL |
| Lyse/Fix Buffer 5X | 558049 | 250mL |
| FITC Annexin V Apoptosis Detection Kit I | 556547 | 100Tst |



































