上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|复旦大学詹成等团队在Nature Communications上发表研究——靶向“铁死亡”为癌症治疗带来新机遇
313 人阅读发布时间:2025-02-28 13:45
近日,复旦大学的詹成教授团队与德克萨斯大学MD安德森癌症中心的甘波谊教授在Nature Communications上发表了一篇题为“Polyamine-mediated ferroptosis amplification acts as a targetable vulnerability in cancer”的研究论文。该研究揭示了精氨酸作为铁死亡促进剂的新角色,并通过精氨酸转化为多胺的过程,发现了多胺以H2O2依赖的方式显著增强癌细胞对铁死亡的敏感性。这一发现不仅为铁死亡相关癌症治疗提供了新的靶点和策略,还深入探讨了癌细胞如何通过代谢调节来影响铁死亡的机制。本文将对这篇研究论文进行详细解析。

一、引言
铁死亡是一种由致死性脂质过氧化物过量触发的铁依赖形式的调性细胞死亡。其独特之处在于,它依赖于富含铁的微环境,过量的H2O2与铁发生Fenton反应,产生高反应性的羟基自由基,攻击并过氧化细胞膜上的磷脂,从而导致膜破裂和细胞死亡。由于癌细胞通常具有较高的代谢活性和ROS(活性氧)负荷,以及增强的多不饱和脂肪酸(PUFA)合成,使得它们本质上对铁死亡更为敏感。因此,了解癌细胞如何通过代谢调节来影响铁死亡,对于开发新的癌症治疗方法具有重要意义。
然而,尽管越来越多的研究表明一些酶及其代谢产物参与铁死亡调节,但内源性代谢物的促铁或抗铁死亡特性仍缺乏系统分析。在此背景下,詹成教授团队与甘波谊教授合作,利用代谢物库进行了广泛筛选,旨在发现新的铁死亡促进剂及其作用机制。
二、研究方法与结果
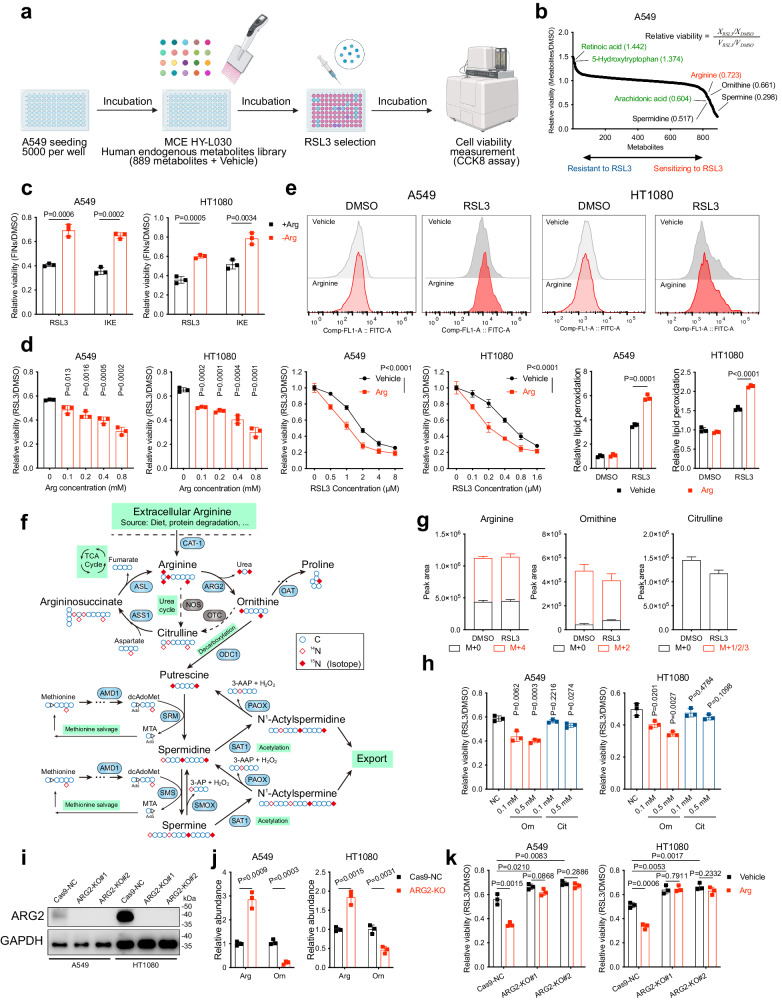
2.1 精氨酸被鉴定为铁死亡促进剂
研究团队首先利用代谢物化合物库对多种潜在的铁死亡促进剂进行了筛选。通过对比不同代谢物处理后的癌细胞存活率,他们发现精氨酸能够显著增强癌细胞对铁死亡的敏感性。为了进一步验证这一发现,研究团队利用多种实验方法,包括流式细胞术、Western blot和细胞活性检测等,深入探讨了精氨酸对癌细胞铁死亡的影响。结果表明,精氨酸确实能够以一种H2O2依赖的方式促进癌细胞的铁死亡。
2.2 多胺的促铁死亡特性及其机制
精氨酸如何促进癌细胞的铁死亡呢?研究团队进一步发现,精氨酸在细胞内被转化为多胺,包括腐胺、精胺和亚精胺等。这些多胺分子以H2O2依赖的方式发挥其促铁死亡特性。具体来说,多胺能够增加癌细胞内的ROS水平,进而促进脂质过氧化物的生成和积累。同时,多胺还能够影响癌细胞内的抗氧化系统,如谷胱甘肽(GSH)和谷胱甘肽过氧化物酶4(GPX4),使其对铁死亡更为敏感。
2.3 铁过载-WNT/MYC/ODC1-多胺-H2O2正反馈轴
研究团队还揭示了铁过载如何影响癌细胞的铁死亡过程。他们发现,铁过载能够通过WNT/MYC信号通路显著激活鸟氨酸脱羧酶1(ODC1)的表达,进而促进多胺的合成。这一过程形成了一个放大铁死亡的正反馈回路:铁过载→WNT/MYC信号通路激活→ODC1表达增加→多胺合成增加→ROS水平升高→脂质过氧化物积累→铁死亡。这一发现不仅解释了铁过载如何促进癌细胞的铁死亡,还为开发针对这一通路的靶向治疗方法提供了理论依据。
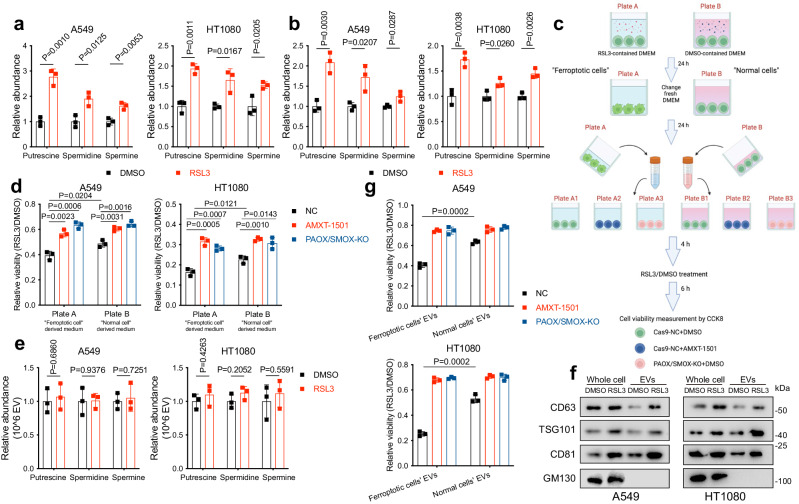
2.4 多胺超载肿瘤的代谢易感性
此外,研究团队还注意到,铁死亡细胞会释放出增强的含有多胺的细胞外囊泡到微环境中。这些囊泡能够进一步使邻近细胞对铁死亡敏感,并加速铁死亡在肿瘤区域的“扩散”。这一发现表明,多胺超载的癌细胞不仅自身对铁死亡敏感,还能够通过细胞外囊泡将这一敏感性传递给周围的癌细胞。因此,多胺代谢成为了一个可靶向的易感因素,为铁死亡相关癌症治疗提供了新的思路。
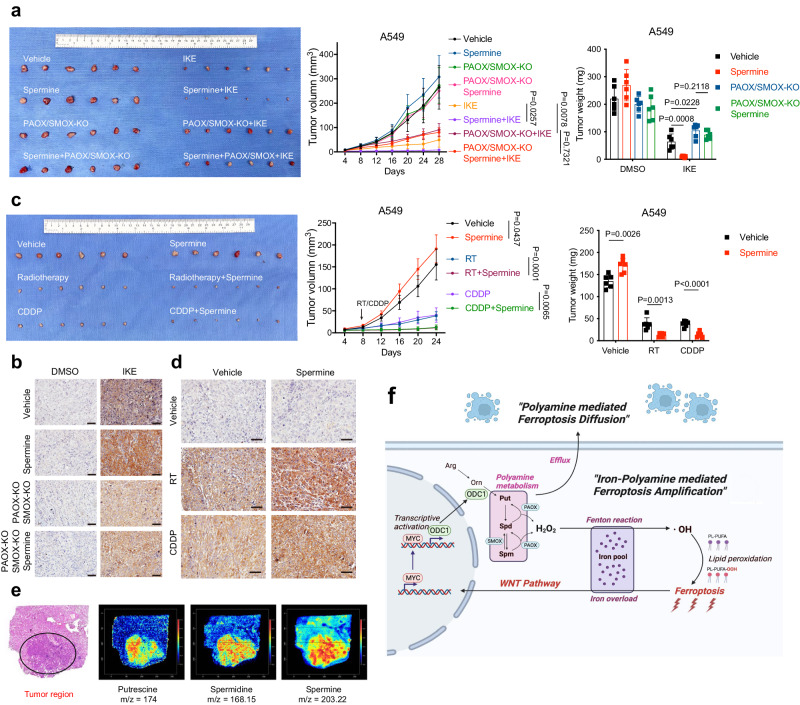
2.5 补充多胺使癌细胞对放疗或化疗增敏
研究团队还探讨了补充多胺对癌细胞放疗或化疗敏感性的影响。他们发现,通过外源性补充多胺,可以进一步增强癌细胞对放疗或化疗的敏感性。这一发现为将多胺代谢作为癌症治疗的辅助手段提供了可能。通过调节多胺水平,可以协同增强传统癌症治疗方法的疗效,从而提高患者的生存率和生活质量。
三、讨论与展望
3.1 铁死亡在癌症治疗中的潜力
越来越多的证据表明,铁死亡在肿瘤生物学和癌症治疗中起着关键作用。一方面,多种经典的癌症治疗策略如化疗、放疗和靶向治疗等均可触发铁死亡。另一方面,铁死亡参与一组与癌症相关的信号通路,如WNT/β-catenin、MYC、HIF-1α和P53等。因此,通过调节癌细胞对铁死亡的反应,可以为治疗传统疗法难治的癌症提供新的途径。
3.2 癌细胞代谢适应与铁死亡的关系
癌细胞具有独特的代谢特征,如ROS的高负荷和增强的PUFA合成等,这些特征使它们本质上对铁死亡更为敏感。然而,癌细胞也能够通过代谢适应来抵抗铁死亡,如通过增加抗氧化酶的表达和活性来降低ROS水平等。因此,了解癌细胞如何通过代谢调节来影响铁死亡对于开发有效的癌症治疗方法至关重要。
3.3 多胺代谢作为癌症治疗的靶点
本研究发现多胺代谢是铁死亡的一个可靶向易感因素。通过调节多胺水平或抑制其合成酶如ODC1的活性,可以影响癌细胞的铁死亡敏感性。此外,由于癌细胞通常具有较高的细胞内多胺丰度,因此多胺代谢成为了一个具有潜力的癌症治疗靶点。未来可以针对这一靶点开发新的药物或治疗方法,以更有效地抑制癌细胞的生长和增殖。
3.4 细胞外囊泡在铁死亡传播中的作用
本研究还发现铁死亡细胞会释放出含有多胺的细胞外囊泡到微环境中,从而进一步使邻近细胞对铁死亡敏感。这一发现揭示了细胞外囊泡在铁死亡传播中的重要作用。未来可以进一步探讨细胞外囊泡的组成和功能以及它们如何影响癌细胞的铁死亡过程,为开发新的癌症治疗策略提供理论依据。
四、结论
本研究通过代谢物库筛选发现精氨酸作为铁死亡促进剂的新角色,并揭示了多胺以H2O2依赖的方式显著增强癌细胞对铁死亡的敏感性。同时,研究还发现了铁过载-WNT/MYC/ODC1-多胺-H2O2放大铁死亡的正反馈轴以及癌细胞通过多胺代谢调节铁死亡的能力。此外,补充多胺还使癌细胞或异种移植瘤对放疗或化疗增敏。这些发现不仅为铁死亡相关癌症治疗提供了潜在的靶点和策略,还深入探讨了癌细胞如何通过代谢调节来影响铁死亡的机制。未来可以针对这些发现进一步开展研究,以开发更有效的癌症治疗方法。
| 名称 | 货号 | 规格 |
| Rabbit anti-SMOX Polyclonal Antibody | abs151305-50ul | 50ul |
| Rabbit anti-CD63 Polyclonal Antibody | abs149061-50ul | 50ul |
| Rabbit anti-CD63 Polyclonal Antibody | abs149061-100ul | 100ul |



































