上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|热射病诱导肝损伤的复杂分子机制:单细胞测序揭示Kupffer细胞铁死亡的关键作用
262 人阅读发布时间:2025-03-03 13:19
引言
在全球气候变化导致的极端高温事件频发的背景下,热射病(Heat Stroke,HS)已成为一个日益严重的健康问题。热射病是一种严重的热应激反应,可能导致多器官功能衰竭,其中肝损伤尤为显著。与其他形式的肝损伤不同,热射病引起的肝损伤以热细胞毒性和炎症加剧为特征,导致死亡率显著升高。然而,热射病诱导肝损伤的具体分子机制尚未完全阐明。近期,南方医科大学马强教授团队在Acta Pharmaceutica Sinica B杂志上发表了一项重要研究,题为“Heme oxygenase 1-mediated ferroptosis in Kupffer cells initiates liver injury during heat stroke”,该研究通过单细胞测序技术深入剖析了热射病诱导肝损伤的复杂分子机制,为未来的治疗策略提供了新的见解。

研究背景
热射病是一种由高温暴露引起的急性热应激反应,其核心特征是体温急剧升高,通常超过40℃,并伴有中枢神经系统功能障碍和多器官损伤。肝脏作为体内重要的代谢和解毒器官,在热射病中常受到严重损伤。临床评估已确定胆红素水平升高是Kupffer细胞(KCs)功能障碍的指标,但KCs与热射病性肝损伤的具体相关性仍不清楚。KCs是肝脏中的常驻巨噬细胞,在维持肝脏稳态和应对病原体感染中发挥着关键作用。然而,在热射病的病理过程中,KCs的功能和命运如何变化,以及它们如何影响肝损伤的进程,仍是亟待解决的问题。
研究目的
本研究旨在阐明KCs的铁死亡机制及其对HS小鼠肝损伤的炎症反应的贡献。铁死亡是一种新型细胞死亡方式,由铁依赖的脂质过氧化引起,与多种疾病的发生和发展密切相关。本研究通过单细胞转录组测序技术,深入分析了KCs在热射病条件下的铁死亡机制,以及其对肝损伤的影响。
研究方法
-
实验动物与分组:研究采用了HS小鼠模型,将小鼠分为正常对照组(NC)和HS组。HS组小鼠通过暴露于高温环境诱导热射病。
-
血清生化指标检测:通过检测小鼠血清中的丙氨酸转氨酶(ALT)、天冬氨酸转氨酶(AST)和总胆红素(TBIL)水平,评估肝损伤程度。
-
单细胞转录组测序:对来自不同组的肝巨噬细胞和单核细胞进行了单细胞转录组测序,包括NC组和HS后0h、6h及24h的样本。
-
流式细胞术:用于验证单细胞测序结果,检测KCs的数量和亚群分布。
-
免疫荧光染色:用于检测特定蛋白的表达和定位,如HMOX-1和EGR1。
-
基因集富集分析(GSEA):用于分析不同KCs亚群中基因表达的富集情况。
研究结果
-
KCs铁死亡导致HS小鼠肝损伤
HS患者肝损伤评估显示,血清ALT、AST和TBIL水平显著升高,且胆红素高者存活率低。KCs参与胆红素产生和运输,进一步检测发现HS小鼠的KCs数量显著降低。炎症因子IL-1β在HS组中升高,并与KCs共定位。氯膦酸盐脂质体(CLP)消耗肝巨噬细胞可减轻HS小鼠肝损伤,提高存活率。此外,HS小鼠KCs铁死亡增强,而铁抑素-1(Fer-1)处理可减少肝细胞死亡,因此铁死亡被确定为肝损伤的关键因素。
-
单细胞转录组测序揭示了具有可变铁死亡敏感性的不同KCs亚群
为了揭示对铁死亡具有不同敏感性的KCs亚群,作者对来自不同组的肝巨噬细胞和单核细胞进行了单细胞转录组测序。进一步的分析确定了10个巨噬细胞簇,并根据差异表达基因(DEGs)定义了六种不同的细胞亚群,包括脂质相关巨噬细胞(LAM)、肝囊巨噬细胞(LCM)、单核细胞来源的巨噬细胞(MoMF)、增殖性巨噬细胞簇(Proli-Macs)以及两种Kupffer细胞(KC1与KC2)。KEGG通路分析显示,KC2与铁死亡通路显著相关。值得注意的是,KC2在热射病6h后显著减少,表明KC2大量死亡。流式细胞术证实了这一结果。
-
KC2对铁死亡具有明显的易感性
对与铁和脂质代谢以及氧化过程相关的铁死亡相关基因的分析显示了KC1和KC2的不同功能。基因集富集分析(GSEA)强调了KC2在与炎症反应、氧化应激和脂质代谢相关的基因中的显著富集。基因本体(GO)分析强调KC2中的氧化应激、脂质代谢和IL-1β调控,而KC1富集了与补体和凝血级联、细胞粘附、白细胞分化和白细胞迁移相关的信号通路。作者观察到在HS组中改变最显著的基因Hmox1在KC2中高表达,进一步支持KC2在铁死亡中的关键作用。这些发现强调了KC2对铁死亡诱导的敏感性,及其在HS诱导的肝损伤中的重要作用。
-
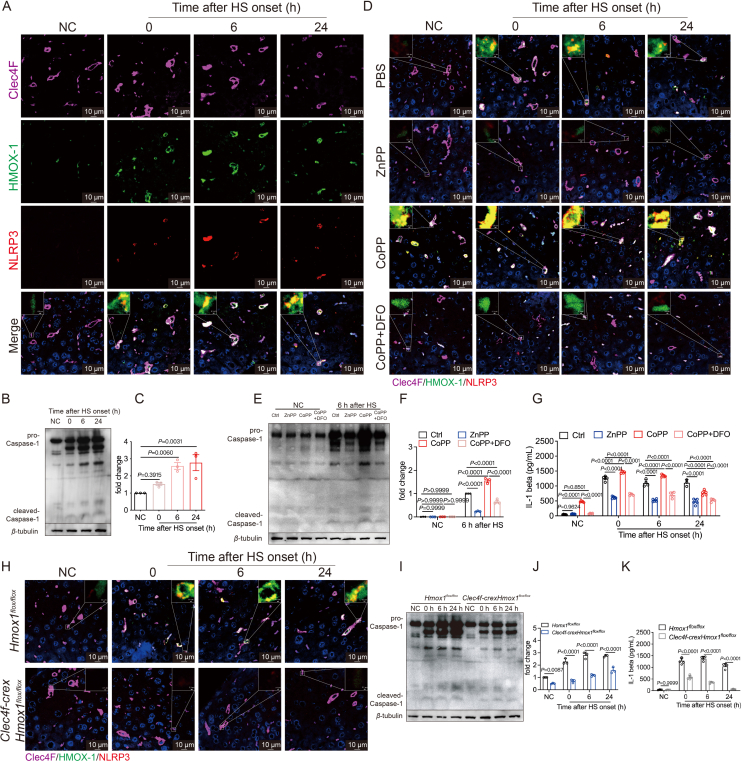
HMOX-1介导的铁死亡促进HS小鼠肝损伤
HMOX-1是一种血红素氧合酶,在热射病条件下,HMOX-1介导的KCs(尤其是KC2)中的铁死亡诱导肝损伤。HMOX-1的调节成为HS相关肝损伤的潜在治疗策略。通过抑制HMOX-1的活性或表达,可以减少KCs的铁死亡,从而减轻肝损伤。
-
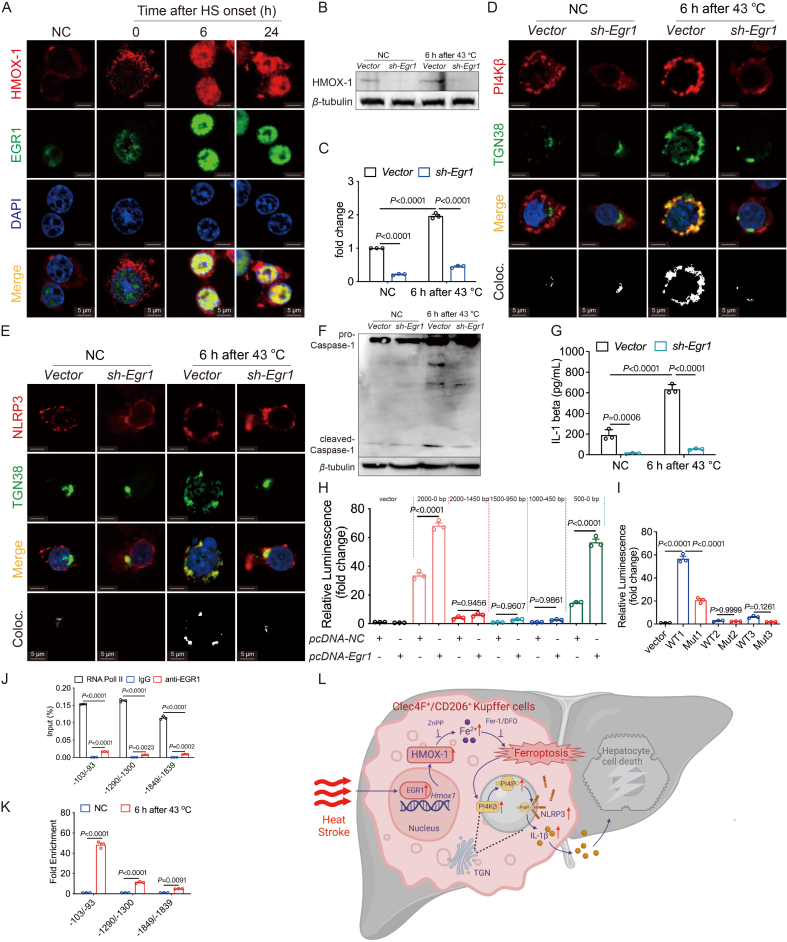
EGR1协调Hmox1转录
为了破译HMOX-1的转录调控,作者利用PROMO和GeneCards数据库来预测潜在的转录因子,将EGR1确定为候选因子。在单细胞转录组测序中,Egr1在HS后的KC2中上调,免疫荧光染色证实EGR1表达增加及其热处理后的核易位。EGR1在KC2中作为HMOX-1表达的关键调节因子,协调铁死亡和NLRP3炎症小体激活,从而在热射病条件下促进肝损伤。
结论与讨论
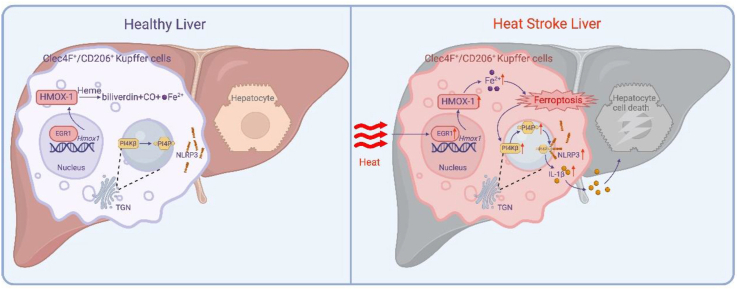
本研究通过单细胞测序技术深入剖析了热射病诱导肝损伤的复杂分子机制,强调了KCs亚群的不同反应,以及HMOX-1在协调KCs铁死亡,尤其是KC2和NLRP3炎症小体激活中的关键作用。这些发现为理解热射病诱导肝损伤的病理过程提供了新的视角,并为未来的治疗策略提供了新的靶点。
首先,本研究揭示了KCs在热射病诱导肝损伤中的关键作用。KCs作为肝脏中的常驻巨噬细胞,在维持肝脏稳态和应对病原体感染中发挥着重要作用。然而,在热射病的病理过程中,KCs的功能和命运发生了显著变化。本研究发现,HS小鼠的KCs数量显著降低,且KCs铁死亡增强。进一步的分析显示,不同KCs亚群对铁死亡具有不同的敏感性,其中KC2对铁死亡具有明显的易感性。这些发现表明,KCs的铁死亡是热射病诱导肝损伤的关键因素之一。
其次,本研究阐明了HMOX-1在KCs铁死亡和肝损伤中的关键作用。HMOX-1是一种血红素氧合酶,在热射病条件下,HMOX-1介导的KCs铁死亡诱导肝损伤。通过抑制HMOX-1的活性或表达,可以减少KCs的铁死亡,从而减轻肝损伤。此外,本研究还发现EGR1作为HMOX-1的关键转录调节因子,在热射病条件下促进HMOX-1的表达和KCs的铁死亡。这些发现为理解HMOX-1在热射病诱导肝损伤中的作用提供了新的见解,并为未来的治疗策略提供了新的靶点。
最后,本研究为未来解决热射病病证提供了坚实的实验基础。热射病是一种严重的热应激反应,其病理过程复杂且涉及多个器官和系统的损伤。本研究从KCs和HMOX-1的角度深入剖析了热射病诱导肝损伤的分子机制,为未来的研究提供了新的方向和思路。未来可以进一步探索其他细胞类型和分子在热射病诱导肝损伤中的作用,以及开发针对这些靶点的有效治疗策略。
综上所述,本研究通过单细胞测序技术深入剖析了热射病诱导肝损伤的复杂分子机制,强调了KCs亚群的不同反应以及HMOX-1在协调KCs铁死亡和NLRP3炎症小体激活中的关键作用。这些发现为理解热射病诱导肝损伤的病理过程提供了新的视角,并为未来的治疗策略提供了新的靶点。随着研究的深入和技术的不断发展,相信未来我们能够更好地理解和治疗热射病这一严重健康问题。
| 名称 | 货号 | 规格 |
| MITOSOX RED MITOCHONDRIAL SUPE | M36008 | 10X50UG |
| BODIPY 581/591 C11(脂质过氧化传感器) | D3861 | 1MG |
| LIPOFECTAMINE 3000- 0.1ML | L3000001 | 0.1mL |