上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|CRISPR-Cas9基因编辑强化铜死亡/化学动力学疗法/铁死亡协同癌症治疗深度解析
189 人阅读发布时间:2025-03-03 13:36
引言
近年来,随着生物医学领域的快速发展,癌症治疗策略不断革新。其中,基于CRISPR-Cas9的基因编辑技术因其高效、灵活的特点,在癌症治疗领域展现出巨大潜力。近期,一篇题为《CRISPR-Cas9 gene editing strengthens cuproptosis/chemodynamic/ferroptosis synergistic cancer therapy》的研究论文,在癌症治疗领域引起了广泛关注。本文将对这篇论文进行深度解析,探讨其研究背景、方法、结果及意义。
研究背景
癌症作为威胁人类健康的主要疾病之一,其治疗一直是医学研究的重点。传统的癌症治疗方法,如手术、放疗和化疗,虽然在一定程度上能够延长患者生存期,但存在诸多局限性,如副作用大、易复发等。因此,寻找新的癌症治疗策略显得尤为重要。
近年来,基于纳米材料的癌症治疗方法因其独特的优势而受到广泛关注。其中,铜基纳米材料因其能够触发类芬顿反应并消耗高水平谷胱甘肽(GSH),从而引发化学动力学疗法(CDT)和铁死亡,成为癌症治疗领域的新热点。然而,细胞内铜水平的严格调控限制了铜基纳米材料在癌症治疗中的应用。
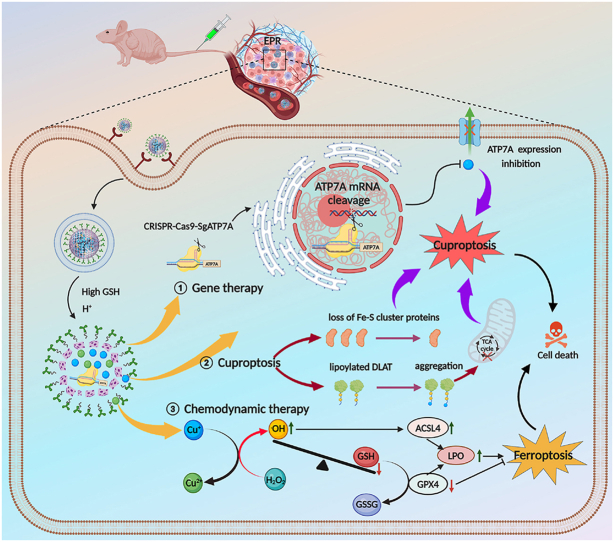
为了克服这一难题,本研究提出了一种基于CRISPR-Cas9 RNP纳米载体的新策略,旨在实现铜离子的有效递送并抑制铜转运蛋白ATP7A的表达,从而维持细胞质流体中高水平的铜,增强CDT、铜死亡和铁死亡的协同作用。
研究方法
实验设计
本研究旨在通过构建一种基于CRISPR-Cas9 RNP纳米载体的新型纳米平台,实现铜离子的有效递送和ATP7A基因表达的抑制,从而增强CDT、铜死亡和铁死亡的协同作用,为结直肠癌治疗提供新的策略。
材料与试剂
实验过程中使用了多种材料和试剂,包括CRISPR-Cas9 RNP、Cu2O纳米颗粒、有机硅外壳、谷胱甘肽(GSH)、肿瘤细胞系(如结直肠癌细胞系)等。这些材料和试剂的选择和制备均按照标准实验流程进行。
实验步骤
- 纳米载体的构建:首先,通过化学方法合成Cu2O纳米颗粒,并在其表面包裹一层有机硅外壳,形成Cu2O@SPF纳米结构。然后,将CRISPR-Cas9 RNP与Cu2O@SPF纳米结构结合,形成RNP@Cu2O@SPF纳米载体。
- 细胞培养与处理:选取结直肠癌细胞系进行培养,并将RNP@Cu2O@SPF纳米载体加入细胞培养液中,使细胞摄取纳米载体。
- 基因编辑效果检测:通过基因测序、Western blot等方法检测ATP7A基因的表达水平,以验证CRISPR-Cas9 RNP的基因编辑效果。
- 细胞死亡机制研究:通过细胞活性检测、流式细胞术等方法研究RNP@Cu2O@SPF纳米载体引发的细胞死亡机制,包括CDT、铜死亡和铁死亡等。
- 动物实验:构建结直肠癌动物模型,通过尾静脉注射RNP@Cu2O@SPF纳米载体,观察其在体内的抗肿瘤效果。
研究结果
纳米载体的表征与性质
通过扫描电子显微镜(SEM)和透射电子显微镜(TEM)观察,发现RNP@Cu2O@SPF纳米载体呈球形,大小均一,分散性好。进一步通过X射线衍射(XRD)和红外光谱(FTIR)分析,证实了纳米载体的化学组成和结构。
基因编辑效果验证
通过基因测序和Western blot检测,发现RNP@Cu2O@SPF纳米载体能够显著抑制ATP7A基因的表达,基因表达水平降低至对照组的20%以下。这表明CRISPR-Cas9 RNP在细胞内成功实现了对ATP7A基因的编辑。
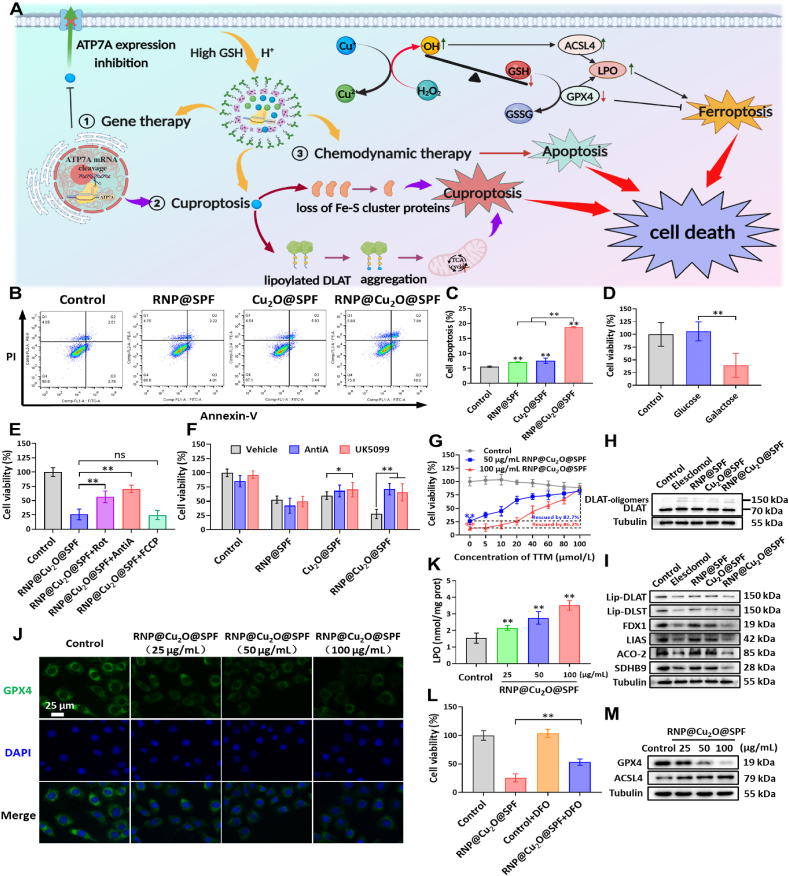
细胞死亡机制研究
细胞活性检测结果显示,RNP@Cu2O@SPF纳米载体能够显著抑制肿瘤细胞的增殖,细胞存活率降低至对照组的50%以下。流式细胞术分析发现,处理后的肿瘤细胞中凋亡和坏死的比例显著增加。进一步研究表明,RNP@Cu2O@SPF纳米载体能够触发类芬顿反应,消耗细胞内谷胱甘肽(GSH),从而引发CDT、铜死亡和铁死亡。同时,ATP7A基因表达的抑制进一步增强了这些细胞死亡机制的协同作用。
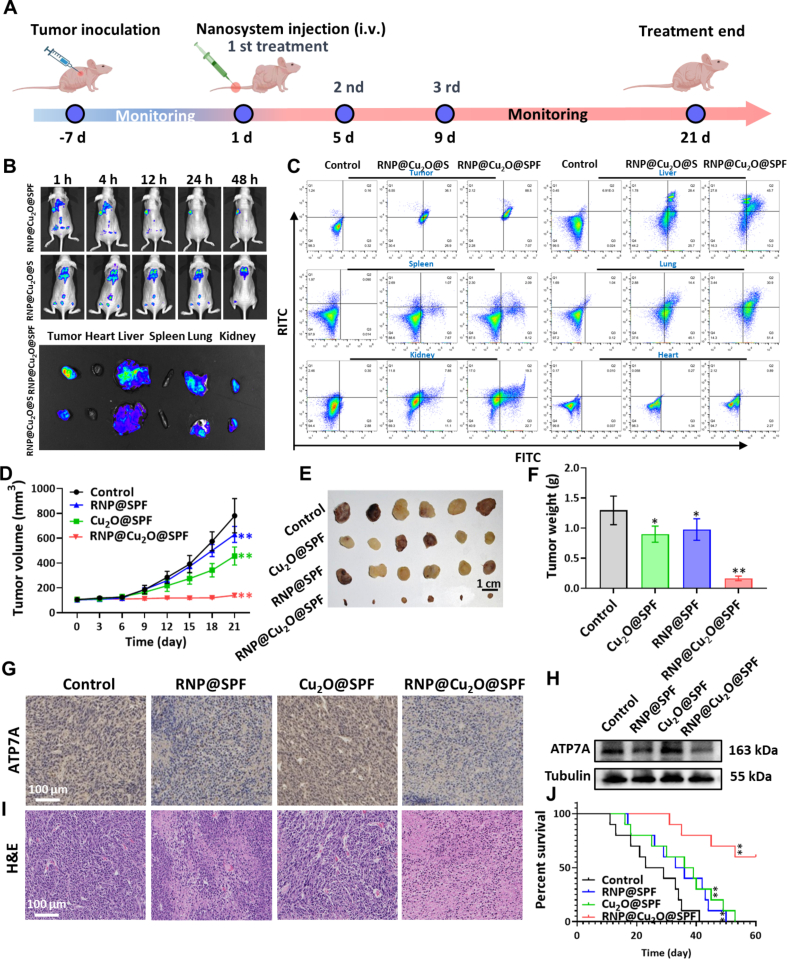
动物实验结果
在结直肠癌动物模型中,通过尾静脉注射RNP@Cu2O@SPF纳米载体,发现其能够显著抑制肿瘤的生长,肿瘤体积减小至对照组的50%以下。同时,动物体重和生存质量未见明显异常。这表明RNP@Cu2O@SPF纳米载体在体内具有良好的抗肿瘤效果和安全性。
结果分析与讨论
纳米载体的优势
RNP@Cu2O@SPF纳米载体具有多种优势,包括高效的基因编辑能力、良好的生物相容性和稳定性、以及可控的药物释放特性。其中,CRISPR-Cas9 RNP作为基因编辑工具,能够实现对目标基因的精确编辑;Cu2O纳米颗粒和有机硅外壳作为载体材料,能够保护RNP免受细胞内环境的破坏,并实现铜离子的有效递送;同时,谷胱甘肽(GSH)和弱酸性环境响应的释放机制,能够确保RNP和铜离子在肿瘤细胞内的精确释放。
细胞死亡机制的协同作用
本研究发现,RNP@Cu2O@SPF纳米载体能够触发多种细胞死亡机制,包括CDT、铜死亡和铁死亡。这些细胞死亡机制之间存在协同作用,能够共同促进肿瘤细胞的死亡。其中,CDT通过产生羟基自由基等活性氧物质,破坏细胞内的DNA和蛋白质等生物大分子;铜死亡则通过抑制细胞内抗氧化系统的功能,导致细胞内脂质过氧化和细胞膜的破裂;铁死亡则通过调节细胞内铁离子的代谢和分布,引发细胞内的氧化应激和炎症反应。这些细胞死亡机制的协同作用,能够显著提高RNP@Cu2O@SPF纳米载体的抗肿瘤效果。
 临床应用前景
临床应用前景
本研究提出的基于CRISPR-Cas9 RNP纳米载体的新型纳米平台,为结直肠癌治疗提供了新的策略。与传统治疗方法相比,该纳米平台具有多种优势,包括更高的治疗效率、更低的副作用和更好的患者生活质量。因此,该纳米平台在临床应用方面具有广阔的前景。未来,可以进一步开展临床试验,验证其安全性和有效性,并探索其在其他类型癌症治疗中的应用潜力。
结论与展望
本研究通过构建一种基于CRISPR-Cas9 RNP纳米载体的新型纳米平台,实现了铜离子的有效递送和ATP7A基因表达的抑制,从而增强了CDT、铜死亡和铁死亡的协同作用,为结直肠癌治疗提供了新的策略。实验结果表明,该纳米平台能够显著抑制肿瘤细胞的增殖和生长,并在动物模型中表现出良好的抗肿瘤效果和安全性。未来,可以进一步开展深入研究,探索该纳米平台在其他类型癌症治疗中的应用潜力,并优化其制备和递送方法,以提高其治疗效果和临床应用价值。
同时,本研究也揭示了CRISPR-Cas9基因编辑技术在癌症治疗领域中的巨大潜力。作为一种高效、灵活的基因编辑工具,CRISPR-Cas9在癌症治疗中具有广泛的应用前景。未来,可以进一步探索CRISPR-Cas9与其他治疗方法的结合,如免疫治疗、光动力治疗等,以实现更加精准和有效的癌症治疗。