上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|AI赋能药物发现:探索三阴性乳腺癌焦亡治疗的新篇章
121 人阅读发布时间:2025-03-04 13:39
传统药物研发领域面临着诸多挑战,如成功率低、成本高、研发周期长等问题。随着科技的进步,尤其是多种组学技术在患者队列数据中的应用,药物研发领域迎来了新的契机。然而,庞杂的数据形式和靶点分布不均使得药物开发和精准医疗成为一项艰巨的任务。为了改变这一现状,复旦大学药学院庞志清副研究员、王建新教授与微软亚洲研究院(上海)李东胜博士团队携手合作,在三阴性乳腺癌(TNBC)的焦亡治疗领域取得了显著进展。他们基于靶标组学开发了一种智能复方药物发现框架,为药物研发提供了一种全新的模式。本文将详细解析这篇题为“AI-powered omics-based drug pair discovery for pyroptosis therapy targeting triple-negative breast cancer”的研究论文,探讨其在药物研发领域的创新意义。
研究背景
三阴性乳腺癌(TNBC)是一种高度侵袭性的乳腺癌亚型,其特点在于雌激素受体(ER)、孕激素受体(PR)和表皮生长因子受体2(HER2)均为阴性,导致缺乏针对性的治疗策略。目前,TNBC的治疗手段相对有限,且预后较差,因此迫切需要新的治疗策略来改善患者预后。
焦亡(Pyroptosis)是一种由炎性小体介导的程序性细胞死亡方式,在肿瘤治疗中具有潜在的应用价值。然而,如何有效诱导TNBC细胞发生焦亡,同时减少对传统化疗药物的耐药性,是当前研究的难点之一。
研究目的
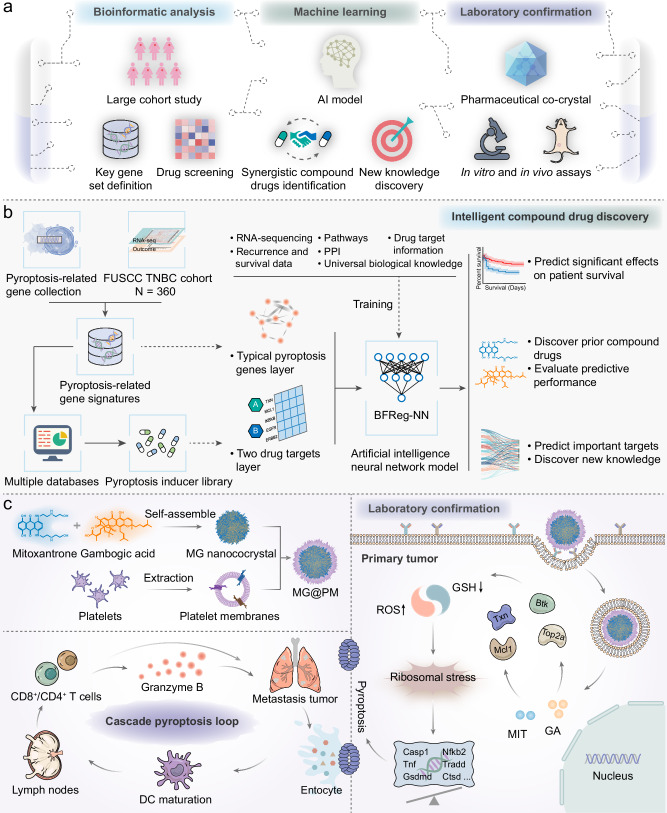
本研究旨在通过整合大数据生信分析、人工智能、剂型开发及实验验证等多学科技术,构建一种智能复方药物发现框架,用于探索针对TNBC的焦亡治疗策略。通过系统性识别TNBC焦亡关键基因,并利用AI技术快速筛选及优化复方焦亡药物组合,最终实现老药新用,为难治性疾病的精准治疗和药物开发提供新的思路。
研究方法
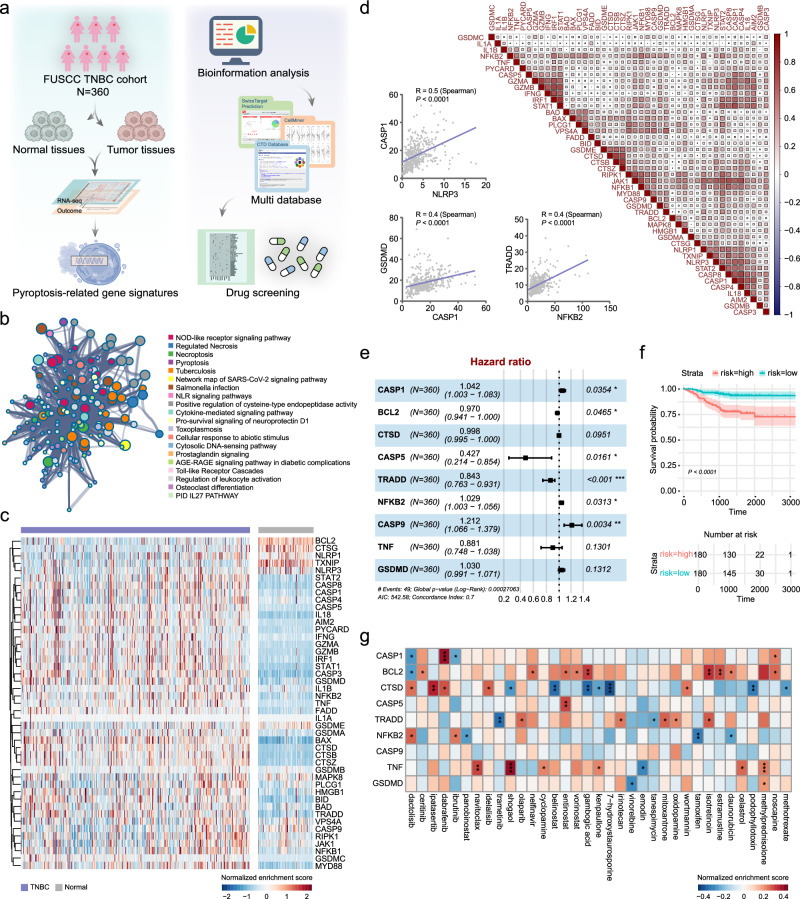
1. 探索TNBC病人的基因图谱特征
研究团队首先利用多种组学技术,包括基因组学、转录组学和蛋白质组学等,对TNBC患者的队列数据进行了深入分析。通过比较正常乳腺组织与TNBC组织的基因表达谱,他们系统性地识别出了一系列与TNBC焦亡相关的关键基因。这些基因在TNBC细胞中表达异常,且与焦亡过程密切相关,为后续的药物筛选提供了重要依据。
2. 建立潜在的焦亡诱导剂集合
为了寻找能够诱导TNBC细胞发生焦亡的药物,研究团队利用药物数据库进行了广泛的挖掘。他们筛选了数千种已知药物,通过计算模拟和实验验证,最终建立了一个包含潜在焦亡诱导剂的集合。这些药物在体外实验中表现出对TNBC细胞的焦亡诱导作用,为后续的药物组合筛选提供了丰富的候选药物库。
3. 构建生物因子调控的神经网络模型BFReg-NN
为了高效、精准地筛选复方焦亡药物组合,研究团队开发了一种基于生物因子调控的神经网络模型BFReg-NN。该模型能够模拟药物在生物体内的作用机制,预测药物组合对TNBC细胞的焦亡诱导效果。通过训练和优化,BFReg-NN能够快速筛选出具有最优焦亡诱导效果的药物组合,为后续的实验验证提供了有力支持。
4. 开发优选药对的新型复方药物制剂MG@PM
在筛选出最优药物组合后,研究团队采用仿生纳米共晶策略,开发了优选药对米托蒽醌和藤黄酸的新型复方药物制剂MG@PM。该制剂具有良好的稳定性和生物利用度,能够在体内有效释放药物,发挥焦亡诱导作用。同时,MG@PM的制备过程简单、成本低廉,具有潜在的临床应用前景。
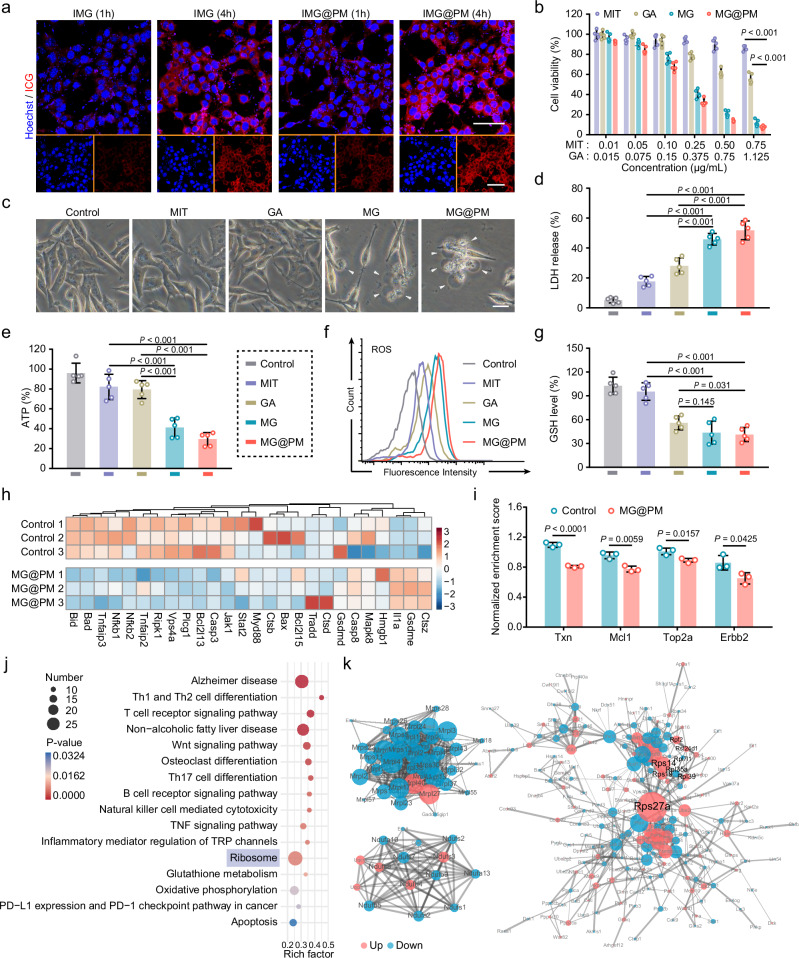
5. 实验验证MG@PM的焦亡诱导及肿瘤免疫效果
为了验证MG@PM的焦亡诱导及肿瘤免疫效果,研究团队在TNBC模型中进行了体内外实验。结果表明,MG@PM能够显著诱导TNBC细胞发生焦亡,同时激活免疫系统,产生强烈的抗肿瘤效果。与临床治疗方案Anti-PD-1/Abraxane相比,MG@PM在转移瘤模型中激活的焦亡级联效应显示出超越其的潜力,为TNBC的治疗提供了新的选择。
研究结果
1. 揭示了复方药物靶点通过核糖体应激调控焦亡特征基因的独特机制
通过深入分析MG@PM诱导TNBC细胞焦亡的分子机制,研究团队发现复方药物靶点能够通过核糖体应激调控焦亡特征基因的表达。这一发现揭示了复方药物在诱导焦亡过程中的关键作用机制,为后续的药物研发提供了重要理论依据。
2. 证实了MG@PM在TNBC模型中的强大焦亡诱导及肿瘤免疫效果
体内外实验结果表明,MG@PM能够显著诱导TNBC细胞发生焦亡,同时激活免疫系统,产生强烈的抗肿瘤效果。这一发现不仅验证了MG@PM的焦亡诱导作用,还揭示了其在肿瘤免疫治疗中的潜在价值。
3. 建立了整合大数据生信分析、人工智能、剂型开发及实验验证于一体的智能复方药物发现框架
本研究成功构建了一种全新的智能复方药物发现框架,该框架整合了大数据生信分析、人工智能、剂型开发及实验验证等多学科技术。通过这一框架,研究团队能够快速筛选出具有最优焦亡诱导效果的药物组合,并开发出新型复方药物制剂。这一方法学策略为难治性疾病的精准治疗和药物开发提供了新的思路。
研究意义
1. 推动AI技术在药物研发领域的应用
本研究成功将AI技术应用于药物研发领域,通过构建生物因子调控的神经网络模型BFReg-NN,实现了药物组合的快速筛选和优化。这一方法不仅提高了药物研发的效率和准确性,还为AI技术在药物研发领域的应用提供了新的思路。
2. 拓展老药新用的可能性
通过筛选和优化复方焦亡药物组合,本研究成功开发出了一种新型复方药物制剂MG@PM。该制剂由两种已知药物组成,但在复方形式下表现出更强的焦亡诱导作用。这一发现不仅拓展了老药新用的可能性,还为药物研发提供了新的药物来源。
3. 为TNBC的治疗提供新的选择
TNBC是一种高度侵袭性的乳腺癌亚型,缺乏针对性的治疗策略。本研究通过探索TNBC的焦亡治疗策略,成功开发出了一种具有显著抗肿瘤效果的新型复方药物制剂MG@PM。这一发现为TNBC的治疗提供了新的选择,有望改善患者的预后和生活质量。
4. 促进多学科交叉融合的研究模式
本研究整合了大数据生信分析、人工智能、剂型开发及实验验证等多学科技术,构建了一种全新的智能复方药物发现框架。这一方法学策略体现了多学科交叉融合的研究模式,为推动药物研发领域的创新和发展提供了新的思路。
结论与展望
本研究通过整合大数据生信分析、人工智能、剂型开发及实验验证等多学科技术,构建了一种全新的智能复方药物发现框架,用于探索针对TNBC的焦亡治疗策略。通过系统性识别TNBC焦亡关键基因,并利用AI技术快速筛选及优化复方焦亡药物组合,研究团队成功开发出了一种新型复方药物制剂MG@PM。该制剂在TNBC模型中表现出强大的焦亡诱导及肿瘤免疫效果,为TNBC的治疗提供了新的选择。
未来,研究团队将继续深化对MG@PM作用机制的研究,探索其在临床应用中的潜力。同时,他们还将拓展智能复方药物发现框架的应用范围,将其应用于其他难治性疾病的药物研发中。相信在多学科交叉融合的研究模式下,药物研发领域将迎来更多的创新和突破。