上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|单细胞分析揭示女性乳腺纤维腺瘤:上皮细胞组成及治疗靶点深度解析
156 人阅读发布时间:2025-03-07 13:33
引言
乳腺纤维腺瘤(FAs)作为青春期女性最常见的乳腺肿瘤,其病理机制的深入解析对于开发有效的治疗方案至关重要。尽管手术切除是FAs最有效的治疗措施,但手术可能导致不良疤痕或广泛的导管损伤,且对于多发性病灶的患者而言,根除所有病变变得尤为困难。因此,非手术治疗措施的需求显得尤为迫切。2023年6月18日,浙江大学医学院附属第二医院和浙江省肿瘤微环境与免疫治疗重点实验室的黄建、陈志刚团队在《Nature Communications》上发表了一篇题为“Single cell profiling of female breast fibroadenoma reveals distinct epithelial cell compositions and therapeutic targets”的研究论文,该研究通过高通量单细胞RNA测序(scRNA-seq)分析,揭示了FAs的细胞组成、上皮结构变化及潜在的治疗靶点,为FAs的治疗提供了新的思路。

研究背景
乳腺纤维腺瘤(FAs)是一种纤维上皮性肿瘤,多发于青春期女性,且长期患有该病症的女性患乳腺癌的风险会增加。手术切除是目前最有效的治疗措施,但手术带来的不良后果,如疤痕和导管损伤,以及多发性病灶的难以根除,使得非手术治疗措施的需求日益凸显。
FAs在临床上被认为具有激素依赖性,但雌激素受体调节剂他莫昔芬在临床试验中的治疗效果并不理想。因此,解析FAs的病理机制,尤其是上皮细胞和基质细胞之间的转录差异机制,对于开发更有效的治疗方法至关重要。然而,由于疾病本身的复杂性和缺乏可重复的人体模型,这方面的研究进展一直较为缓慢。
研究方法
为了深入解析FAs的病理机制,研究人员采用了高通量单细胞RNA测序(scRNA-seq)技术,对来自诊断为典型FAs的人类女性个体的4个新鲜乳腺FA和2个配对邻近正常组织进行了单细胞RNA测序。共检测到28,101个单细胞转录组(来自纤维腺瘤的17,776个和来自正常组织的10,325个),涵盖了23,437个基因。
基于不同的基因表达特征,研究人员将这些细胞分配到10个细胞簇中,包括成熟的管腔细胞(ML)、管腔祖细胞(LP)和基底细胞(BC)、成纤维细胞(FB)、内皮细胞(EC)、周细胞(PT)、T细胞(T)、B细胞(B)和髓细胞(M),以及未知细胞(UN)。这一细胞分类为后续的深入分析提供了基础。
研究结果
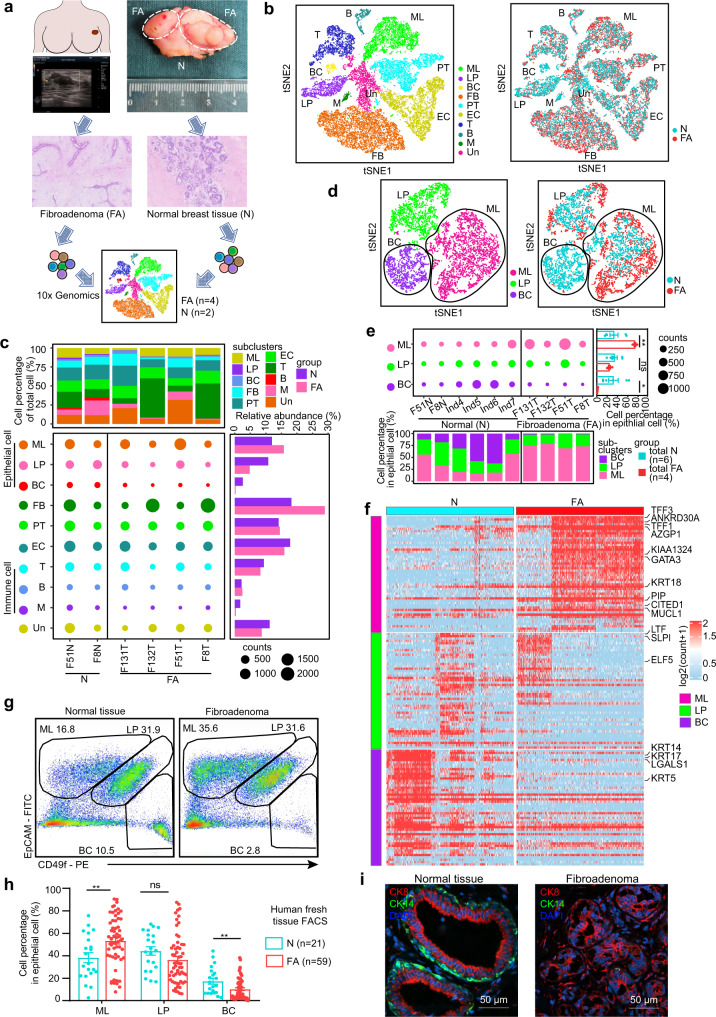
1. FAs的细胞组成和上皮结构特征
单细胞转录组分析确定了FAs的细胞组成和上皮结构特征。与正常乳腺组织相比,FAs中的基质细胞几乎不表达激素受体,而上皮细胞则表达了高水平的激素受体。免疫组织化学染色结果进一步证实了这一点,即激素受体主要在上皮细胞而非基质细胞中表达。
在FAs的基质细胞中,成纤维细胞显著增多,但增殖基因(MKI67、PCNA)和KI67免疫组化染色的分析显示,这种增加可能并非由更高的增殖引起。研究人员进一步从肿瘤组织中分离出原代上皮细胞和成纤维细胞,并进行了共培养实验。结果显示,正常乳腺组织中的成纤维细胞可以被FA上皮募集,这证明了上皮细胞在FAs形成中的重要作用。
此外,scRNA数据还显示,与正常乳腺上皮细胞相比,FAs的上皮细胞组成中成熟管腔细胞扩大,基底细胞减少。这一现象在进一步对59例新鲜FA组织及组织和21例正常乳腺组织的上皮亚群进行表征时得到了证实。FAs中基底细胞的损失表明双层结构发生了变化,这些数据表明FAs的细胞组成和结构特征与正常乳腺上皮细胞存在显著差异。
2. FAs中的上皮细胞显示激素反应性特征
为了探究FAs上皮细胞群的功能差异,研究人员进行了GO分析。结果显示,FAs上皮细胞与激素反应密切相关。基因富集分析进一步显示,受雌激素和雌激素诱导基因调节的TFF1和TFF3在FAs中变化最为显著。
免疫荧光和免疫组织化学染色进一步证实了FAs患者中这些激素相关蛋白的表达模式。对3种不同上皮细胞类型的差异表达基因(DEGs)进行比较发现:成熟管腔细胞上调的基因主要与激素反应信号通路相关;管腔祖细胞上调的基因主要与上皮细胞增殖相关;基底细胞上调的基因主要与腺体发育的调节相关。这些结果表明FAs中的上皮细胞具有激素响应的功能特征。
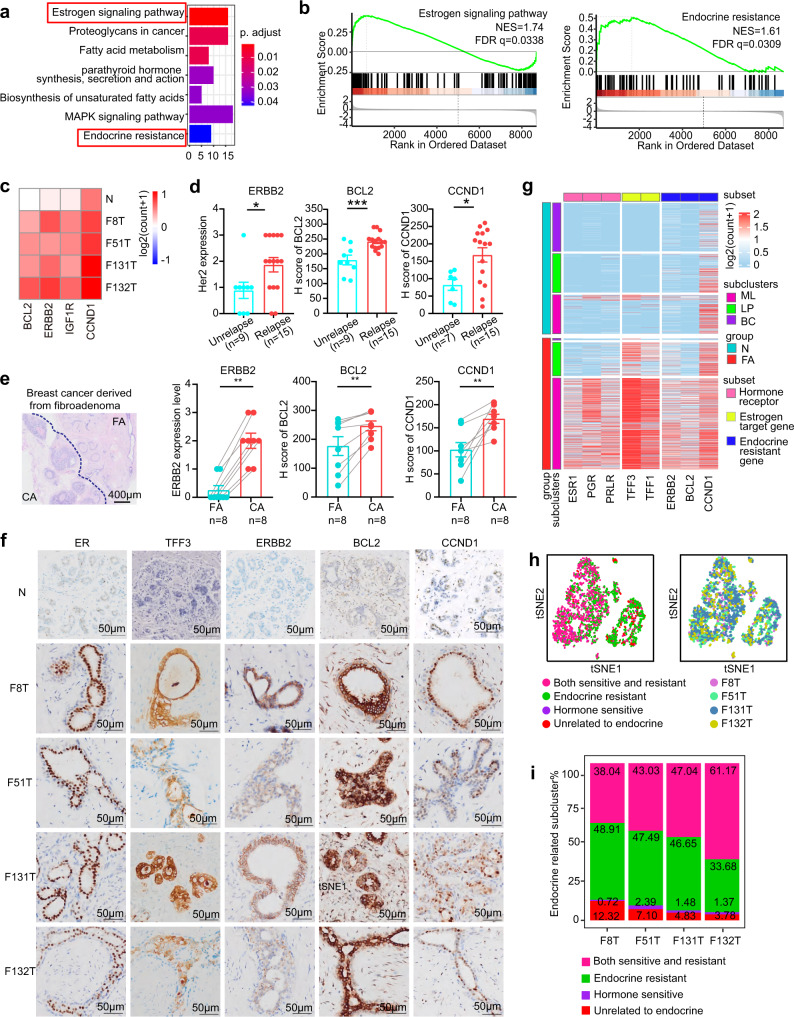
3. FAs中激素敏感性和激素抵抗性共存
临床研究显示激素敏感性通路可以控制FAs。然而,研究人员通过KEGG分析发现,除了激素敏感通路外,内分泌抵抗通路也参与其中。GSEA分析也提供了类似的结果。参与内分泌抵抗性通路的基因主要分为3个功能类别:ERBB2/IGF1R、CCND1和BCL2。这些基因与内分泌抵抗及乳腺癌复发风险增加有关。
为了验证这些发现,研究人员回顾了15例术后3年内同一乳房部位复发的FAs患者和9例无复发患者的资料。结果显示,复发FAs组中ERBB2、CCND1和BCL2的表达水平显著高于未复发组,且与FAs复发呈正相关。此外,乳腺癌患者的ERBB2、CCND1和BCL2表达水平也显著高于FAs患者。
进一步的研究发现,每位患者的上皮细胞中均能检测到ERBB2+细胞、BCL2+细胞和CCND1+细胞。对4名FAs患者进行免疫染色,并结合单细胞RNA测序进行验证。结果在正常人体组织中表达水平较低的激素敏感标记物(ER、TFF1、TFF3)和内分泌抵抗标记物(ERBB2、BCL2、CCND1)在FAs患者中均被检出,且样本间具有显著的异质性。这些数据表明FAs中激素敏感性和激素抵抗性共存。
4. 他莫昔芬与CCND1、BCL2或ERBB2抑制剂的联合用药显著抑制了他莫昔芬耐药FAs类器官的活力
由于激素敏感和激素耐药途径在FAs中共存,研究人员探索了为FAs患者提供个体化内分泌治疗的可能性。为此,他们建立了一个可扩展的FAs类器官平台,并开发了39例FA患者的类器官。这些类器官的组织学特征与原始FA上皮非常相似,且全外显子组测序结果显示类器官总体上保留了人类纤维腺瘤的基因组结构。
RNA测序显示,相对于正常上皮,类器官和FAs之间激素敏感和激素抗性标记的转录变化相似。与正常乳腺类器官相比,FAs类器官中激素敏感标记物和耐药通路标记物也上调。GSEA还揭示了人类FAs类器官中激素敏感和激素抗性通路的阳性富集。FACS进一步证明,人FAs衍生类器官的上皮细胞与原始FAs具有几乎相同的细胞组成。
为了验证激素响应功能特征,研究人员用10 nM雌二醇处理FA衍生的类器官,结果显示ER响应的标志基因显著上调,且刺激了类器官的生长。这些数据表明FA衍生的类器官是激素反应性的,可作为人类FAs的模型代表,用于开发个体化内分泌治疗。
药敏结果显示,不同患者对他莫昔芬的反应存在异质性。大多数类器官的IC50值要高于临床他莫昔芬耐药患者。基于不同人FA衍生的类器官中他莫昔芬耐药途径标志物的差异表达,研究人员将他莫昔芬与CDK4/6抑制剂Palbociclib、BCL2抑制剂Venetoclax和ERBB2抑制剂lapatinib联合,在IC10的浓度下进行药物敏感性筛选。结果显示,他莫昔芬与CCND1、BCL2或ERBB2抑制剂的用药组合显著抑制了他莫昔芬耐药FAs的生存能力,为FAs的干预提供了潜在治疗方法。
结论与展望
本研究通过高通量单细胞RNA测序分析,揭示了FAs中不同的细胞组成和上皮结构变化,并证实了上皮细胞可表现出激素响应功能特征,同时同步激活雌激素敏感和激素抗性机制。此外,研究人员还建立了一个可扩展的患者来源的FA类器官平台,通过对通路抑制剂进行系统探究以测试FAs的治疗反应。这些发现为乳腺FAs的潜在治疗策略提供了有力支持。
未来的研究可以进一步探索FAs中激素敏感性和激素抵抗性共存的机制,以及如何利用这一发现来开发更有效的个体化内分泌治疗方法。同时,FA类器官平台的建立也为研究FAs的病理机制和药物筛选提供了新的工具。随着研究的深入,相信未来会有更多针对FAs的有效治疗方法出现,为患者带来更好的治疗效果和生活质量。
| 名称 | 货号 | 规格 |
| USP9X (D4Y7W) Rabbit mAb | 14898S | 100ul |
| Pan-Keratin (C11) Mouse mAb | 4545T | 20ul |
| PD-1 (Intracellular Domain) (D7D5W) XP® Rabbit mAb | 84651S | 100ul |
| Fixable Viability Stain 700 | 564997 | 100ug |