上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|上海交大研发水凝胶微球疫苗,增强消融后抗肿瘤免疫反应
219 人阅读发布时间:2025-03-07 13:33
引言
胰腺导管腺癌(PDAC)是一种高度侵袭性的消化道癌症,其5年生存率极低,仅为7%左右。由于多数患者在确诊时已错过手术机会,化疗和免疫治疗的效果也有限,因此探索新的治疗策略显得尤为重要。微创不可逆电穿孔(IRE)消融术作为一种非热消融疗法,在治疗不可切除的胰腺癌中显示出一定的潜力。然而,胰腺癌的免疫抑制肿瘤微环境(TME)常常导致肿瘤复发和转移,使得单纯的IRE消融治疗难以达到理想的疗效。为了克服这一难题,上海交通大学附属瑞金医院的王忠敏和崔文国教授团队在《Nature Communications》上发表了一篇题为“Interventional hydrogel microsphere vaccine as an immune amplifier for activated antitumour immunity after ablation therapy”的研究论文,介绍了一种新型的水凝胶微球疫苗,通过增强内源性适应性抗肿瘤免疫,显著提高了消融治疗后的疗效。

研究背景
胰腺癌的治疗挑战
胰腺导管腺癌(PDAC)是一种极具挑战性的恶性肿瘤,其早期症状不明显,确诊时往往已处于晚期,错过了手术的最佳时机。目前,胰腺癌的化疗方案有限,且常伴有全身毒性作用,治疗效果并不理想。因此,探索新的治疗手段对于提高胰腺癌患者的生存率具有重要意义。
IRE消融术的原理与优势
不可逆电穿孔(IRE)消融术是一种新兴的非热消融疗法,其原理是利用高频电场在细胞膜上引起纳米级穿孔,扰乱细胞稳态,导致强烈的免疫原性细胞死亡(ICD)和抗原释放。IRE消融术能够在不损伤周围血管和神经的情况下有效摧毁肿瘤,并显著降低胰瘘形成和出血的风险。这一疗法在治疗局部实体瘤方面显示出明显的优势。
免疫抑制肿瘤微环境的影响
尽管IRE消融术在治疗胰腺癌中取得了一定的疗效,但肿瘤复发和转移仍然是影响患者生存率的重要因素。胰腺癌的免疫抑制肿瘤微环境是导致肿瘤复发的主要原因之一。在这种环境中,免疫细胞浸润不足,免疫细胞功能受损,免疫抑制分子积累,使得肿瘤细胞能够逃避免疫系统的监视和清除。因此,如何改善胰腺癌的免疫微环境,增强内源性适应性抗肿瘤免疫,成为提高消融治疗后疗效的关键。
免疫检查点阻断疗法的局限性
在临床实践中,免疫检查点阻断(ICB)疗法是最常用的免疫疗法之一。然而,PD-1/PD-L1或CTLA-4抑制在胰腺癌中的疗效并不理想,除非在极其罕见的微卫星不稳定胰腺癌病例中。尽管有研究表明,PD-1/PD-L1抑制可以与IRE消融产生治疗协同作用,但临床证据表明,接受联合治疗的患者仍然面临肿瘤复发的风险增加。因此,寻找新的免疫疗法,触发内源性适应性免疫应答的有效扩增,对于改善消融治疗后的免疫治疗至关重要。
研究结果
水凝胶微球疫苗的设计
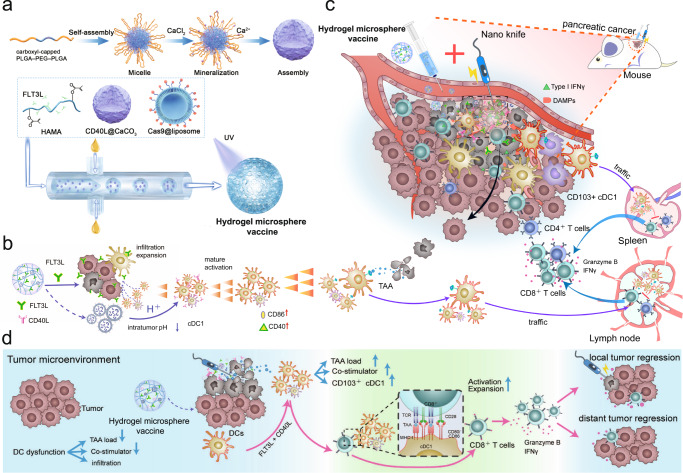
针对胰腺癌的免疫抑制肿瘤微环境,王忠敏和崔文国教授团队开发了一种新型的水凝胶微球疫苗。这种疫苗的设计思路是通过触发CD103+CD11b-cDC1介导的抗原交叉呈递级联反应,增强内源性CD8+T细胞的抗肿瘤免疫力。具体来说,研究人员将Cas9质粒和CD40L分别加载到脂质体和CaCO3纳米颗粒中,然后将它们与FLT3L细胞因子和透明质酸(HA)混合,在微流体控制下制备成水凝胶微球疫苗。这种疫苗能够在肿瘤床相对较低的pH环境下释放其携带的细胞因子和免疫佐剂,从而激活肿瘤微环境中的免疫细胞。
水凝胶微球疫苗的免疫激活机制
水凝胶微球疫苗在注射到肿瘤部位后,能够在酸性环境下释放FLT3L和CD40L细胞因子。FLT3L能够促进树突状细胞(DC)的增殖和分化,尤其是CD103+CD11b-cDC1亚型的扩增。CD40L则能够与DC表面的CD40受体结合,激活DC并促进其成熟和抗原呈递能力。此外,水凝胶微球疫苗还能够诱导cDC1介导的抗原交叉呈递和CD8+T细胞活化的火箭样级联扩增。在这一过程中,cDC1迁移到肿瘤引流淋巴结(TdLN),将捕获的肿瘤抗原呈递给CD8+T细胞,从而启动特异性抗肿瘤免疫反应。
水凝胶微球疫苗在小鼠模型中的疗效验证
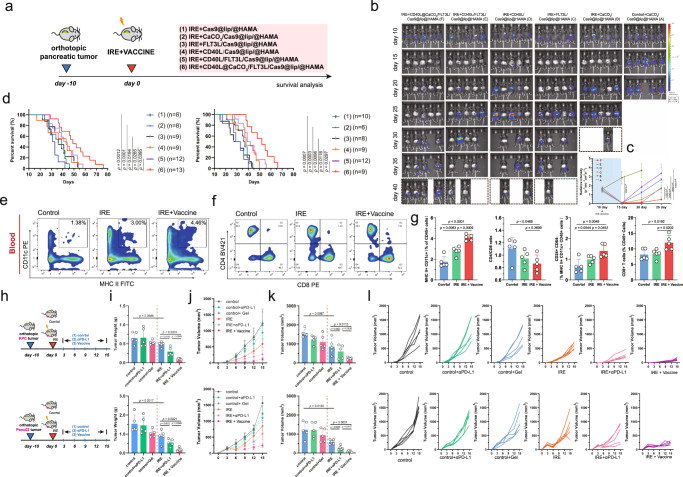
为了验证水凝胶微球疫苗的疗效,研究人员在雄性小鼠的原位胰腺癌模型中进行了实验。他们发现,与单纯接受IRE消融治疗的小鼠相比,接受水凝胶微球疫苗和IRE联合治疗的小鼠存活率显著提高,且远处转移瘤的生长受到明显抑制。此外,水凝胶微球疫苗还能够有效激活全身抗肿瘤免疫,促进肿瘤从“冷”环境向“热”环境的转化。这些结果表明,水凝胶微球疫苗作为一种免疫放大器,能够显著增强消融治疗后的抗肿瘤免疫反应。
水凝胶微球疫苗的免疫机制探讨
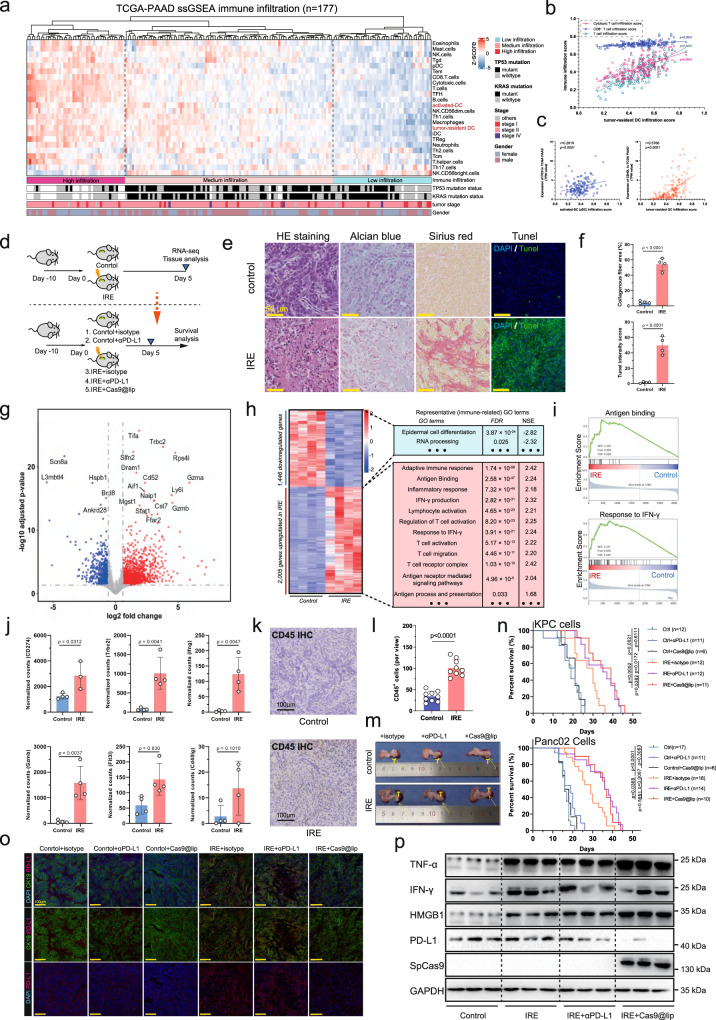
研究人员进一步探讨了水凝胶微球疫苗的免疫机制。他们发现,水凝胶微球疫苗能够显著扩增肿瘤内CD103+CD11b-cDC1的比例,并促进其表面CD86和CD40的表达。这些变化表明,水凝胶微球疫苗对肿瘤驻留的cDC1具有靶向扩增和激活作用。此外,水凝胶微球疫苗还能够刺激cDC1迁移到TdLN,激活肿瘤特异性CD8+T细胞。这一过程中,cDC1提供MHC-I/抗原复合物给CD8+T细胞上的TCR,形成TCR-MHC-I-抗原复合物,这对于CD8+T细胞特异性的抗肿瘤免疫至关重要。流式细胞术分析显示,接受水凝胶微球疫苗治疗的小鼠TdLNS中CD8+T细胞的密度、增殖能力等显著增加,提示增强的cDC1级联促进了CD8+T细胞的激活。
水凝胶微球疫苗的安全性与有效性评估
为了评估水凝胶微球疫苗的安全性和有效性,研究人员在小鼠模型中进行了详细的研究。他们发现,接受局部注射水凝胶疫苗的荷瘤小鼠肝酶天冬氨酸转氨酶(AST)和丙氨酸转氨酶(ALT)水平没有升高,表明水凝胶微球疫苗对肝脏没有毒性作用。此外,与未接受水凝胶微球疫苗治疗的小鼠相比,接受治疗的小鼠肿瘤内CD8+T细胞密度显著增加,且肿瘤浸润性细胞毒性T淋巴细胞(CTLs)的增殖和活化能力也显著增强。这些结果表明,水凝胶微球疫苗以安全有效的方式增强了消融治疗后的抗肿瘤免疫反应。
讨论与展望
水凝胶微球疫苗的优势与挑战
水凝胶微球疫苗作为一种新型的免疫疗法,在增强消融治疗后的抗肿瘤免疫反应方面显示出显著的优势。其设计巧妙地将免疫佐剂和细胞因子封装在可注射的水凝胶微球中,实现了局部释放和持续刺激免疫细胞的目的。此外,水凝胶微球疫苗还能够触发cDC1介导的抗原交叉呈递级联反应,显著增强了内源性CD8+T细胞的抗肿瘤免疫力。然而,水凝胶微球疫苗的研发和应用也面临一些挑战。例如,复杂的药物配方增加了批量生产和临床翻译的难度;药物输送工具的简化和后续制药技术的支持对于随后的临床转型是必要的。此外,目前的技术限制使得研究人员使用了MHC-I封锁而不是有针对性的cDC1耗尽,这可能影响了对其他APCs激活CD8+T细胞可能性的完全排除。因此,后续工作还应重点研究CD8+T细胞在免疫激活中的上游激活途径以及水凝胶微球疫苗与其他免疫疗法的联合应用效果。
未来研究方向
未来的研究可以进一步探索水凝胶微球疫苗与其他免疫疗法的联合应用效果。例如,将水凝胶微球疫苗与免疫检查点阻断疗法相结合,可能会进一步增强抗肿瘤免疫反应并延长患者的生存期。此外,还可以研究水凝胶微球疫苗在不同类型的肿瘤中的应用效果以及其对患者生活质量的影响。另外,随着生物材料科学和纳米技术的不断发展,未来有望开发出更加高效、安全、便捷的水凝胶微球疫苗制备和输送系统,为肿瘤免疫治疗提供更加有力的支持。
结论
上海交通大学附属瑞金医院的王忠敏和崔文国教授团队开发了一种新型的水凝胶微球疫苗,通过触发CD103+CD11b-cDC1介导的抗原交叉呈递级联反应,显著增强了消融治疗后的抗肿瘤免疫反应。在雄性小鼠的原位胰腺癌模型中,水凝胶微球疫苗以安全有效的方式将免疫冷肿瘤微环境转化为热环境,显著提高了存活率并抑制了远处转移瘤的生长。这一研究成果为胰腺癌等恶性肿瘤的免疫治疗提供了新的策略和方法,有望为改善患者的预后和提高生活质量带来新的希望。随着研究的深入和技术的不断发展,相信水凝胶微球疫苗将在未来的肿瘤免疫治疗中发挥更加重要的作用。
| 名称 | 货号 | 规格 |
| USP9X (D4Y7W) Rabbit mAb | 14898S | 100ul |
| Pan-Keratin (C11) Mouse mAb | 4545T | 20ul |
| PD-1 (Intracellular Domain) (D7D5W) XP® Rabbit mAb | 84651S | 100ul |
| Fixable Viability Stain 700 | 564997 | 100ug |