上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|华中大科研团队发现RNF186导致溃疡性结肠炎的分子机制
158 人阅读发布时间:2025-04-24 15:52
引言
炎症性肠病(Inflammatory bowel diseases, IBD)是一种慢性复发性的肠道炎症疾病,主要包括克罗恩病(Crohn disease, CD)和溃疡性结肠炎(ulcerative colitis, UC)。IBD的临床表现主要为反复发作的腹痛、腹泻和黏液脓血便等,其发病机理至今尚未完全明确。然而,越来越多的证据表明,多种遗传、环境和免疫因素共同导致了IBD的发生和发展。患者长期的炎症性病变不仅严重影响生活质量,还增加了罹患大肠癌及小肠腺癌的风险。目前,尽管对IBD进行了大量研究,但仍缺乏有效的治疗药物,疾病常常迁延不愈,给患者身心造成了极大的痛苦。
自噬作为细胞发育、分化、存活和衰老等多种生理过程的重要调控机制,近年来在IBD的研究中受到了广泛关注。全基因组关联分析(GWAS)已经确定了多个IBD易感性相关的基因,其中多个基因编码的蛋白参与了细胞自噬的调节,包括Atg16l1、ULK1和IRGM等。这些发现进一步表明自噬在宿主防御病原体和维持肠道稳态中发挥着重要作用。
RNF186(Ring finger protein 186)编码一种含有Ring结构域的E3泛素连接酶,是一种在多种生物过程中发挥重要作用的蛋白。先前的分子遗传学研究发现,RNF186的两个罕见变异RNF186A64T和RNF186R179X与溃疡性结肠炎的易感性相关。然而,RNF186在溃疡性结肠炎中的具体作用机制及其变异与UC易感性的关系尚不清楚。
近日,华中科技大学生命学院王晨辉教授团队与同济医学院荣岳光教授团队合作,在国际权威期刊《自噬》(Autophagy)上发表了一篇题为“RNF186 regulates EFNB1 (ephrin B1)-EPHB2-induced autophagy in the colonic epithelial cells for the maintenance of intestinal homeostasis”的研究论文。该研究首次揭示了RNF186通过调节EFNB1-EPHB2通路诱导的自噬在溃疡性结肠炎发生和发展中的重要作用,为溃疡性结肠炎的治疗提供了新的思路和手段。

研究背景
-
炎症性肠病(IBD)
IBD是一种以慢性复发性肠道炎症为主要特征的疾病,主要包括克罗恩病和溃疡性结肠炎。IBD的发病机理复杂,涉及多种遗传、环境和免疫因素。患者长期的炎症性病变不仅影响生活质量,还增加了患大肠癌及小肠腺癌的风险。尽管对IBD进行了大量研究,但目前仍缺乏有效的治疗药物,疾病常常迁延不愈。
-
自噬在IBD中的作用
自噬是一种细胞内的降解过程,通过溶酶体或自噬溶酶体降解受损或多余的细胞器和蛋白质,维持细胞稳态。自噬在细胞发育、分化、存活和衰老等多种生理过程中发挥着重要作用。近年来的研究发现,自噬在宿主防御病原体和维持肠道稳态中也扮演着关键角色。GWAS已经确定了多个IBD易感性相关的基因,其中多个基因编码的蛋白参与了细胞自噬的调节,如Atg16l1、ULK1和IRGM等。
-
RNF186与溃疡性结肠炎的易感性
RNF186是一种含有Ring结构域的E3泛素连接酶,参与多种生物过程的调控。先前的分子遗传学研究发现,RNF186的两个罕见变异RNF186A64T和RNF186R179X与溃疡性结肠炎的易感性相关。其中,RNF186A64T导致UC易感,而RNF186R179X是保护性变异,携带该变异不易感UC。然而,RNF186在溃疡性结肠炎中的具体作用机制及其变异与UC易感性的关系尚不清楚。
研究目的
本研究旨在探讨RNF186在溃疡性结肠炎中的具体作用机制,特别是其如何通过调节EFNB1-EPHB2通路诱导的自噬影响溃疡性结肠炎的发生和发展。通过该研究,希望能够为溃疡性结肠炎的治疗提供新的思路和手段。
研究方法
-
实验材料
研究采用了多种实验材料,包括结肠上皮细胞系、小鼠模型、RNF186及EPHB2敲除小鼠、重组蛋白EFNB1-Fc等。
-
实验方法
- 细胞培养与转染:将结肠上皮细胞系进行培养,并通过脂质体转染技术将RNF186及其变异体基因导入细胞。
- 自噬检测:利用荧光显微镜观察自噬体的形成,并通过Western blot检测自噬相关蛋白的表达水平。
- 泛素化修饰检测:通过质谱鉴定和免疫共沉淀技术检测RNF186对EPHB2的泛素化修饰。
- 动物实验:构建RNF186及EPHB2敲除小鼠,并通过DSS诱导小鼠结肠炎模型,观察小鼠的结肠炎症状及自噬水平。
- 药物治疗实验:为小鼠注射重组蛋白EFNB1-Fc,观察其对DSS诱导的结肠炎症状的治疗作用。
研究结果
-
RNF186通过泛素化修饰调节EFNB1-EPHB2信号
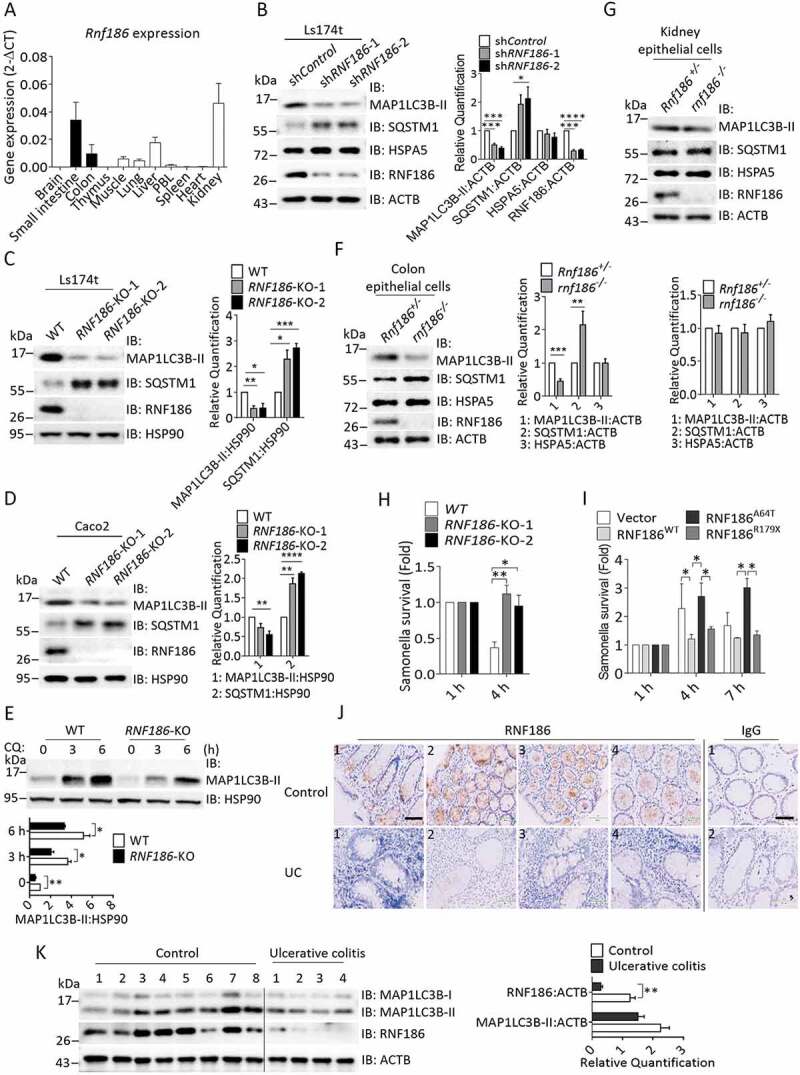
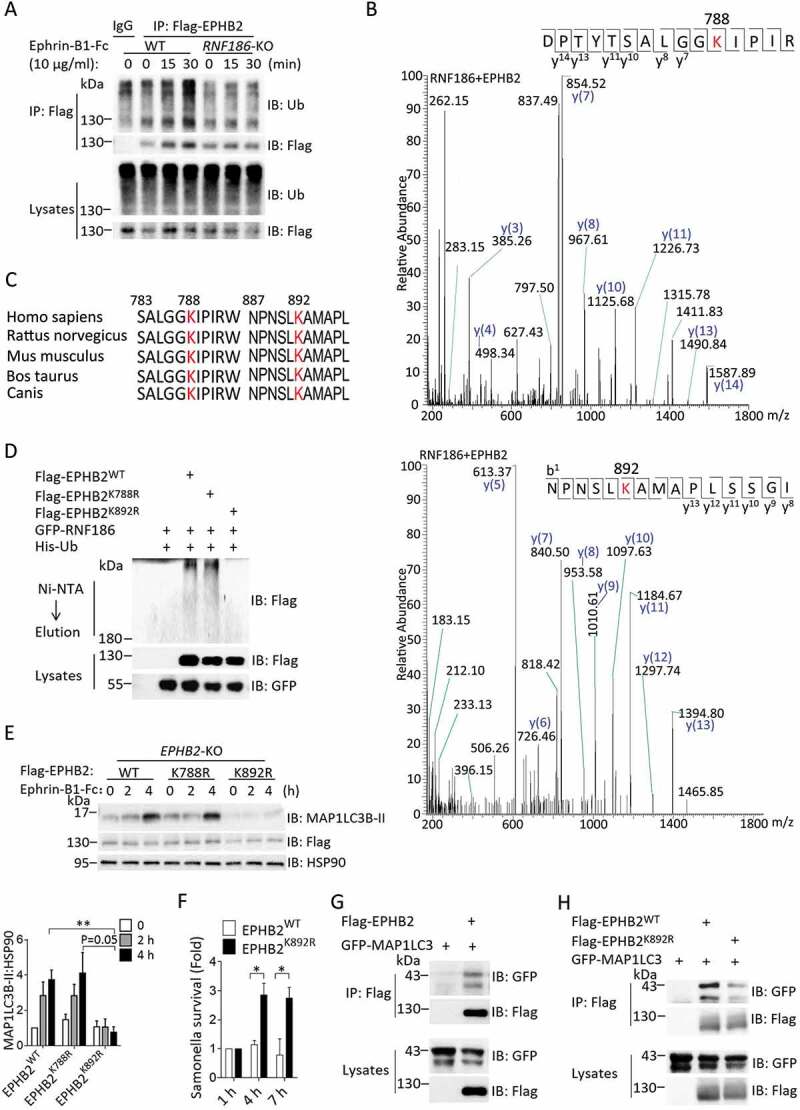
研究团队发现,RNF186作为一种E3泛素连接酶,能够泛素化修饰受体酪氨酸激酶EPHB2。通过质谱鉴定,确定了EPHB2的K892位点在RNF186的催化下发生泛素化修饰。进一步的研究发现,RNF186的UC易感性变体RNF186A64T失去了与EPHB2的相互作用,损伤了EPHB2的泛素化;而UC保护性变体RNF186R179X增加了与EPHB2的相互作用,促进了EPHB2的泛素化。这些结果表明,RNF186通过泛素化修饰调节EPHB2的信号传导。
-
RNF186对EFNB1-EPHB2诱导的自噬至关重要
EPHB2的配体EFNB1能够作用于肠道上皮细胞诱导自噬。研究团队发现,这一过程依赖于RNF186介导的EPHB2第892位赖氨酸泛素化。通过功能研究,团队发现EFNB1-RNF186-EPHB2轴诱导的自噬对于肠道上皮清除胞内细菌感染至关重要。该通路失活会导致肠道上皮细胞清除胞内菌缺陷,提示该机制是RNF186变异导致UC易感性的主要原因。
-
重组蛋白EFNB1-Fc具有治疗溃疡性结肠炎的潜力
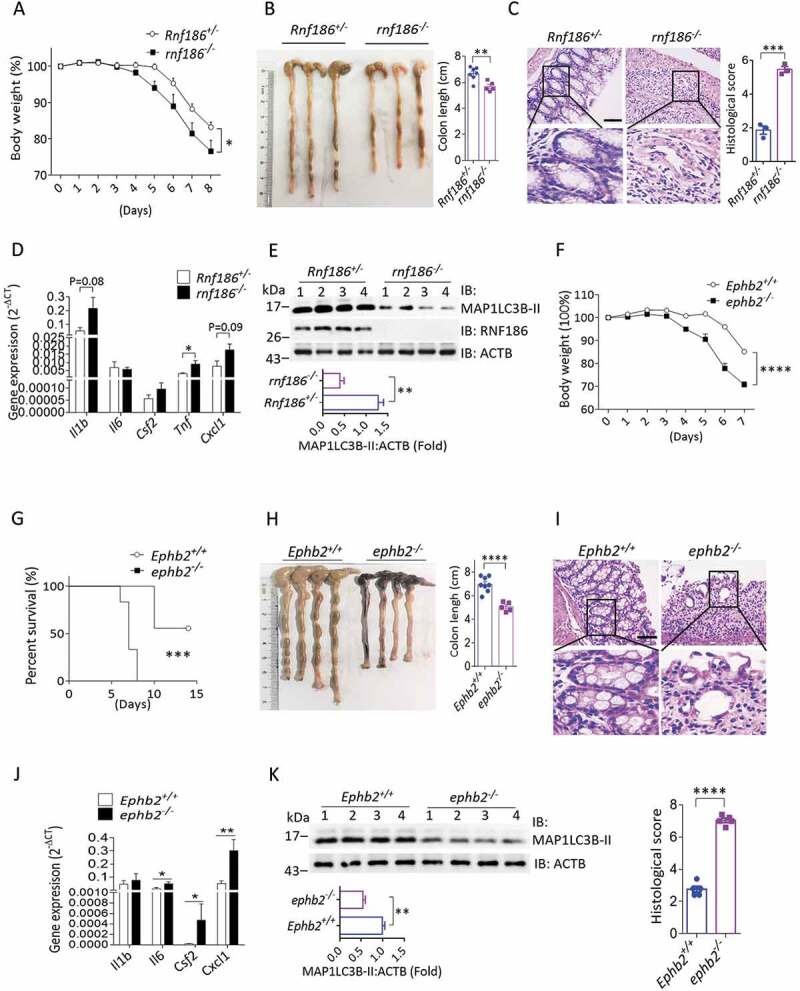
研究团队进一步发现,为小鼠注射重组蛋白EFNB1-Fc能够激活结肠上皮自噬,并在一定程度上减轻DSS诱导的结肠炎症状。这一发现提示,重组蛋白EFNB1-Fc具有成为治疗溃疡性结肠炎药物的潜力。
研究意义
-
揭示了RNF186在溃疡性结肠炎中的重要作用
本研究首次揭示了RNF186通过调节EFNB1-EPHB2通路诱导的自噬在溃疡性结肠炎发生和发展中的重要作用。这一发现不仅丰富了我们对溃疡性结肠炎发病机理的认识,还为溃疡性结肠炎的治疗提供了新的靶点和思路。
-
为溃疡性结肠炎的治疗提供了新的手段
研究发现重组蛋白EFNB1-Fc具有治疗溃疡性结肠炎的潜力。这一发现为溃疡性结肠炎的治疗提供了新的药物候选,有望为患者带来更好的治疗效果和生活质量。
-
推动了自噬在肠道稳态维持中的研究
本研究进一步证实了自噬在肠道稳态维持中的重要作用。通过揭示RNF186-EFNB1-EPHB2轴诱导的自噬对肠道上皮清除胞内细菌感染的调控机制,为自噬在肠道稳态维持中的研究提供了新的视角和思路。
讨论与展望
本研究揭示了RNF186通过调节EFNB1-EPHB2通路诱导的自噬在溃疡性结肠炎中的重要作用,为溃疡性结肠炎的治疗提供了新的思路和手段。然而,仍有一些问题需要进一步探讨和研究:
-
RNF186变异的分子机制
本研究发现RNF186的两个罕见变异RNF186A64T和RNF186R179X对溃疡性结肠炎的易感性具有不同影响。然而,这些变异的分子机制尚不清楚。未来的研究可以进一步探讨这些变异如何影响RNF186的结构和功能,以及如何通过调控这些变异来预防和治疗溃疡性结肠炎。
-
重组蛋白EFNB1-Fc的临床应用
本研究发现重组蛋白EFNB1-Fc具有治疗溃疡性结肠炎的潜力。然而,该蛋白的临床应用还需要进一步的研究和验证。未来的研究可以评估该蛋白在溃疡性结肠炎患者中的安全性和有效性,并探索其与其他药物的联合使用策略。
-
自噬在IBD中的其他作用
本研究主要关注了自噬在溃疡性结肠炎中的作用。然而,自噬在其他类型的IBD(如克罗恩病)中的作用也值得进一步探讨。未来的研究可以揭示自噬在IBD不同阶段的调控机制和功能差异,为IBD的治疗提供更全面的理解和策略。
| 名称 | 货号 | 规格 |
| Rabbit anti-EFNB1 Polyclonal Antibody | abs136501-100ug | 100ug |
| Anti-RNF186 | HPA034547-25ul | 25ul |
| HA-Tag(C29F4)Rabbit mAb | 3724-5ml | 5ml |
| GFP (B-2) | sc-9996 | 200ug/ml |