上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|Kdm2a在巨噬细胞中的缺失通过增强Pparg位点的H3K36me2促进生热作用,保护小鼠免受高脂饮食诱导的肥胖
113 人阅读发布时间:2025-04-25 11:08
一、引言
肥胖已成为全球性的健康问题,它不仅影响个体的生活质量,还与多种慢性疾病如2型糖尿病、心血管疾病和某些癌症的风险增加密切相关。近年来,随着表观遗传学研究的深入,人们开始认识到基因表达的调控在肥胖及其相关代谢疾病中的重要性。其中,组蛋白去甲基化酶Kdm2a作为一种关键的表观遗传调控因子,在细胞增殖、分化和凋亡等过程中发挥着重要作用。本研究发现,巨噬细胞中Kdm2a的缺失能够通过增强Pparg位点的H3K36me2水平,促进M2型巨噬细胞的极化,进而增强生热作用,保护小鼠免受高脂饮食(HFD)诱导的肥胖。这一发现为肥胖及其相关代谢疾病的治疗提供了新的思路。

二、研究背景
- 肥胖与代谢疾病
肥胖是由于能量摄入超过能量消耗而导致的体内脂肪积累过多。它不仅影响个体的外貌和自信心,更重要的是,肥胖与多种代谢性疾病密切相关,如2型糖尿病、心血管疾病、高血压、血脂异常和某些癌症等。这些疾病给个人和社会带来了巨大的经济负担和健康风险。
- 巨噬细胞极化与代谢调控
巨噬细胞是免疫系统中的重要细胞类型,它们在维持组织稳态、抵御病原体入侵和促进组织修复等方面发挥着关键作用。根据功能和表型的不同,巨噬细胞可以分为M1型和M2型两种。M1型巨噬细胞主要参与炎症反应,具有杀菌和抗肿瘤作用;而M2型巨噬细胞则主要参与组织修复和免疫调节,具有抗炎和促进组织再生的作用。近年来的研究表明,巨噬细胞极化在代谢调控中也发挥着重要作用。M2型巨噬细胞能够促进脂肪酸的摄取和脂解,从而调节能量平衡和代谢稳态。
- Kdm2a与表观遗传调控
Kdm2a是一种组蛋白去甲基化酶,它能够通过催化H3K36me2的去甲基化作用,参与表观遗传调控。H3K36me2是一种重要的组蛋白修饰形式,它与基因表达调控、DNA复制和修复以及细胞周期进程等过程密切相关。Kdm2a通过调节H3K36me2的水平,可以影响染色质的结构和稳定性,从而调控基因的表达模式。近年来的研究表明,Kdm2a在多种疾病的发生和发展中发挥着重要作用,包括肿瘤、心血管疾病和代谢性疾病等。
三、研究方法与结果
- 实验设计
本研究采用基因敲除技术,构建了髓系特异性Kdm2a敲除小鼠(LysM-Cre-Kdm2af/f,Kdm2a-/-)。通过高脂饮食喂养这些小鼠,观察它们对肥胖及其相关代谢疾病的抵抗能力。同时,利用分子生物学和细胞生物学技术,探讨Kdm2a缺失对巨噬细胞极化和生热作用的影响及其机制。
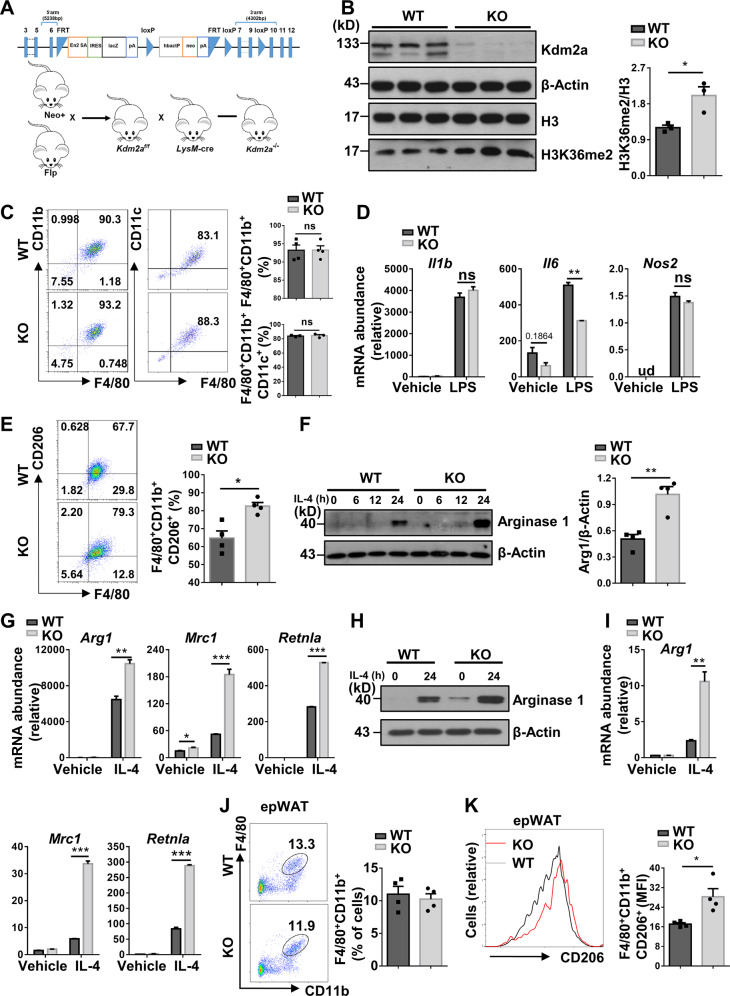
- Kdm2a缺失促进M2型巨噬细胞极化
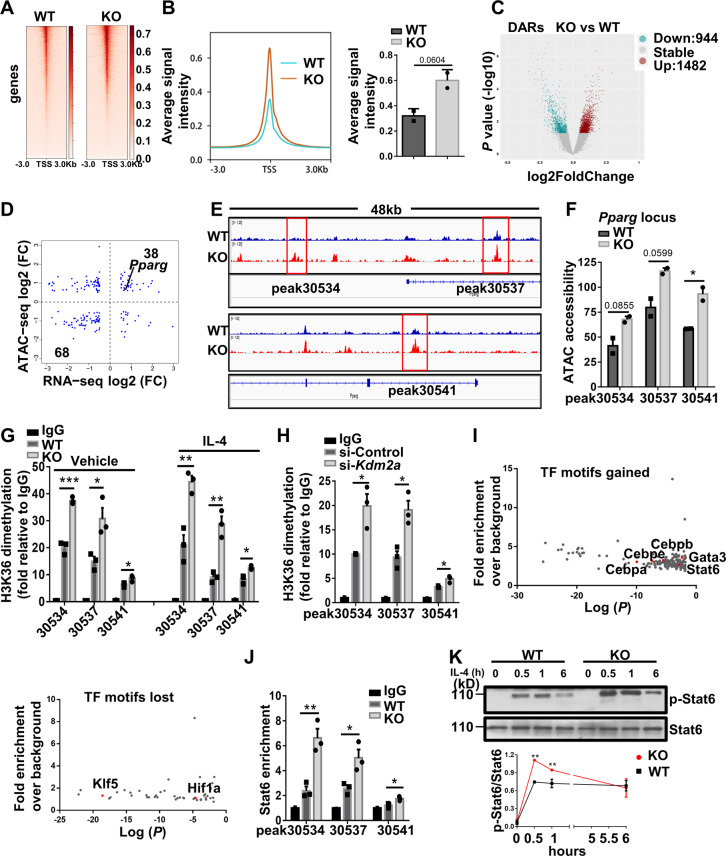
研究结果显示,Kdm2a缺失的巨噬细胞表现出更强的M2型极化特征。这些细胞具有更高的脂肪酸摄取和脂解能力,从而促进了代谢稳态的维持。进一步的研究发现,Kdm2a缺失能够增加Pparg位点H3K36me2的水平,同时增强染色质的可接近性和Stat6的招募。这些变化使得巨噬细胞更倾向于M2型极化,从而发挥抗炎和促进组织再生的作用。
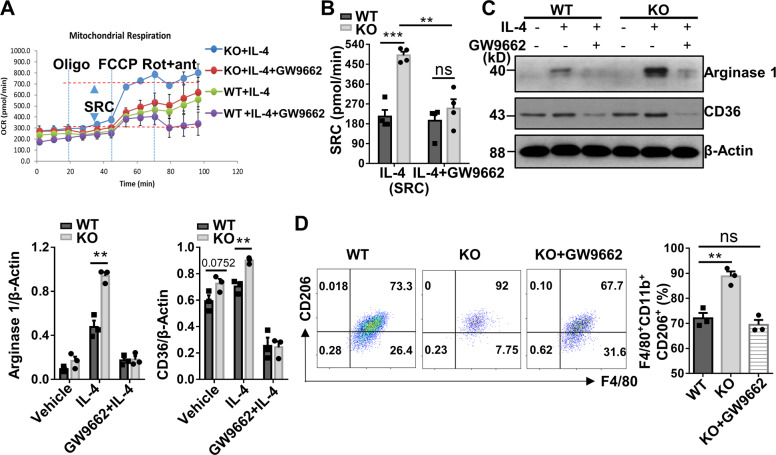
- Kdm2a缺失增强生热作用,抵抗肥胖
在高脂饮食喂养的条件下,Kdm2a缺失的小鼠表现出更强的抵抗肥胖的能力。这些小鼠的体重增长较慢,脂肪组织积累较少,且胰岛素敏感性和肝功能得到改善。进一步的研究发现,Kdm2a缺失的巨噬细胞能够提供一个有利于生热的微环境。在高脂饮食或寒冷刺激下,这些小鼠表现出更高的诱导脂肪棕色化和米色化的能力,从而促进了能量的消耗。这一发现揭示了Kdm2a在调节能量平衡和代谢稳态中的重要作用。
- 机制探讨
为了深入探讨Kdm2a缺失促进M2型巨噬细胞极化和生热作用的机制,研究者进行了进一步的实验。他们发现,Kdm2a缺失能够影响Pparg基因的表达和调控。Pparg是一种重要的核受体转录因子,它在脂肪细胞分化和代谢调控中发挥着关键作用。Kdm2a缺失通过增加Pparg位点H3K36me2的水平,改变了染色质的结构和稳定性,从而影响了Pparg基因的表达模式。这一变化使得巨噬细胞更倾向于M2型极化,并促进了生热作用的发生。
四、研究意义与讨论
- 研究意义
本研究首次揭示了Kdm2a在巨噬细胞极化、生热作用和肥胖抵抗中的重要作用。通过构建髓系特异性Kdm2a敲除小鼠,研究者发现Kdm2a缺失能够促进M2型巨噬细胞的极化,增强生热作用,从而保护小鼠免受高脂饮食诱导的肥胖。这一发现不仅为肥胖及其相关代谢疾病的治疗提供了新的思路,也为表观遗传学在代谢调控中的研究提供了新的视角。
- 机制探讨与未来研究方向
本研究虽然揭示了Kdm2a缺失促进M2型巨噬细胞极化和生热作用的机制,但仍有许多问题有待进一步探讨。例如,Kdm2a是如何影响Pparg基因表达和调控的?除了Pparg之外,是否还有其他基因也参与了这一过程?此外,Kdm2a在其他类型的细胞和疾病中是否也发挥着类似的作用?这些问题都需要进一步的研究来解答。
未来的研究方向可以包括以下几个方面:一是深入探讨Kdm2a影响Pparg基因表达和调控的具体机制;二是寻找其他可能参与Kdm2a缺失促进M2型巨噬细胞极化和生热作用的基因和信号通路;三是研究Kdm2a在其他类型的细胞和疾病中的作用及其机制;四是开发针对Kdm2a的靶向药物或治疗方法,为肥胖及其相关代谢疾病的治疗提供新的手段。
- 临床应用前景与挑战
本研究的结果为肥胖及其相关代谢疾病的治疗提供了新的思路。通过调节Kdm2a的表达或活性,可能可以促进M2型巨噬细胞的极化,增强生热作用,从而改善肥胖及其相关代谢疾病的症状。然而,将这一研究成果应用于临床仍面临许多挑战。例如,如何准确地调节Kdm2a的表达或活性?如何确保治疗的安全性和有效性?如何评估治疗效果并监测可能的副作用?这些问题都需要进一步的研究和临床试验来解答。
尽管如此,本研究的结果仍然为肥胖及其相关代谢疾病的治疗提供了新的希望。随着研究的深入和技术的进步,相信未来会有更多的针对Kdm2a的靶向药物或治疗方法被开发出来,为肥胖及其相关代谢疾病的患者带来更好的治疗效果和生活质量。
五、结论
本研究通过构建髓系特异性Kdm2a敲除小鼠,发现Kdm2a在巨噬细胞极化、生热作用和肥胖抵抗中发挥着重要作用。Kdm2a缺失能够促进M2型巨噬细胞的极化,增强生热作用,从而保护小鼠免受高脂饮食诱导的肥胖。这一发现不仅为肥胖及其相关代谢疾病的治疗提供了新的思路,也为表观遗传学在代谢调控中的研究提供了新的视角。未来的研究将进一步探讨Kdm2a影响M2型巨噬细胞极化和生热作用的具体机制,并开发针对Kdm2a的靶向药物或治疗方法,为肥胖及其相关代谢疾病的治疗提供新的手段。
| 名称 | 货号 | 规格 |
| PPARgamma (81B8) Rabbit mAb | 2443S | 100ul |
| Stat6 (D3H4) Rabbit mAb | 5397T | 20μl |
| Rabbit anti-Phospho-STAT6(Tyr641) Polyclonal Antibody | abs130926-50ug | 50ug |
| CD68 (E-11) | sc-17832 | 200ug/ml |



































