上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|共生细菌通过降低6-巯基嘌呤的生物利用度促进炎症性肠病中硫唑嘌呤治疗失败
211 人阅读发布时间:2025-05-15 13:33
引言
炎症性肠病(Inflammatory Bowel Disease, IBD)是一种慢性、复发性的胃肠道炎症性疾病,主要包括克罗恩病和溃疡性结肠炎两种类型。IBD的治疗策略多样,其中硫唑嘌呤(Azathioprine, AZA)作为一种免疫抑制剂,被广泛应用于IBD的维持治疗中,以减轻炎症、控制病情进展。然而,AZA治疗失败的情况并不罕见,这在一定程度上导致了疾病的复发和进展。尽管AZA治疗失败的原因复杂多样,但近年来,越来越多的研究开始关注肠道微生物群在这一过程中的潜在作用。本文将对一篇题为《Commensal bacteria promote azathioprine therapy failure in inflammatory bowel disease via decreasing 6-mercaptopurine bioavailability》的研究文献进行深度解析,探讨共生细菌如何通过影响6-巯基嘌呤(6-Mercaptopurine, 6-MP)的生物利用度来促进AZA治疗失败。
研究背景与目的
AZA是一种前体药物,在体内通过代谢转化为6-MP,进而发挥免疫抑制作用。然而,AZA治疗失败在IBD患者中并不少见,这限制了其临床应用效果。已有研究表明,肠道微生物群在药物代谢、生物利用度以及疾病进展中扮演着重要角色。然而,关于共生细菌如何影响AZA及其代谢产物6-MP的生物利用度,以及这一机制如何导致AZA治疗失败的具体过程,尚缺乏深入研究。因此,本研究旨在探究共生细菌在AZA治疗失败中的作用机制,为IBD的精准治疗提供新的思路。
研究方法
- 样本收集与分析:研究者首先收集了IBD患者的粪便样本,通过高通量测序技术分析了肠道微生物群的组成。同时,结合患者的临床数据,评估了AZA治疗失败与肠道微生物群之间的关系。
- 动物实验:为了验证共生细菌对AZA治疗失败的影响,研究者构建了小鼠结肠炎模型,并通过灌胃方式引入了特定共生细菌,观察其对AZA治疗效果的影响。
- 药物代谢研究:研究者还分析了共生细菌对6-MP生物利用度的影响,通过测定小鼠体内6-MP及其代谢产物的浓度,探讨了共生细菌如何通过影响药物代谢来促进AZA治疗失败。
- 机制探究:为了深入了解共生细菌影响AZA治疗效果的机制,研究者进一步分析了共生细菌对肠道免疫细胞的影响,以及如何通过调节硒依赖性黄嘌呤脱氢酶(Selenium-dependent Xanthine Dehydrogenase, sd-XDH)活性来影响6-MP的生物利用度。
研究结果
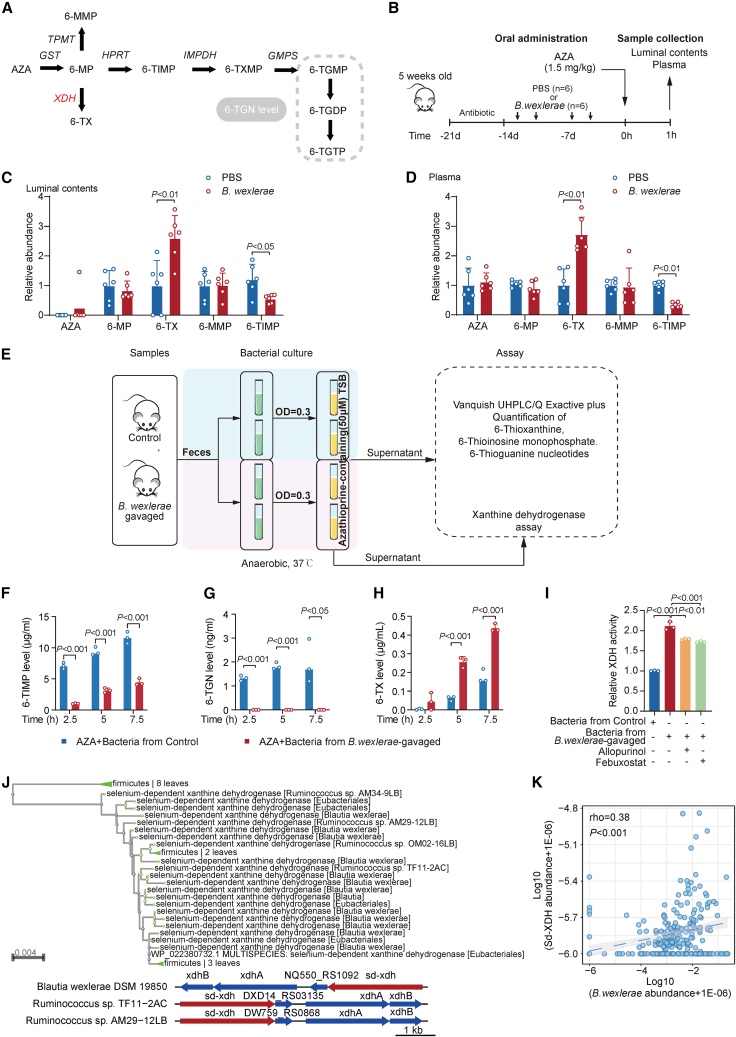
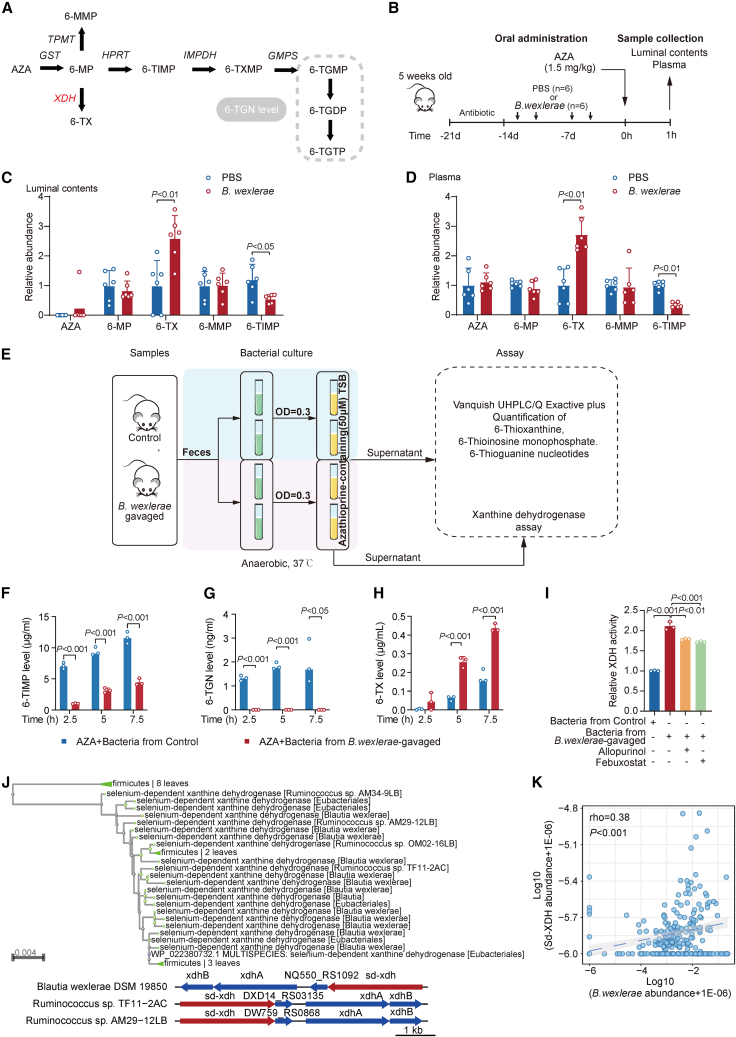
- 共生细菌与AZA治疗失败的关系:研究发现,在AZA治疗失败的IBD患者中,Blautia wexlerae(一种共生细菌)的丰度显著升高。此外,Blautia wexlerae的丰度与疾病复发时间呈负相关,即Blautia wexlerae丰度越高,疾病复发时间越短。
- 共生细菌对AZA治疗效果的影响:动物实验结果显示,引入Blautia wexlerae的小鼠在AZA治疗后,结肠炎症状更加严重,治疗效果明显减弱。这表明Blautia wexlerae能够影响AZA的治疗效果。
- 共生细菌对6-MP生物利用度的影响:研究者发现,Blautia wexlerae能够通过增强sd-XDH活性,将6-MP转化为其无活性的代谢产物6-噻黄嘌呤(6-Thioxanthine, 6-TX),从而降低6-MP的生物利用度。这一发现揭示了共生细菌影响AZA治疗效果的具体机制。
- 机制探究:进一步的研究表明,Blautia wexlerae能够增加肠道中炎性巨噬细胞的数量,这些细胞能够分泌促炎因子,进一步加剧肠道炎症。同时,Blautia wexlerae还能够通过调节sd-XDH活性,影响6-MP的代谢过程,从而降低AZA的治疗效果。
- 潜在的治疗策略:研究者还发现,补充富含次黄嘌呤磷酸核糖转移酶(Hypoxanthine Phosphoribosyltransferase, HPRT)的枯草芽孢杆菌(Bacillus subtilis)能够有效缓解Blautia wexlerae引起的AZA治疗失败。这表明通过调节肠道微生物群,可能为提高AZA的治疗效果提供新的途径。
研究意义与讨论
本研究首次揭示了共生细菌Blautia wexlerae在AZA治疗失败中的关键作用,以及这一机制如何通过影响6-MP的生物利用度来实现。这一发现不仅为IBD的精准治疗提供了新的思路,也为理解肠道微生物群在药物代谢和疾病进展中的作用提供了重要依据。
- 精准治疗:根据本研究的结果,未来的IBD治疗策略可以更加关注患者的肠道微生物群组成,特别是Blautia wexlerae的丰度。对于Blautia wexlerae丰度较高的患者,可以考虑采用其他免疫抑制剂或调整治疗方案,以提高治疗效果。
- 微生物群调节:本研究还发现,通过补充特定益生菌(如枯草芽孢杆菌)可以调节肠道微生物群,从而缓解AZA治疗失败。这提示我们,在未来的IBD治疗中,可以尝试结合益生菌治疗,以优化治疗效果。
- 药物研发:本研究的结果也为新型IBD药物的研发提供了启示。未来的药物研发可以更加关注药物在肠道微生物群中的代谢过程,以及如何通过调节肠道微生物群来提高药物的生物利用度和治疗效果。
然而,本研究也存在一些局限性。例如,样本量相对较小,可能限制了研究结果的普遍性和准确性。此外,本研究主要集中在Blautia wexlerae这一种共生细菌上,而肠道微生物群是一个复杂的生态系统,其他共生细菌也可能对AZA的治疗效果产生影响。因此,未来的研究需要进一步扩大样本量,并深入探究其他共生细菌在AZA治疗失败中的作用机制。
结论与展望
本研究揭示了共生细菌Blautia wexlerae在AZA治疗失败中的关键作用,以及这一机制如何通过影响6-MP的生物利用度来实现。这一发现不仅为IBD的精准治疗提供了新的思路,也为理解肠道微生物群在药物代谢和疾病进展中的作用提供了重要依据。未来的研究可以进一步探究其他共生细菌在AZA治疗失败中的作用机制,以及如何通过调节肠道微生物群来提高AZA的治疗效果。同时,也可以尝试结合益生菌治疗等新型治疗手段,以优化IBD的治疗效果,提高患者的生活质量。
| 名称 | 货号 | 规格 |
| APC-R700 Rat Anti-Mouse F4/80(T45-2342) | 565787 | 50ug |
| Fixable Viability Stain 510 | 564406 | 100ug |
| BV605 Rat Anti-Mouse Ly-6C(AL-21) | 563011 | 50ug |
| Ms CD8a PE 53-6.7 100ug | 553032 | 100ug |