上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|近红外光触发一氧化氮释放促进脊髓损伤修复
190 人阅读发布时间:2025-05-22 14:15
引言
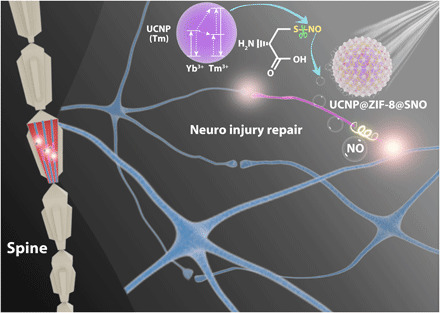
脊髓损伤(SCI)是一种由外部物理冲击引起的严重神经系统损伤,可导致复杂的级联反应,最终可能导致瘫痪。这种损伤不仅严重影响患者的生活质量,也给社会和家庭带来沉重负担。然而,现有的临床药物对脊髓损伤的治疗效果有限,主要是因为血脊髓屏障(BSCB)通透性较差或药物功能单一。近期,一项发表在《Science Advances》上的研究提出了一种基于近红外(NIR)光触发的“多效信使”策略,该策略通过按需释放一氧化氮(NO)来促进脊髓损伤的修复。

研究背景
SCI后,损伤部位的微环境发生显著变化,包括炎症反应、胶质增生和神经元凋亡等,这些变化严重阻碍了神经功能的恢复。传统的治疗方法如药物治疗、物理治疗等,虽然在一定程度上能够缓解病情,但往往无法从根本上解决SCI导致的神经功能障碍。因此,开发一种新型、高效的治疗方法对于SCI患者来说至关重要。
NO作为一种具有多种生物学活性的小分子物质,在心血管系统、神经系统和免疫系统中均发挥着重要作用。近年来,越来越多的研究开始关注NO在SCI治疗中的应用潜力。然而,如何实现NO在损伤部位的精准释放和有效控制,仍是当前研究的难点之一。
研究方法
本研究提出了一种基于NIR光触发的NO释放系统,该系统由包覆有沸石咪唑框架-8(ZIF-8)和一氧化氮供体(CysNO)的上转换纳米粒子(UCNP)核心构成。该系统能够在NIR光的照射下,实现NO的按需释放,从而实现对SCI的精准治疗。
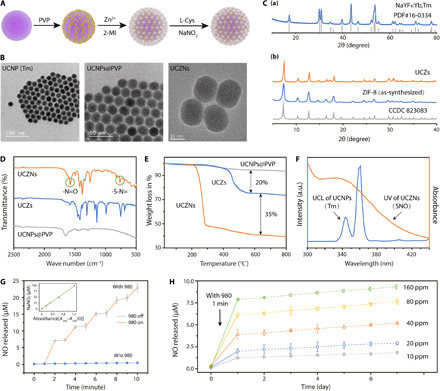
具体而言,研究者首先合成了UCNP核心,并在其表面包覆了ZIF-8框架,同时引入了CysNO作为NO供体。通过优化合成条件,研究者得到了具有优异稳定性和生物相容性的NO释放系统。随后,研究者利用NIR光照射该系统,观察NO的释放情况,并评估了其对SCI的治疗效果。
研究结果
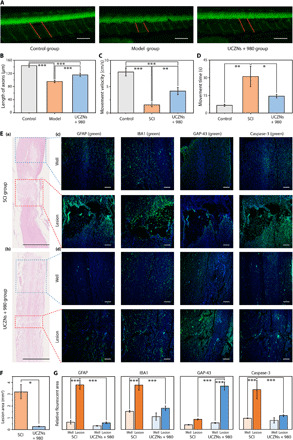
研究结果显示,该NO释放系统能够在NIR光的照射下实现NO的精准释放,且释放量可通过调整NIR光的强度和照射时间来控制。通过将该系统应用于SCI大鼠模型中,研究者发现该系统能够显著促进神经元的再生和神经保护,同时抑制胶质增生和炎症反应,从而实现对SCI的有效治疗。
进一步的研究表明,该NO释放系统的治疗效果主要归因于NO的多效作用,包括抑制胶质增生和炎症反应、促进神经再生以及保护神经元免受凋亡等。这些作用共同促进了SCI后神经功能的恢复。
结果分析
- NO的多效作用:NO作为一种多效信号分子,在SCI治疗中发挥着重要作用。本研究发现,NO能够抑制胶质增生和炎症反应,这有助于减轻损伤部位的微环境恶化,为神经再生创造有利条件。同时,NO还能促进神经元的再生和神经保护,这直接促进了神经功能的恢复。此外,NO还能保护神经元免受凋亡,从而进一步提高了SCI的治疗效果。
- NIR光触发的精准释放:传统的NO释放方法往往难以实现NO的精准释放和有效控制。本研究提出的NIR光触发NO释放系统,能够在NIR光的照射下实现NO的精准释放,且释放量可通过调整NIR光的强度和照射时间来控制。这种精准释放方式有助于避免NO的过量释放和潜在副作用,提高了SCI治疗的安全性和有效性。
- 系统的生物相容性和稳定性:本研究制备的NO释放系统具有良好的生物相容性和稳定性,能够在体内长时间稳定存在并发挥治疗作用。这对于SCI的长期治疗具有重要意义。
讨论
本研究提出的NIR光触发NO释放系统为SCI的治疗提供了一种新的思路和方法。然而,在实际应用中,仍需考虑以下几个方面的问题:
- 系统的优化和改进:虽然本研究制备的NO释放系统已经取得了显著的治疗效果,但仍需进一步优化和改进。例如,可以通过调整UCNP的组成和结构,提高NO的释放效率和生物利用度;同时,也可以探索其他NO供体和载体材料,以进一步提高系统的治疗效果和安全性。
- 与其他治疗方法的结合:SCI的治疗需要综合考虑多种因素,包括神经损伤的程度、患者的身体状况等。因此,在实际应用中,可以将本研究提出的NIR光触发NO释放系统与其他治疗方法相结合,如细胞移植、药物治疗等,以实现更好的治疗效果。
- 临床试验的推进:尽管本研究已经在动物模型中取得了显著的治疗效果,但仍需进行临床试验以验证其安全性和有效性。在未来的研究中,可以进一步探索该系统的临床应用前景,为SCI患者带来更好的治疗选择。
结论
本研究提出了一种基于NIR光触发的NO释放系统,用于促进脊髓损伤的修复。该系统能够在NIR光的照射下实现NO的精准释放,并通过NO的多效作用促进神经元的再生和神经保护,同时抑制胶质增生和炎症反应。通过将该系统应用于SCI大鼠模型中,研究者发现该系统能够显著促进神经功能的恢复。这一研究成果不仅为SCI的治疗提供了一种新的思路和方法,也为未来的神经科学研究、组织工程等领域提供了新的启示和借鉴。
对未来研究的展望
随着对SCI发病机制和治疗方法的深入研究,越来越多的新型治疗方法不断涌现。本研究提出的NIR光触发NO释放系统作为其中的一种,具有广阔的应用前景和深远的意义。在未来的研究中,可以进一步探索该系统的优化和改进方法,以提高其治疗效果和安全性;同时,也可以结合其他治疗方法,如细胞移植、基因治疗等,以实现更好的治疗效果。此外,还可以进一步探索NO在SCI治疗中的其他作用机制,为SCI的治疗提供更加全面和深入的认识。
总之,本研究为SCI的治疗提供了一种新的思路和方法,也为未来的神经科学研究、组织工程等领域提供了新的启示和借鉴。相信在未来的研究中,随着对SCI发病机制和治疗方法的不断深入了解,我们将会为SCI患者带来更加有效和安全的治疗方法。
| 名称 | 货号 | 规格 |
| Native mouse NGF 2.5S protein (>95%) | N-100-50ug | 50ug |
| Native mouse NGF 2.5S protein (>95%) | N-100-0.5mg | 0.5mg |
| Native mouse NGF 2.5S protein (>95%) | N-100-0.1mg | 0.1mg |
| Native mouse NGF 2.5S protein (>95%) | N-100-10ug | 10ug |