上海优宁维生物科技股份有限公司代理商
19 年
手机商铺
- NaN
- 0
- 0
- 2
- 2
技术资料/正文
文献解析|肝细胞特异性Nrf2缺乏减轻高脂饮食诱导的肝脂肪变性——PPARγ表达降低的作用探讨
260 人阅读发布时间:2025-07-11 15:09
一、引言与研究背景概览
非酒精性脂肪肝病(NAFLD)已成为全球范围内日益普遍的慢性疾病,其复杂的发病机制尚未完全明晰。NAFLD不仅影响肝脏健康,还与代谢综合征、2型糖尿病及心血管疾病等紧密相关,对人类健康构成严重威胁。近年来,针对NAFLD发病机制的探索不断深入,特别是细胞特异性因子在疾病进展中的作用备受关注。本文将深入解析一篇题为《Hepatocyte-specific Nrf2 deficiency mitigates high-fat diet-induced hepatic steatosis: Involvement of reduced PPARγ expression》的文献,该研究通过构建肝细胞特异性Nrf2敲除小鼠模型,揭示了Nrf2在肝细胞中对高脂饮食诱导肝脂肪变性的影响,并探讨了其潜在的分子机制。
二、研究设计与实验方法
实验动物模型的构建
研究者首先利用基因编辑技术,构建了肝细胞特异性(Nrf2(L)-KO)和巨噬细胞特异性(Nrf2(Mϕ)-KO)的Nrf2敲除小鼠,以及相应的Nrf2-LoxP对照小鼠。这些小鼠模型为探究Nrf2在不同细胞类型中对NAFLD进展的影响提供了关键工具。
高脂饮食诱导与表型分析
随后,研究者将上述小鼠置于高脂饮食(HFD)条件下,并观察其肝脏形态、炎症反应及脂肪变性程度的变化。通过组织学分析、生化指标检测等手段,全面评估了Nrf2缺乏对不同细胞类型中NAFLD进展的影响。
分子机制探讨
在观察到肝细胞特异性Nrf2缺乏能够减轻HFD诱导的肝脂肪变性后,研究者进一步探讨了其潜在的分子机制。通过实时荧光定量PCR、Western blot等分子生物学技术,检测了肝细胞中过氧化物酶体增殖物激活受体γ(PPARγ)及其下游脂生成基因的表达水平,以揭示Nrf2与PPARγ之间的相互作用关系。
三、研究结果与深入分析
肝细胞特异性Nrf2缺乏对HFD诱导肝脂肪变性的保护作用
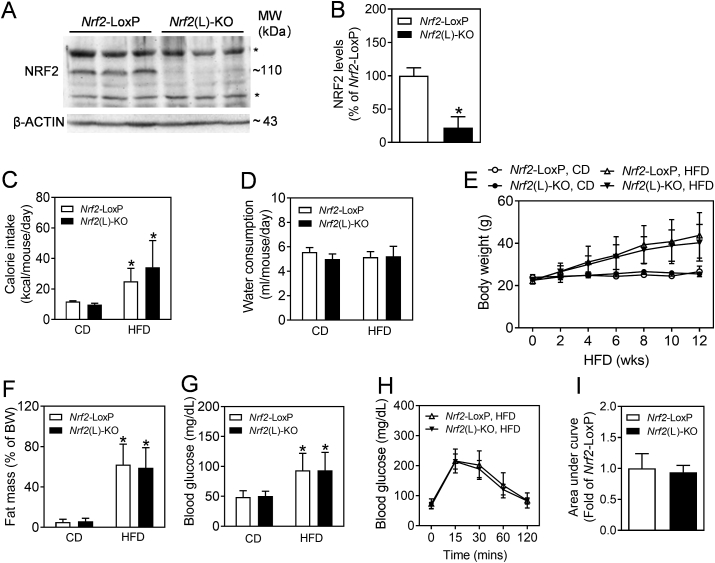
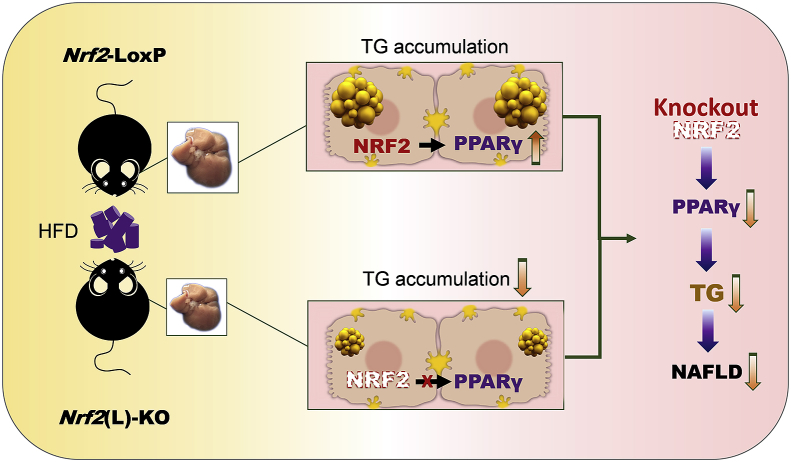
研究结果显示,与Nrf2-LoxP对照小鼠相比,肝细胞特异性Nrf2敲除小鼠(Nrf2(L)-KO)在HFD喂养后表现出肝脏肿大程度减轻、炎症反应减弱及肝脂肪变性程度降低的表型。这一发现首次揭示了肝细胞中Nrf2在促进NAFLD进展中的重要作用。
巨噬细胞特异性Nrf2缺乏对HFD诱导肝脂肪变性的影响有限
与肝细胞特异性敲除结果不同,巨噬细胞特异性Nrf2敲除小鼠(Nrf2(Mϕ)-KO)在HFD喂养后的肝脂肪变性程度与Nrf2-LoxP对照小鼠无显著差异。这一结果表明,巨噬细胞中的Nrf2对NAFLD进展的影响相对较小,进一步强调了肝细胞在NAFLD发病中的核心地位。
Nrf2缺乏抑制PPARγ及其下游脂生成基因的表达
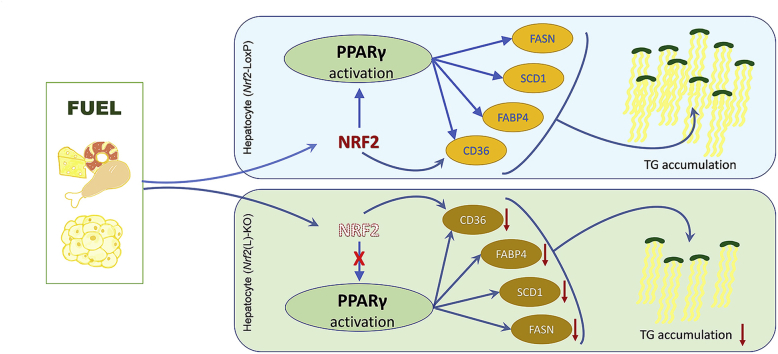
在分子机制探讨方面,研究者发现肝细胞特异性Nrf2缺乏能够显著抑制PPARγ及其下游脂生成基因(如脂肪酸结合蛋白4、脂蛋白脂酶及脂肪酸合成酶)的表达。这一发现揭示了Nrf2与PPARγ之间的相互作用关系,并提示Nrf2可能通过调控PPARγ及其下游信号通路来促进NAFLD进展。
PPARγ激动剂及过表达对Nrf2缺乏效应的逆转作用
为了进一步验证Nrf2与PPARγ之间的相互作用关系,研究者使用了PPARγ激动剂及过表达技术。结果显示,PPARγ激动剂能够以NRF2依赖的方式增强肝细胞中PPARγ的表达及其转录活性;而过表达PPARγ1或γ2则能够逆转由Nrf2缺乏引起的下游基因表达降低。这些结果进一步证实了Nrf2在调控PPARγ及其下游信号通路中的关键作用,并为NAFLD的潜在治疗策略提供了新思路。
四、讨论与展望
本研究通过构建肝细胞特异性Nrf2敲除小鼠模型,揭示了Nrf2在肝细胞中对高脂饮食诱导肝脂肪变性的影响及其潜在的分子机制。研究结果不仅加深了我们对NAFLD发病机制的理解,还为疾病的治疗提供了新的靶点和思路。
Nrf2与PPARγ的相互作用关系
本研究发现Nrf2能够调控PPARγ及其下游脂生成基因的表达,从而参与NAFLD的进展。这一发现为我们揭示了Nrf2与PPARγ之间的相互作用关系,并提示我们未来可以通过干预这一信号通路来治疗NAFLD。
肝细胞在NAFLD发病中的核心地位
通过对比肝细胞和巨噬细胞特异性Nrf2敲除小鼠的表型差异,本研究进一步强调了肝细胞在NAFLD发病中的核心地位。这一发现为我们未来的研究提供了方向,即应更加关注肝细胞在NAFLD进展中的作用及其相关信号通路的调控。
潜在的治疗策略与展望
基于本研究的结果,我们可以设想一些潜在的治疗策略。例如,通过抑制肝细胞中的Nrf2活性或降低PPARγ的表达水平,可能能够减轻NAFLD的进展。此外,针对Nrf2与PPARγ相互作用通路的靶向药物也可能成为治疗NAFLD的新选择。然而,这些策略的有效性和安全性尚需进一步的临床试验验证。
五、结论
综上所述,《Hepatocyte-specific Nrf2 deficiency mitigates high-fat diet-induced hepatic steatosis: Involvement of reduced PPARγ expression》一文通过构建肝细胞特异性Nrf2敲除小鼠模型,深入探讨了Nrf2在肝细胞中对高脂饮食诱导肝脂肪变性的影响及其潜在的分子机制。研究结果不仅为我们揭示了Nrf2与PPARγ之间的相互作用关系,还为NAFLD的治疗提供了新的靶点和思路。未来,我们将继续深入研究这一信号通路在NAFLD进展中的作用及其调控机制,以期为患者带来更有效的治疗方案。
| 名称 | 货号 | 规格 |
| PPARgamma (C26H12) Rabbit mAb | 2435T | 20ul |
| PPARgamma (C26H12) Rabbit mAb | 2435S | 100ul |
| α Tubulin (B-7) | sc-5286 | 200μg/ml |
| F4/80 (C-7) | sc-377009 | 200μg/ml |